题目内容
氮的某种氧化物中,氮元素与氧元素的质量比为7:16,则该氧化物化学式为 ,该氧化物中氮的化合价为 ,该氧化物的相对分子质量为 .
考点:元素质量比的计算,有关元素化合价的计算,相对分子质量的概念及其计算
专题:化学式的计算
分析:氮的某种氧化物中,氮元素与氧元素的质量比为7:16,则可设氮的某种氧化物化学式为NxOy;相对分子质量为构成分子的各原子的相对原子质量之和,在化合物中正负化合价代数和为零,进行分析解答.
解答:解:
由题意,氮的某种氧化物中,氮元素与氧元素的质量比为7:16,则可设氮的某种氧化物化学式为NxOy;则
=
,则1个该氮的某种氧化物中氮原子和氧原子的个数比为x:y=1:2,该氮的某种氧化物的化学式为NO2.
因为氧元素显-2价,设氮元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-2)×2=0,则x=+4价.
其相对分子质量为14+16×2=46.
故答案为:
NO2;+4价;46.
由题意,氮的某种氧化物中,氮元素与氧元素的质量比为7:16,则可设氮的某种氧化物化学式为NxOy;则
| 14x |
| 16y |
| 7 |
| 16 |
因为氧元素显-2价,设氮元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-2)×2=0,则x=+4价.
其相对分子质量为14+16×2=46.
故答案为:
NO2;+4价;46.
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案
相关题目
在MgO中,镁元素和氧元素的质量比为( )
| A、3:2 | B、2:3 |
| C、3:4 | D、4:3 |
 小华同学在准备“对蜡烛及其燃烧的探究活动”时,发现实验室有许多用剩下的小蜡烛头,感觉浪费了太可惜.于是实验小组决定自己动手用小蜡烛头为原料制造蜡烛.过程如图:
小华同学在准备“对蜡烛及其燃烧的探究活动”时,发现实验室有许多用剩下的小蜡烛头,感觉浪费了太可惜.于是实验小组决定自己动手用小蜡烛头为原料制造蜡烛.过程如图:
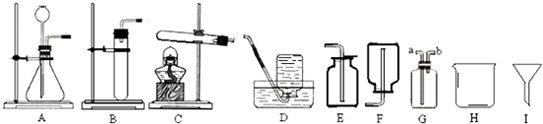
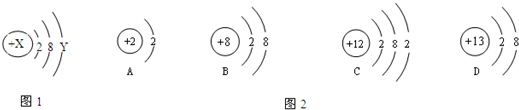
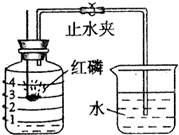 已知空气的主要成分是氮气和氧气.某课外活动小组设计了测定空气中氧气含量的实验,实验装置如图所示.
已知空气的主要成分是氮气和氧气.某课外活动小组设计了测定空气中氧气含量的实验,实验装置如图所示.