题目内容
某同学欲测定草木灰中碳酸钾的含量,称取69g试样于烧杯中,加入29.2g稀盐酸恰好完全反应,充分反应后,称得混合物的总质量为93.8g(忽略二氧化碳的溶解对质量的影响).请计算:(1)反应过程中产生的二氧化碳质量为______g.
(2)该草木灰试样中碳酸钾的质量分数.
【答案】分析:(1)反应前后烧杯中的物质减少的质量为二氧化碳的质量.
(2)根据二氧化碳的质量求出碳酸钾的质量,再根据 %,求出草木灰中碳酸钾的质量分数.
%,求出草木灰中碳酸钾的质量分数.
解答:解:(1)69g+29.2g-93.8g=4.4g 故答案为:4.4
(2)设碳酸钾的质量为x
K2CO3+2HCl=2KCl+H2O+CO2↑
138 44
x 4.4g
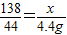
x=13.8g
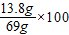 %=20% 答:草木灰中碳酸钾的质量分数为20%.
%=20% 答:草木灰中碳酸钾的质量分数为20%.
点评:稀盐酸是混合物,其溶质是氯化氢气体,根据化学方程式进行计算时不能将稀盐酸的质量作为反应物的质量直接代入进行计算.
(2)根据二氧化碳的质量求出碳酸钾的质量,再根据
 %,求出草木灰中碳酸钾的质量分数.
%,求出草木灰中碳酸钾的质量分数.解答:解:(1)69g+29.2g-93.8g=4.4g 故答案为:4.4
(2)设碳酸钾的质量为x
K2CO3+2HCl=2KCl+H2O+CO2↑
138 44
x 4.4g
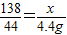
x=13.8g
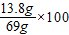 %=20% 答:草木灰中碳酸钾的质量分数为20%.
%=20% 答:草木灰中碳酸钾的质量分数为20%.点评:稀盐酸是混合物,其溶质是氯化氢气体,根据化学方程式进行计算时不能将稀盐酸的质量作为反应物的质量直接代入进行计算.

练习册系列答案
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目