题目内容
若A、B、C为三种金属,根据下列化学反应,推断出A、B、C三种金属的活动性顺序由强到弱依次为①A+B(NO3)2=A(NO3)2 +B②C+B(NO3)2=C(NO3)2 +B,③A+H2SO4=ASO4 +H2↑④C与硫酸不反应( )
分析:金属和盐溶液反应时,前面的金属可以把排在它后面的金属从盐溶液中置换出来,而金属和酸溶液反应时,只有在金属活动性顺序表中排在H前的金属才能把酸溶液中的氢离子置换出来.
解答:解:由于A可以把B从盐溶液中置换出来,说明A的金属活动性比B强,而C也可以把B从盐溶液中置换出来,说明C的金属活动性也比B强,A可以把氢置换出来,而C不行,说明在金属活动性表中,A在氢前而C在氢后.即:A>C>B.
故选B.
故选B.
点评:此题是对金属活动性顺序的考查,解题的关键是掌握金属活动性顺序表的实际应用,主要有:①排在氢前面的金属能和酸反应生成氢气,②排在前面的金属能把它后面的金属从盐溶液中置换出来.

练习册系列答案
相关题目


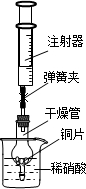
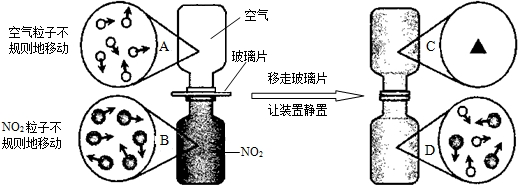
 根据题意填空:
根据题意填空: ,若X等于11,则该微粒表示
,若X等于11,则该微粒表示 B、
B、 C、
C、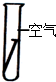 D、
D、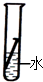
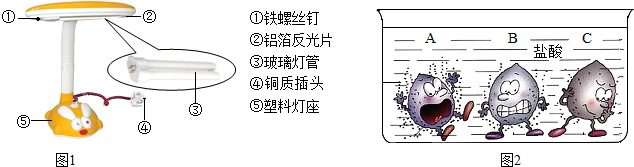
 ①右图所示的台灯,序号标示的物质中属于金属材料的有 ▲ (填序号);小明发现台灯的铁螺丝钉表面已经锈蚀,原因是铁与空气中的氧气及 ▲ 等发生了化学反应。
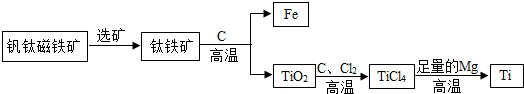
①右图所示的台灯,序号标示的物质中属于金属材料的有 ▲ (填序号);小明发现台灯的铁螺丝钉表面已经锈蚀,原因是铁与空气中的氧气及 ▲ 等发生了化学反应。 ①A、B、C三种金属的活动性由强到弱的顺序是
①A、B、C三种金属的活动性由强到弱的顺序是