题目内容
已知反应CuCl2 + 2NaOH = Cu(OH)2↓+ 2NaCl。向一定量盐酸和氯化铜溶液的混合物中逐滴加入氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如下图所示。下列说法正确的是

A.P点表示的溶液pH="7"
B.M点表示的溶液中只含有一种溶质
C.从M点到N点溶液质量增加20 g
D.P点表示的溶液比N点表示的溶液中氯化钠的质量分数小
【答案】
D
【解析】
试题分析:向一定量盐酸和氯化铜溶液的混合物中逐滴加入氢氧化钠溶液,则盐酸先与氢氧化钠反应,反应结束后,氢氧化钠将与氯化铜反应,生成氢氧化铜沉淀。
P点表示氢氧化钠溶液已经过量,溶液pH大于7;
M点表示盐酸与氢氧化钠恰好反应完全,此时溶液中含有氯化钠和氯化铜;
从M点到N点表示,滴入了20g氢氧化钠溶液,溶液质量增加小于20 g,因为这个过程中有氢氧化铜沉淀产生;
P点表示的溶液比N点表示的溶液中氯化钠的质量分数小,因为此时又滴入了较多的氢氧化钠溶液。
选D。
考点:化学反应中的数量变化关系;溶液的组成;溶液中溶质的质量分数。
点评:读懂题中图示的含义是解题的关键,溶液是由溶剂和溶解了的溶质组成的;
溶质质量分数=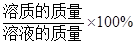 。
。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
已知反应CuCl2 + 2NaOH = Cu(OH)2↓+ 2NaCl。向一定量盐酸和氯化铜溶液的混合物中逐滴加入氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如下图所示。下列说法正确的是
| A.P点表示的溶液pH="7" |
| B.M点表示的溶液中只含有一种溶质 |
| C.从M点到N点溶液质量增加20 g |
| D.P点表示的溶液比N点表示的溶液中氯化钠的质量分数小 |
 (2012?西城区一模)已知反应CuCl2+2NaOH=Cu(OH)2↓+2NaCl.向一定量盐酸和氯化铜溶液的混合物中逐滴加入氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示.下列说法正确的是( )
(2012?西城区一模)已知反应CuCl2+2NaOH=Cu(OH)2↓+2NaCl.向一定量盐酸和氯化铜溶液的混合物中逐滴加入氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示.下列说法正确的是( )

