题目内容
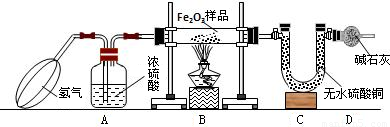
(2004?黄冈)下列化学方程式符合题意,且书写正确的是( )
分析:A、根据锌的化合价是+2价进行分析;
B、根据氢氧化钠只和氯化氢反应不和氢气反应进行分析;
C、根据铜不和硫酸反应进行分析;
D、根据铁锈的主要成分是氧化铁进行分析.
B、根据氢氧化钠只和氯化氢反应不和氢气反应进行分析;
C、根据铜不和硫酸反应进行分析;
D、根据铁锈的主要成分是氧化铁进行分析.
解答:解:A、生成物错误,锌元素的化合价为+2价,正确的化学方程式为:3Zn+2FeCl3=3ZnCl2+2Fe,故A错误;
B、氢氧化钠只和氯化氢反应不和氢气反应,故氢氧化钠可以吸收氢气中含有的少量氯化氢气体,化学方程式完全正确,故B正确;
C、铜排在氢的后面,不能与酸反应,故C错误;
D、氧化铁的主要成分是氧化铁,正确的方程式为:6HCl+Fe2O3=2FeCl3+3H2O,故D正确;
故选BD
B、氢氧化钠只和氯化氢反应不和氢气反应,故氢氧化钠可以吸收氢气中含有的少量氯化氢气体,化学方程式完全正确,故B正确;
C、铜排在氢的后面,不能与酸反应,故C错误;
D、氧化铁的主要成分是氧化铁,正确的方程式为:6HCl+Fe2O3=2FeCl3+3H2O,故D正确;
故选BD
点评:在解此类题时,首先分析应用的原理是否正确,然后再根据方程式的书写规则进行判断.

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目