题目内容
将0.4%的氢氧化钠溶液滴加到2mL0.4%的盐酸中,测得混合液的pH变化曲线如图.某学习小组对加入0~VmL氢氧化钠过程中,所得混合液pH增大原因进行了如下探究:
【猜想假设】
猜想Ⅰ:pH增大是因为 ;
猜想Ⅱ:pH增大是因为发生了反应,写出反应方程式 .
【实验探究】
为验证猜想Ⅱ,请你帮助该小组完成下列实验.(可供选择的实验用品有:pH计、0.4%的氢氧化钠溶液、0.4%的盐酸、水.)
(1)向2mL0.4%的盐酸中加入VmL0.4%的氢氧化钠溶液,用pH计测得混合液的pH=7.
(2)向2mL0.4%的盐酸中加入VmL ,用pH计测得混合液的pH 7(填“>”、“=”或“<”).
综合(1)和(2)证明猜想Ⅱ成立.

考点:
中和反应及其应用;溶液的酸碱性与pH值的关系;书写化学方程式、文字表达式、电离方程式.
专题:
科学探究.
分析:
稀盐酸显酸性,pH小于7,氢氧化钠溶液显碱性,pH大于7;
稀盐酸和氢氧化钠反应生成氯化钠和水.
解答:
解:【猜想假设】
猜想Ⅰ:pH增大是因为混合后溶液体积增大,溶液体积变大时,氢离子浓度变小,pH升高;
猜想Ⅱ:pH增大是因为发生了反应,稀盐酸和氢氧化钠反应的化学方程式为:NaOH+HCl=NaCl+H2O.
故填:混合后溶液体积增大;NaOH+HCl=NaCl+H2O.
【实验探究】
(1)向2mL0.4%的盐酸中加入VmL0.4%的氢氧化钠溶液,用pH计测得混合液的pH=7,说明稀盐酸和氢氧化钠发生了中和反应.
(2)向2mL0.4%的盐酸中加入VmL水,用pH计测得混合液的pH<7,通过比较可知猜想Ⅱ成立.
故填:水;<.
点评:
实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

 出彩同步大试卷系列答案
出彩同步大试卷系列答案根据下列实验装置图,回答问题
| 发生装置 | 收集装置 | 洗气装置 |
|
|
|
|
写出图中仪器a的名称: 。
(2) 实验室用加热氯酸钾和二氧化锰混合物制取氧气的化学方程式为 ,
可选择的发生装置为 (填字母)。
(3) 实验室用石灰石和稀盐酸反应制取二氧化碳的化学方程式为 ,
该反应生成的二氧化碳中常混有少量氯化氢气体,可通过盛有饱和碳酸氢钠溶液的F装置除去氯化氢气体,则该混合气体应从F装置的 口(填“①”或“②”)通入。
下列4个图形能正确反映对应变化关系的是( )

|
| A. | ①向一定量稀硫酸中加入NaOH溶液 |
|
| B. | ②向一定量CuSO4溶液中加入Zn粉 |
|
| C. | ③加热KClO3与MnO2固体混合物 |
|
| D. | ④向一定量NaOH和Ca(OH)2的混合溶液中加入Na2CO3溶液 |
质量为50g溶质质量分数为20%的氢氧化钾溶液和质量为50g溶质质量分数为20%的稀硫酸混合,所得溶液的PH( )
|
| A. | 小于7 | B. | 等于7 | C. | 大于7 | D. | 不确定 |
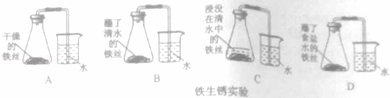
铁生锈探秘
为探究铁生锈的原因,化学兴趣小组的同学进行了如图所示的四个实验,实验结果显示:B、D实验中铁生了锈,而A、C实验中没有明显的现象,仔细分析这4 个实验,回答下列问题:
(1)评价方案
对照实验指除了一个变量外,其他的量都保持不变的实验.该实验方案中采用了对照实验方法.请指出其中的对照实验(填ABCD实验代号)和变量.
第①组对照实验 ,变量 .
第②组对照实验 ,变量 .
第③组对照实验 ,变量 .
(2)解释数据
实验时,每隔一段时间测量导管内水面上升的高度,结果如下表所示(表中所列数据为导管中水面上升的高度/cm )
| 时间/小时 | 0 | 0.5 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
| A | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| B | 0 | 0 | 0 | 0.3 | 0.8 | 2.0 | 3.5 |
| C | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| D | 0 | 0.4 | 1.2 | 3.4 | 7.6 | 9.5 | 9.8 |
导致B、D实验装置中导管内水面上升的原因是 .
(3)获得结论
根据本实验,你认为导致铁生锈的物质有 ;能加快铁生锈的物质是 .