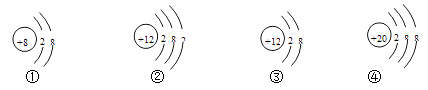题目内容
【题目】某班同学为验证酸的化学通性,做了五组实验。分析并回答问题。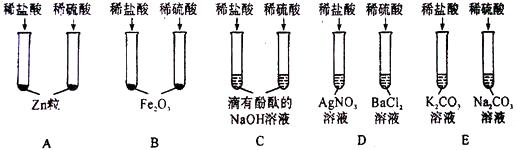
(1)A组试管中都产生H2。若要制得较纯的H2 , 选稀硫酸而不选盐酸的原因是。
(2)C组试管中药品滴加至一定程度实验现象相同,该现象是。
(3)写出D组任一试管中发生反应的化学方程式。
(4)上述五组实验中没有体现酸的通性的是(填序号)。
【答案】
(1)盐酸有挥发性或盐酸会挥发出氯化氢气体(制得的氢气中混有氯化氢气体)
(2)红色溶液褪为无色
(3)HCl+AgNO3 = AgCl↓+HNO3(H2SO4+BaCl2 = BaSO4↓+2HCl)
(4)D
【解析】(1)盐酸具有挥发性,挥发出氯化氢气体,制得的氢气中混有氯化氢气体,不纯净。
(2)C组试管中药品滴加,酸与碱发生中和反应,消耗了NaOH溶液,现象为红色溶液退为无色。
(3)HCl+AgNO3 = AgCl↓+HNO3(H2SO4+BaCl2 = BaSO4↓+2HCl)
(4)酸能与酸碱指示剂、活泼金属、金属氧化物、碱、盐等反应,ABCE分别能体现酸能与活泼金属、金属氧化物、碱、碳酸盐等反应;D中盐酸只能与硝酸银溶液反应,故五组实验中没有体现酸的通性的是D。
【考点精析】关于本题考查的中和反应及其应用,需要了解中和反应:酸与碱作用生成盐和水的反应才能得出正确答案.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
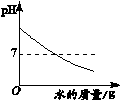
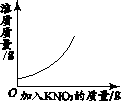
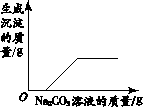
【题目】下列4个图像能正确反映对应变化关系的是( )
A | B | C | D |
|
|
|
|
向一定量NaOH溶液中加水 | 向一定量不饱和KNO3溶液中逐渐加入KNO3固体 | 向一定量澄清石灰水中加入Na2CO3溶液 | 向等质量的Mg、MgO中加入稀盐酸 |
A.A
B.B
C.C
D.D