题目内容
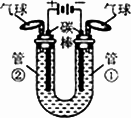
(探究题·讨论题)电解水生成氢气和氧气,证明了水是由氢、氧两种元素组成的.由此,老师要求同学们根据所学知识,设计实验证明双氧水是由氢、氧两种元素组成的.三位同学有以下讨论:(如图)
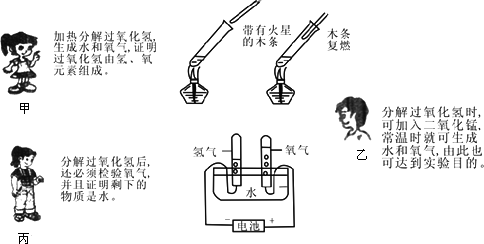
针对以上的讨论,请你当一次小老师,对上述三位同学的发言进行总结,并帮助他们设计出实验方案.
答案:
解析:
提示:
解析:
|
甲、乙、丙三位同学的发言都正确,甲、乙两位同学表述的主要是实验原理,加不加二氧化锰都可行,不过加入的二氧化锰后尽管不需要加热,但需要证明二氧化锰是催化剂(其质量和化学性质不变),考虑到实际操作的复杂性,不加二氧化锰更好;丙同学在甲、乙两位同学的基础上更进了一步,指明需要证明生成物.具体方案如下:用一支试管取少量过氧化氢,给试管加热,把带火星的木条伸到试管口,带火星木条复燃;充分反应后,电解冷却后的剩余物,发现有氢气和氧气生成(同电解水的实验),由此证明双氧水由氢、氧两种元素组成. |
提示:
|
三位同学的发言都有道理,电解水生成氢气和氧气,证明水是由氢、氧两种元素组成的;由此想到证明过氧化氢是由氢、氧两种元素组成的,可通过分解过氧化氢生成水和氧气的方法,这个思路是很正确的.是否需要加催化剂二氧化锰以及证明分解后的生成物是他们讨论的焦点.设计实验方案时要在确保能达到实验目的的前提下,使方案简洁、易于操作. |

练习册系列答案
 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目