题目内容
现一块铜合金,可能是黄铜(铜、锌合金)、青铜(铜、锡合金)、白铜[铜、镍(Ni)合金]中的一种,现欲测定其组成.
[查阅资料]Ⅰ.锌、锡、镍皆能与稀硫酸发生置换反应,生成+2价的金属离子;
Ⅱ.相对原子质量Zn-65,Sn-119,Ni-59.
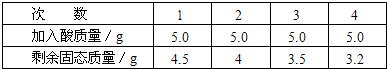
[实验步骤及数据]取5g合金粉碎后放入烧杯中,将20g15%稀H2SO4分四次加入烧杯中充分反应后,测定剩余固体质量数据记录如下:
| 次数 | 1 | 2 | 3 | 4 |
| 加入酸质量/g | 5.0 | 5.0 | 5.0 | 5.0 |
| 剩余固态质量/g | 4.5 | 4 | 3.5 | 3.2 |
(2)合金中另一金属为何种金属.
解:①合金中铜的质量分数=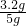 ×100%═64%
×100%═64%
②设该金属的化学式为R,其相对原子质量为x,则:
R+H2SO4 ═RSO4+H2↑
x 98
5g-4.5g=0.5g 5.0g×15%=0.75g
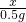 ═
═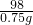
x=65.3≈65
故另一种金属为锌.
答:(1)合金中铜的质量分数64%.
(2)合金中另一金属为锌.
分析:(1)由题意知道,锌、锡、镍皆能与稀硫酸发生置换反应,铜不与稀硫酸反应,可以判断出最后剩余的3.2g是铜的质量,从而可以求出合金中铜的质量分数.
(2)先求出20g15%稀H2SO4中溶质的质量 5.0g×15%=0.75g,再根据表格中知道当加入酸的质量为5.0g时,参加反应的金属的质量为5.0g-4.5g═0.5g,代入方程式中就可以求出另一金属的相对原子质量,从而可以判断出合金中另一金属为何种金属.
点评:解此题的关键是审清题意,找出突破口,再结合方程式进行计算,可以得到问题答案.
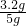 ×100%═64%
×100%═64% ②设该金属的化学式为R,其相对原子质量为x,则:
R+H2SO4 ═RSO4+H2↑
x 98
5g-4.5g=0.5g 5.0g×15%=0.75g
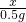 ═
═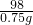
x=65.3≈65
故另一种金属为锌.
答:(1)合金中铜的质量分数64%.
(2)合金中另一金属为锌.
分析:(1)由题意知道,锌、锡、镍皆能与稀硫酸发生置换反应,铜不与稀硫酸反应,可以判断出最后剩余的3.2g是铜的质量,从而可以求出合金中铜的质量分数.
(2)先求出20g15%稀H2SO4中溶质的质量 5.0g×15%=0.75g,再根据表格中知道当加入酸的质量为5.0g时,参加反应的金属的质量为5.0g-4.5g═0.5g,代入方程式中就可以求出另一金属的相对原子质量,从而可以判断出合金中另一金属为何种金属.
点评:解此题的关键是审清题意,找出突破口,再结合方程式进行计算,可以得到问题答案.

练习册系列答案
相关题目
(本题有a、b两小题,考生任选一题解答,不得两题都解.若两题都解,则以a小题计分)
a.实验室里同学们要配制一定溶质质量分数的氯化钙溶液.药品柜中可供选择的药品只有氢氧化钙、氧化钙、碳酸钙和硝酸钙四种固体及一定溶质质量分数的稀盐酸.同学们交流讨论后,选择了一种固体药品并称取15g加入烧杯中,再向其中加入105.4g稀盐酸,充分反应后过得到5g固体和111 g氯化钙溶液(实验中物质损耗忽略不计),并将上述配好的氯化钙溶液倒入贴有相应标签的试剂瓶中.请回答下列问题:
(1)同学们选择的固体药品是 ;
(2)请写出题中发生反应的化学方程式 ;
(3)请根据已知条件求解生成氯化钙质量 g.
b.现一块铜合金,可能是黄铜(铜锌合金)、青铜(铜、锡合金)、白铜[铜、镍(Ni)合金]中的一种,现欲测定其组成.
[查阅资料]Ⅰ.锌、锡、镍皆能与稀硫酸发生置换反应,生成+2价的金属离子;
Ⅱ.相对原子质量Zn-65,Sn-119,Ni-59.
[实验步骤及数据]取5g合金粉碎后放入烧杯中,将20g15%稀H2SO4分四次加入烧杯中充分反应后,测定剩余固体质量数据记录如下:
试求:①合金中铜的质量分数为 .②合金中另一金属是 .
a.实验室里同学们要配制一定溶质质量分数的氯化钙溶液.药品柜中可供选择的药品只有氢氧化钙、氧化钙、碳酸钙和硝酸钙四种固体及一定溶质质量分数的稀盐酸.同学们交流讨论后,选择了一种固体药品并称取15g加入烧杯中,再向其中加入105.4g稀盐酸,充分反应后过得到5g固体和111 g氯化钙溶液(实验中物质损耗忽略不计),并将上述配好的氯化钙溶液倒入贴有相应标签的试剂瓶中.请回答下列问题:
(1)同学们选择的固体药品是
(2)请写出题中发生反应的化学方程式
(3)请根据已知条件求解生成氯化钙质量
b.现一块铜合金,可能是黄铜(铜锌合金)、青铜(铜、锡合金)、白铜[铜、镍(Ni)合金]中的一种,现欲测定其组成.
[查阅资料]Ⅰ.锌、锡、镍皆能与稀硫酸发生置换反应,生成+2价的金属离子;
Ⅱ.相对原子质量Zn-65,Sn-119,Ni-59.
[实验步骤及数据]取5g合金粉碎后放入烧杯中,将20g15%稀H2SO4分四次加入烧杯中充分反应后,测定剩余固体质量数据记录如下:
| 次数 | 1 | 2 | 3 | 4 |
| 加入酸的质量/g | 5.0 | 5.0 | 5.0 | 5.0 |
| 剩余固态质量/g | 4.5 | 4 | 3.5 | 3.2 |
人类发展的历史进程中人们不断研制出各种不同的用具,制造用具的材料也在不断变化.
(1)磁悬浮的核心技术得制备超导材料.有一种超导材料的化学式为Y2BaCu6O10,它是以Y2O3、BaCO3和CuO为原料经研磨烧结而成.假设此过程中所有元素的化合价不变,在合成该超导材料的同时还生成-种产物,该物质是 (写化学式).
(2)现一块铜合金,可能是黄铜(铜锌合金)、青铜(铜、锡合金)、白铜[铜、镍(Ni)合金]中的一种,现欲测定其组成.
[查阅资料]
Ⅰ.锌、锡、镍皆能与稀硫酸发生置换反应,生成+2价的金属离子;
Ⅱ.相对原子质量Zn-65,Sn一119,Ni一59.
[实验步骤及数据]取5g合金粉碎后放入烧杯中,将20g15%稀H2SO4分四次加入烧杯中充分反应后,测定剩余固体质量数据记录如下:
试求:
①合金中铜的质量分数.
②通过计算判断合金中另一金属为何种金属.
(1)磁悬浮的核心技术得制备超导材料.有一种超导材料的化学式为Y2BaCu6O10,它是以Y2O3、BaCO3和CuO为原料经研磨烧结而成.假设此过程中所有元素的化合价不变,在合成该超导材料的同时还生成-种产物,该物质是
(2)现一块铜合金,可能是黄铜(铜锌合金)、青铜(铜、锡合金)、白铜[铜、镍(Ni)合金]中的一种,现欲测定其组成.
[查阅资料]
Ⅰ.锌、锡、镍皆能与稀硫酸发生置换反应,生成+2价的金属离子;
Ⅱ.相对原子质量Zn-65,Sn一119,Ni一59.
[实验步骤及数据]取5g合金粉碎后放入烧杯中,将20g15%稀H2SO4分四次加入烧杯中充分反应后,测定剩余固体质量数据记录如下:
| 次 数 | l | 2 | 3 | 4 |
| 加入酸质量/g | 5.0 | 5.0 | 5.0 | 5.0 |
| 剩余固态质量/g | 4.5 | 4 | 3.5 | 3.2 |
①合金中铜的质量分数.
②通过计算判断合金中另一金属为何种金属.
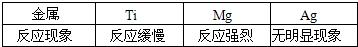
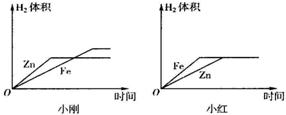
 2CuO+H2O+CO2↑,古代人们发现翠绿的孔雀石在森林大火中会变成红色的铜,请写出转化为铜的另一个反应方程式:_________
2CuO+H2O+CO2↑,古代人们发现翠绿的孔雀石在森林大火中会变成红色的铜,请写出转化为铜的另一个反应方程式:_________

