题目内容
【题目】化学与我们的生活密切相关。
(1)新装修的房间里面放一些炭包(里面装的是活性炭),这是利用了活性炭具有_____。
(2)被蚊虫叮咬后,通常在叮咬处涂上肥皂水止痒,这样处理利用的原理是_____。
(3)纯棉布与涤纶布的鉴别方法是_____。
(4)蜂窝煤是一种常见燃料,如图所示。把煤做成蜂窝状的科学道理是_____。
(5)为了防止青少年患佝偻病,老年人患骨质疏松,应经常食用以下食物_____(填写序号)。
a.牛奶 b.水果 c.虾皮 d.豆腐 e.瘦肉

【答案】吸附性 酸碱中和反应 灼烧,有烧纸的味道的是棉布,有刺激难闻的气体生成的是涤纶布 增大煤与氧气的接触面积; acd
【解析】
(1)新装修的房间里面放一些炭包(里面装的是活性炭),这是利用了活性炭的吸附性,故填吸附性。
(2)被蚊虫叮咬后,通常在叮咬处涂上肥皂水止痒,这样处理利用的原理是酸碱中和反应,故填酸碱中和反应。
(3)纯棉布与涤纶布的鉴别方法是灼烧,棉布燃烧时有烧纸的味道,涤纶布燃烧有刺激难闻的气体生成,所以点燃闻气味可以鉴别棉布与涤纶布,故填灼烧,有烧纸的味道的是棉布,有刺激难闻的气体生成的是涤纶布。
(4)把煤做成蜂窝状的科学道理是增大了煤与氧气的接触面积,能使煤充分燃烧,故填增大煤与氧气的接触面积。
(5)a.牛奶中富含钙元素;
b.水果中富含维生素;
c.虾皮中富含钙元素;
d.豆腐中富含钙元素与蛋白质;
e.瘦肉中富含锌元素和蛋白质,为了防止青少年患佝偻病,老年人患骨质疏松,应经常食用牛奶、虾皮、豆腐等含钙丰富的食物,故填acd。

【题目】草木灰中富含钾盐,主要成分是碳酸钾,还含有少量氯化钾和硫酸钾。化学小组的同学从草木灰中提取钾盐,并检验其部分成分。请根据部分盐溶解性表和学过的知识回答下列问题:
部分盐的溶解性表(室温)
阴离子/阳离子 | NO3﹣ | Cl﹣ | SO42﹣ | CO32﹣ |
K+ | 溶 | 溶 | 不 | 溶 |
Ba2+ | 溶 | 溶 | 不 | 不 |
Ca2+ | 溶 | 溶 | 微 | 不 |
Ag+ | 溶 | 不 | 微 | 不 |
实验一:分离提纯
①取适量草木灰样品,研碎。
②将研碎的草木灰样品置于烧杯中,加入适量的蒸馏水溶解。
③过滤
④蒸发结晶。将滤液加入蒸发皿中,用酒精灯加热,并用玻璃棒不断搅拌。
步骤③过滤需要的玻璃仪器有_____;
步骤④中,用玻璃棒搅拌的目的是_____。
实验二:验证成分
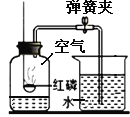
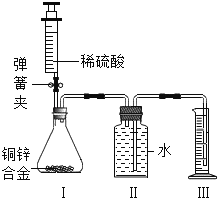
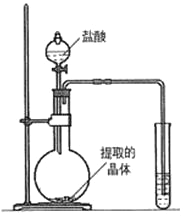
(1)验证碳酸钾存在:取少量实验一所得的晶体置于烧瓶中,按如图所示的装置实验,则试管中装的药品是_____,证明晶体中含有碳酸钾的实验现象是_____。烧瓶中发生反应的化学方程式是_____。
(2)验证硫酸钾存在:
甲同学取少量实验一所得的晶体于试管中,加蒸馏水溶解后,再加入氯化钡溶液,产生白色沉淀,于是他得出晶体中含有硫酸钾的结论。
乙同学认为,甲同学的方案不合理,其理由是:_____。
乙同学继续向甲同学所得白色沉淀中加入过量的_____,观察到_____,证明了晶体中硫酸钾的存在。
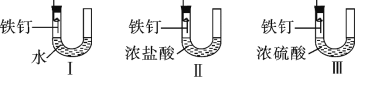
【题目】很多水龙头是铜质镀铬的,为了了解铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,同学们进行如下探究活动:
(查阅资料)铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜。铬能与稀硫酸反应,生成蓝色的硫酸亚铬( CrSO4)溶液,铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液。
(预测)三种金属在金属活动性顺序中的相对位置关系:
①Cr Al Cu ②Al Cr Cu ③Al Cu Cr
(实验过程)取大小相同的三种金属薄片,用砂纸打磨光亮。
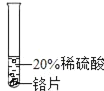
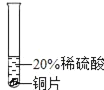
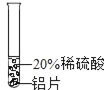
实验一 | 实验二 | 实验三 | |
实验 方案 |
|
|
|
实验 现象 | 铬片表面产生气泡缓慢,溶液变蓝色。 | _____ | 铝片表面产生气泡较快。 |
结论 | 铬能和稀硫酸发生反应,反应速率较慢。 | 铜不与稀硫酸反应 | _____ |
三种金属在金属活动性顺序中的相对位置关系是_____ | |||
(回答问题)(1)用砂纸打磨金属片的目的是_____。
(2)实验一所发生反应的化学方程式是_____。
(3)小东提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,小燕认为不可行,理由是_____。
(4)小清认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种药品可以是_____。
(归纳)比较金属活动性强弱的方法有
①_____ ②_____。
【题目】为了对氯化钾样品(含少量KNO3)进行组分分析,甲、乙、丙三位同学分别进行实验,它们的实验数据如下表.请仔细观察和分析数据,回答下列问题.
甲 | 乙 | 丙 | |
所取固体样品的质量(g) | 20 | 10 | 10 |
加入AgNO3溶液的质量(g) | 100 | 100 | 150 |
反应后所得沉淀的质量(g) | 14.35 | 14.35 | 14.35 |
(1)样品中氯化钾的质量分数是____?(小数点后面保留两位数,下同)
(2)三位同学分别把反应后的溶液过滤,哪一位同学所得的滤液是只含一种溶质的溶液?此溶液的溶质质量分数是____?