题目内容
1.某工厂从含有CuSO4、ZnSO4、FeSO4的废水中回收重要原料硫酸锌和有关金属,实验过程如图
请回答:
写出步骤①中发生反应的化学方程式Zn+FeSO4=Fe+ZnSO4 ;Zn+CuSO4=ZnSO4+Cu;步骤②的操作是用磁铁吸引;固体D的化学式为Fe;以上物质A~G中,含有锌元素的是ABCEG(填字母序号).
分析 根据题中的信息,推导出反应物和生产物,正确书写化学方程式.根据加入的过量锌与硫酸铜和硫酸亚铁反应,得到的固体B中含有铁、铜、锌,再利用磁铁分离开铁,再利用硫酸把铜和锌分开,再进一步进行分析即可.
解答 解:过量A是加入的锌,锌与硫酸亚铁反应生成铁和硫酸锌,所以化学方程式是:Zn+FeSO4═Fe+ZnSO4;锌与硫酸铜反应生成铜和硫酸锌,所以化学方程式是:Zn+CuSO4═ZnSO4+Cu;由于锌与硫酸亚铁反应生成铁和硫酸锌,锌与硫酸铜反应生成铜和硫酸锌,且加入的锌是过量的,所以固体B中含有锌、铁、铜;溶液C是硫酸锌溶液;固体B用磁铁把铁吸引出来,所以固体D是铁;固体E中含有锌和铜,由于锌能与硫酸反应,铜与硫酸不反应,所以加入的溶液F是稀硫酸,溶液G是硫酸锌溶液;所以含有锌元素的有ABCEG.
故答案为:Zn+CuSO4═Cu+ZnSO4,Zn+FeSO4═Fe+ZnSO4; 用磁铁吸引; Fe; ABCEG.
点评 本题要熟练掌握金属铁的性质、冶炼以及金属活动顺序等知识,培养学生对知识的概括和总结能力.

练习册系列答案
相关题目
12.实验室可利用碱式碳酸铜(化学式:Cu2(OH)2CO3)制备氧化铜,并进行碳粉还原氧化铜的实验.
①制备氧化铜并检验产物,装置如图1所示(省略夹持仪器):已知烧碱可与二氧化碳反应,无水硫酸铜为白色固体可吸收水、变蓝.
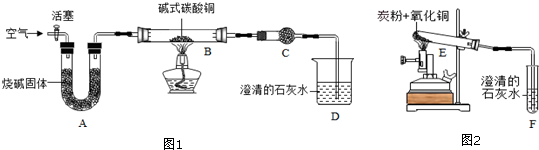
步骤一:连接A和B,打开活塞,通入空气.
步骤二:关闭活塞,连上C和D,开始加热.
步骤三:在加热过程中,记录在B中固体质量变化如下表,在t3时停止加热.
B中发生反应的化学方程式为:□Cu2(OH)2CO3═□CuO+□H2O+□CO2↑
请在□中填入配平后的系数,依次为1、2、1、1.C中试剂是无水硫酸铜 无水硫酸铜.A的作用是吸收空气中的水蒸气和二氧化碳 水蒸气和二氧化碳,防止对产物检验造成干扰.选择t3时停止加热的理由是固体质量不再减少,证明碱式碳酸铜已经完全分解
②一定量碳粉还原①中制得的氧化铜并检验产物,装置如图2所示:实验过程中,观察到F中溶液变浑浊,E中的现象是黑色粉末变成红色,反应完全后,若仅撤走酒精喷灯停止加热,可能导致的后果是F中的液体通过导管流入E中,造成试管炸裂
③分析:若①中省略步骤三,对②中反应产物判断可能产生的影响及其原因.不能确定炭粉还原氧化铜的生成物中是否含有二氧化碳.
因为可能有①中未分解的碱式碳酸铜在实验②中分解,产生二氧化碳气体,干扰对炭粉还原氧化铜反应生成物的判断.
①制备氧化铜并检验产物,装置如图1所示(省略夹持仪器):已知烧碱可与二氧化碳反应,无水硫酸铜为白色固体可吸收水、变蓝.

步骤一:连接A和B,打开活塞,通入空气.
步骤二:关闭活塞,连上C和D,开始加热.
步骤三:在加热过程中,记录在B中固体质量变化如下表,在t3时停止加热.
| 加热时间(min) | 0 | t1 | t2 | t3 |
| B中固体质量(g) | 6.66 | 5.20 | 4.80 | 4.80 |
请在□中填入配平后的系数,依次为1、2、1、1.C中试剂是无水硫酸铜 无水硫酸铜.A的作用是吸收空气中的水蒸气和二氧化碳 水蒸气和二氧化碳,防止对产物检验造成干扰.选择t3时停止加热的理由是固体质量不再减少,证明碱式碳酸铜已经完全分解
②一定量碳粉还原①中制得的氧化铜并检验产物,装置如图2所示:实验过程中,观察到F中溶液变浑浊,E中的现象是黑色粉末变成红色,反应完全后,若仅撤走酒精喷灯停止加热,可能导致的后果是F中的液体通过导管流入E中,造成试管炸裂
③分析:若①中省略步骤三,对②中反应产物判断可能产生的影响及其原因.不能确定炭粉还原氧化铜的生成物中是否含有二氧化碳.
因为可能有①中未分解的碱式碳酸铜在实验②中分解,产生二氧化碳气体,干扰对炭粉还原氧化铜反应生成物的判断.
 如图为过滤装置,根据实验回答下列问题:
如图为过滤装置,根据实验回答下列问题: