题目内容
(1)金属镁是一种活泼的金属,可与热水反应生成氢气和氢氧化镁[Mg(OH)2].写出该反应的化学方程式:______ Mg(OH)2+H2↑
【答案】分析:(1)利用反应物生成物及反条件结合化学方程式的书写解决即可.
(2)①酚酞变质时刚开始溶液不会变红.
②是进行对比试验证明二氧化碳的作用.
③氢氧化镁的溶解度随温度的降低而变小所以升温后看红色是否恢复,进而作出判断.
④从酚酞自身会与空气中的氧气反应分析猜想.
解答:答:(1)依据反应物是水与镁生成物是氢氧化镁和氢气,条件是加热,结合化学方程式的书写要求完成即可.
(2)①甲同学的猜想也有明显错误,因为一开始加入时酚酞已经变红了,而酚酞遇碱性溶液变红是酚酞的特性,一开始变红说明酚酞未变质.
②是进行对比试验证明二氧化碳的作用,通过溶液通入二氧化碳的现象可对比出二氧化碳的作用.
③如果氢氧化镁的溶解度随温度的降低而变小所以升温后氢氧化镁的溶解度升高红色就会重新出现,进而作出红色消失原因的判断.
④酚酞自身也可能与空气中的成分特别是氧气反应导致红色褪去.
故答案为:(1)Mg+2H2O Mg(OH)2+H2↑
Mg(OH)2+H2↑
(2)①若酚酞变质,刚开始溶液就不会变红色;
②进行对比实验,证明溶液褪色是否因吸收CO2引起;
③
④溶液褪色可能因为溶液中的酚酞与空气中的氧气反应.
点评:本题是已设计的实验方案进行评价,以及自己设计实验方案的题目,要注意考虑所涉及物质的化学性质,据它们的化学性质来设计方案,这是我们解题的大方向.
(2)①酚酞变质时刚开始溶液不会变红.
②是进行对比试验证明二氧化碳的作用.
③氢氧化镁的溶解度随温度的降低而变小所以升温后看红色是否恢复,进而作出判断.
④从酚酞自身会与空气中的氧气反应分析猜想.
解答:答:(1)依据反应物是水与镁生成物是氢氧化镁和氢气,条件是加热,结合化学方程式的书写要求完成即可.
(2)①甲同学的猜想也有明显错误,因为一开始加入时酚酞已经变红了,而酚酞遇碱性溶液变红是酚酞的特性,一开始变红说明酚酞未变质.
②是进行对比试验证明二氧化碳的作用,通过溶液通入二氧化碳的现象可对比出二氧化碳的作用.
③如果氢氧化镁的溶解度随温度的降低而变小所以升温后氢氧化镁的溶解度升高红色就会重新出现,进而作出红色消失原因的判断.
④酚酞自身也可能与空气中的成分特别是氧气反应导致红色褪去.
故答案为:(1)Mg+2H2O
 Mg(OH)2+H2↑
Mg(OH)2+H2↑ (2)①若酚酞变质,刚开始溶液就不会变红色;
②进行对比实验,证明溶液褪色是否因吸收CO2引起;
③
| 实验方法 | 可能观察到的现象和结论 |
| 将原褪色的溶 液升高温度(加热) | 若溶液恢复成红色,则说明氢氧化镁溶解度随温度的降低而变小是造成溶液褪色的原因 |
点评:本题是已设计的实验方案进行评价,以及自己设计实验方案的题目,要注意考虑所涉及物质的化学性质,据它们的化学性质来设计方案,这是我们解题的大方向.

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
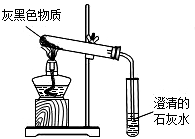 镁将成为21世纪重要的轻型环保材料,我国含有非常丰富的镁资源.
镁将成为21世纪重要的轻型环保材料,我国含有非常丰富的镁资源. 镁将成为21世纪重要的轻型环保材料,我国含有非常丰富的镁资源.
镁将成为21世纪重要的轻型环保材料,我国含有非常丰富的镁资源. C+2MgO,此反应类型属于________反应(填分解、化合、置换).由此你对燃烧有什么新的认识________(写一点)
C+2MgO,此反应类型属于________反应(填分解、化合、置换).由此你对燃烧有什么新的认识________(写一点) C+2MgO,此反应类型属于______反应(填分解、化合、置换).由此你对燃烧有什么新的认识______(写一点)
C+2MgO,此反应类型属于______反应(填分解、化合、置换).由此你对燃烧有什么新的认识______(写一点)