题目内容
某同学用如下装置,进行有关碳及其氧化物的实验(图中固定试管的仪器已略去).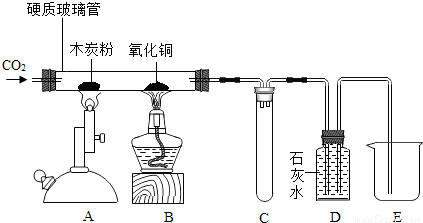
| 步骤 | 现象 | 分析 |
| ①点燃A处酒精喷灯,一段时间 | 木炭粉减少,D中有气泡、石灰水变浑浊且______. | 硬质玻璃管中发生反应的化学方程式是______ |
【答案】分析:①根据碳还原二氧化碳生成一氧化碳,因此木炭粉减少,过量的二氧化碳能使石灰水变浑浊,根据D装置能收集气体,因此液面下降分析;
②根据一氧化碳还原氧化铜生成铜和二氧化碳,因此B处黑色粉末变为光亮红色,D中石灰水变浑浊,液面下降分析;
③根据玻璃管内的气体随温度降低而压强减小分析;
过量一氧化碳已收集在D中,并没有排放到空气中,不会造成污染.
解答:解:①点燃A处酒精喷灯一段时间,碳还原二氧化碳生成一氧化碳,因此木炭粉减少,过量的二氧化碳能使石灰水变浑浊,根据D装置能收集气体,因此液面下降,发生反应的化学方程式是2C+CO2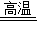 2CO;
2CO;
②点燃B处酒精灯,一段时间,一氧化碳还原氧化铜生成铜和二氧化碳,因此B处黑色粉末变为光亮红色,D中石灰水变浑浊,根据D装置能收集气体,因此液面下降,生反应的化学方程式是CO+CuO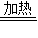 Cu+CO2;
Cu+CO2;
③停止通入二氧化碳,熄灭A、B两处火焰,玻璃管内的气体随温度降低而压强减小,因此D中液体倒流入C;
该装置不需要添加尾气处理装置,因为过量一氧化碳已收集在D中,并没有排放到空气中,不会造成污染.
故答案为:①液面下降;2C+CO2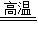 2CO;
2CO;
②黑色粉末变为光亮红色;CO+CuO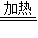 Cu+CO2;
Cu+CO2;
③出现液体;
不需要,因为过量一氧化碳已收集在D中,并没有排放到空气中,不会造成污染.
点评:此题是一道实验的综合题,解题的关键是对相关物质性质的分析,另外解题时实验的一些关键现象也常常是解题的重要突破口,同时考查了有毒气体对环境的污染.
②根据一氧化碳还原氧化铜生成铜和二氧化碳,因此B处黑色粉末变为光亮红色,D中石灰水变浑浊,液面下降分析;
③根据玻璃管内的气体随温度降低而压强减小分析;
过量一氧化碳已收集在D中,并没有排放到空气中,不会造成污染.
解答:解:①点燃A处酒精喷灯一段时间,碳还原二氧化碳生成一氧化碳,因此木炭粉减少,过量的二氧化碳能使石灰水变浑浊,根据D装置能收集气体,因此液面下降,发生反应的化学方程式是2C+CO2
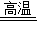 2CO;
2CO;②点燃B处酒精灯,一段时间,一氧化碳还原氧化铜生成铜和二氧化碳,因此B处黑色粉末变为光亮红色,D中石灰水变浑浊,根据D装置能收集气体,因此液面下降,生反应的化学方程式是CO+CuO
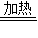 Cu+CO2;
Cu+CO2;③停止通入二氧化碳,熄灭A、B两处火焰,玻璃管内的气体随温度降低而压强减小,因此D中液体倒流入C;
该装置不需要添加尾气处理装置,因为过量一氧化碳已收集在D中,并没有排放到空气中,不会造成污染.
故答案为:①液面下降;2C+CO2
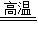 2CO;
2CO;②黑色粉末变为光亮红色;CO+CuO
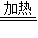 Cu+CO2;
Cu+CO2;③出现液体;
不需要,因为过量一氧化碳已收集在D中,并没有排放到空气中,不会造成污染.
点评:此题是一道实验的综合题,解题的关键是对相关物质性质的分析,另外解题时实验的一些关键现象也常常是解题的重要突破口,同时考查了有毒气体对环境的污染.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
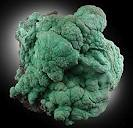 孔雀石[碱式碳酸铜,主要成分是Cu2(OH)2CO3]具有色彩浓淡的条状花纹(如图),是矿物中最吸引人的装饰材料之一,也是人类最早冶炼铜的原料.
孔雀石[碱式碳酸铜,主要成分是Cu2(OH)2CO3]具有色彩浓淡的条状花纹(如图),是矿物中最吸引人的装饰材料之一,也是人类最早冶炼铜的原料.冶炼铜的反应原理为:Cu(OH)2CO3
| ||
2CuO+C
| ||
某校课外小组同学在实验室验证上述反应.
(1)加热分解碱式碳酸铜,生成氧化铜.装置如下图所示.
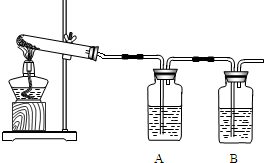
①瓶A中盛有的试剂是
②瓶B中盛有的试剂是澄清石灰水,用来
③反应结束,熄灭酒精灯前,应
(2)木炭和氧化铜反应,生成铜.
将木炭粉末和氧化铜粉末混合均匀,放进试管,加热充分反应.将试管中的粉末倒出,有铜生成,还有少量黑色粉末剩余.该小组同学设计方案验证黑色粉末的成分.
查阅资料:部分内容如下:木炭和氧化铜都是黑色粉末.氧化铜与稀硫酸反应生成硫酸铜,木炭与稀硫酸不反应.
| 操作和药品 | 现象 | 分析和结论 | |
| 方案Ⅰ | 取少量剩余黑色粉末,充分灼烧 | ①______________ ________________ |
原剩余黑色粉末是 氧化铜 |
| 方案Ⅱ | ②_______________ __________________ |
③_____________ _________________ |
原剩余黑色粉末是 氧化铜 |
(3)某同学探究在实际反应中,木炭和氧化铜反应生成铜时反应物的最佳质量比.设计方案如下:
| 配方1 | 配方2 | 配方3 | 配方4 | |
| 木炭质量(g) | 0.4 | 0.5 | 0.6 | 0.7 |
| 氧化铜质量(g) | 8 | 8 | 8 | 8 |
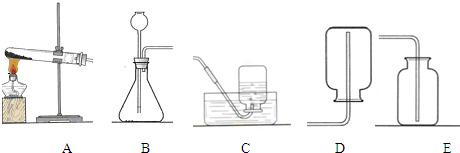
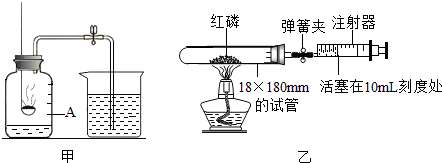
 如图是某同学测定空气中氧气的体积分数的实验装置图,请回答如下问题:
如图是某同学测定空气中氧气的体积分数的实验装置图,请回答如下问题: