题目内容
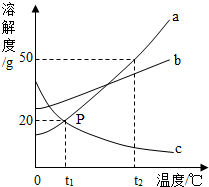
 根据图中a、b、c三种物质的溶解度曲线,回答下列问题:
根据图中a、b、c三种物质的溶解度曲线,回答下列问题:
(1)P点表示在t1℃两物质的溶解度关系为b________c(填“>”、“<”或“=”).
(2)t2℃,a、b、c三种物质的饱和溶液溶质质量分数的大小关系为________.
(3)t2℃时,50g b物质加入到50g水中充分溶解后,所得溶液的质量为________.
解:(1)曲线中交点表示该温度时两种物质的溶解度相等,所以P点表示在t1℃两物质的溶解度相等;
(2)根据饱和溶液的质量分数: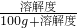 ×100%公式可知饱和溶液中溶质的质量分数与溶解度有关,因为t2℃,a、b、c三种物质的溶解度大小是:b>a>c,所以它们饱和溶液的质量分数也是:b>a>c;
×100%公式可知饱和溶液中溶质的质量分数与溶解度有关,因为t2℃,a、b、c三种物质的溶解度大小是:b>a>c,所以它们饱和溶液的质量分数也是:b>a>c;
(3)t2℃时,b物质的溶解度是50g,即100g水中溶解50g,所以50g水中只能溶解25g,所以所得溶液质量为50g+25g=75g;
故答案为:(1)=;(2)b>a>c;(3)75g.
分析:(1)根据曲线中交点的含义考虑;
(2)根据饱和溶液质量分数的计算考虑;
(3)根据t2℃时,b物质的溶解度考虑.
点评:解答本题的关键是要知道溶解度曲线表示的意义,知道了溶解度如何比较大小,饱和溶液溶质质量分数的计算公式,固体物质从溶液中结晶析出的方法.
(2)根据饱和溶液的质量分数:
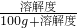 ×100%公式可知饱和溶液中溶质的质量分数与溶解度有关,因为t2℃,a、b、c三种物质的溶解度大小是:b>a>c,所以它们饱和溶液的质量分数也是:b>a>c;
×100%公式可知饱和溶液中溶质的质量分数与溶解度有关,因为t2℃,a、b、c三种物质的溶解度大小是:b>a>c,所以它们饱和溶液的质量分数也是:b>a>c;(3)t2℃时,b物质的溶解度是50g,即100g水中溶解50g,所以50g水中只能溶解25g,所以所得溶液质量为50g+25g=75g;
故答案为:(1)=;(2)b>a>c;(3)75g.
分析:(1)根据曲线中交点的含义考虑;
(2)根据饱和溶液质量分数的计算考虑;
(3)根据t2℃时,b物质的溶解度考虑.
点评:解答本题的关键是要知道溶解度曲线表示的意义,知道了溶解度如何比较大小,饱和溶液溶质质量分数的计算公式,固体物质从溶液中结晶析出的方法.

练习册系列答案
相关题目
 请根据图中a、b、c三种物质的溶解度曲线,回答下列问题:
请根据图中a、b、c三种物质的溶解度曲线,回答下列问题: 请根据图中a、b、c三种物质的溶解度曲线,回答下列问题:
请根据图中a、b、c三种物质的溶解度曲线,回答下列问题: 根据图中a、b、c三种物质的溶解度曲线,回答下列问题:
根据图中a、b、c三种物质的溶解度曲线,回答下列问题:

 请根据图中a、b、c三种物质的溶解度曲线,回答下列问题:
请根据图中a、b、c三种物质的溶解度曲线,回答下列问题: