题目内容
12.多彩的“碳”,多姿的生活,让我们一起走进“碳”的世界.(1)下列含碳元素的物质中,属于有机物的是B(填字母序号).
A.碳酸钙 B.醋酸 C.二氧化碳
(2)二氧化碳与碳的反应吸收热量(选填“吸收”或“放出”).
(3)碳与水在一定条件下反应可产生水煤气,其微观示意图如图1所示:

写出该反应的化学方程式C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2.
(4)科学家利用NaOH溶液喷淋“捕捉”空气中的CO2.其工业流程如图2所示:
①吸收塔中发生反应的化学方程式为CO2+2NaOH=Na2CO3+H2O.
②操作①中一定(填“一定”或“不一定”)含有过滤.
③上述工业流程中B(选填A、B、C)内发生了复分解反应.
A.吸收塔 B.分离池 C.煅烧炉
④上述流程中可以循环使用的物质是CaO、NaOH.
⑤用NaOH溶液喷淋“捕捉”空气中的CO2的好处是增大反应接触面积,充分反应.
分析 (1)根据有机物的组成定义来分析;
(2)根据二氧化碳与碳的反应条件来分析;
(3)根据图示书写方程式;
(4)①由题目给出的信息可知:吸收塔中发生的反应是二氧化碳和氢氧化钠溶液反应生成碳酸钠和水,分离池中发生的反应是氧化钙和水反应生成氢氧化钙,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,煅烧炉中发生的反应是碳酸钙高温分解生成氧化钙、二氧化碳,据此书写方程式;
②因为生石灰和水反应生成熟石灰,熟石灰和碳酸钠反应生成碳酸钙白色沉淀和氢氧化钠,因此分离池中过滤出的是碳酸钙白色沉淀;物质①是碳酸钠和氢氧化钙反应生成的氢氧化钠溶液;
③根据发生的化学反应和反应类型特点分析解答;
④据①分析可知:整个流程中,循环利用的物质是氢氧化钠溶液和生石灰;
⑤NaOH溶液喷成雾状的目的是增大气体与液体的接触面积,使反应更充分.
解答 解:(1)下列含碳元素的物质中,属于有机物的是醋酸;
(2)二氧化碳与碳的反应条件是高温,该反应吸收热量;
(3)碳与水在一定条件下反应可产生一氧化碳和氢气;
(4)①由题目给出的信息可知:吸收塔中发生的反应是二氧化碳和氢氧化钠溶液反应生成碳酸钠和水,方程式是:2NaOH+CO2═Na2CO3+H2O;
②因为生石灰和水反应生成熟石灰,熟石灰和碳酸钠反应生成碳酸钙白色沉淀和氢氧化钠,因此分离池中过滤出的是碳酸钙白色沉淀;
③复分解反应是两种化合物相互交换成分生成另外两种化合物的反应,由(1)化学反应的特点可知:分离池中Ca(OH)2+Na2CO3═CaCO3↓+2NaOH属于复分解反应;
④吸收塔中发生的反应是二氧化碳和氢氧化钠溶液反应生成碳酸钠和水,分离池中发生的反应是氧化钙和水反应生成氢氧化钙,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,煅烧炉中发生的反应是碳酸钙高温分解生成氧化钙、二氧化碳,故整个流程中,循环利用的物质是氢氧化钠溶液和生石灰;
⑤NaOH溶液喷成雾状的目的是增大气体与液体的接触面积,使反应更充分;
答案:(1)B; (2)吸收; (3)C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2;
(4)①CO2+2NaOH=Na2CO3+H2O;
②一定;
③B;
④CaO、NaOH;
⑤增大反应接触面积,充分反应.
点评 本题考査了有关二氧化碳的性质和化学方程式的书写等,考查的知识点比较多,要综合应用,着重考查了向上对知识的理解和运用.

 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案| A. | 钢铁门窗比铝合金门窗更耐腐蚀 | |
| B. | 化肥KN03比NH4NO3营养元素种类多 | |
| C. | 青少年缺钙会患佝偻病和发育不良 | |
| D. | 种植吃叶的蔬菜,应施用较多的氮肥 |
| A. | Y>X>Z | B. | X>Y>Z | C. | Y>Z>X | D. | Z>Y>X |
(1)确定固体的成分.
【提出猜想】猜想Ⅰ:固体中只含碳酸钠;
猜想Ⅱ:固体中只含氢氧化钠;
猜想Ⅲ:固体中含有碳酸钠和氢氧化钠.
【进行实验】
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量固体溶于水,加入 过量的氯化钡溶液; | 产生白色沉淀 | 猜想Ⅲ成立 |
| ②将上述反应后的混合液过滤,取少量滤液,加入无色酚酞试液. | 酚酞试液变红色 |
【查阅资料】二氧化碳几乎不溶于饱和碳酸氢钠溶液中.
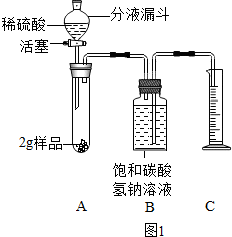
【进行实验】取2g固体,在25℃、101kPa下用图1所示装置进行实验,步骤如下:
①连接好装置并检查气密性;
②装入药品,通过分液漏斗滴加足量稀硫酸后,关闭分液漏斗活塞;
③充分反应后,恢复至25℃、101kPa,量筒中液体的体积为220mL.
【实验分析】
①装置B中的饱和碳酸氢钠溶液不能用水代替,原因是二氧化碳能够溶于水.
②充分反应后,装置A中残留的二氧化碳对实验结果是否有明显影响?没有(选填“有”或“没有”).
③已知在25℃、101kPa下二氧化碳的密度为1.8g/L,则固体中碳酸钠的质量分数为47.7%(结果保留至0.1%).
(3)除去固体中的碳酸钠.
【进行实验】实验流程如图2:
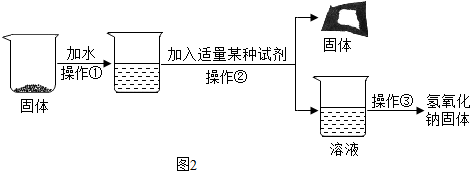
【实验分析】该流程中发生反应的化学方程式为Na2CO3+Ba(OH)2═BaCO3↓+2NaOH.操作①、②、③均需用到的一种仪器是玻璃棒.
| 序号 | 物质 | 杂质 | 所用试剂和操作方法 |
| A | CO2 | HCl | 将混合气体通过AgNO3溶液 |
| B | NaNO3溶液 | Na2SO4 | 加入过量的Ba(NO3)2溶液,过滤 |
| C | NaOH溶液 | Na2CO3 | 加入适量CaCl2溶液、过滤 |
| D | 铁粉 | Fe2O3 | 加入适量的稀盐酸,过滤 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 人体无法消化吸收纤维素,所以食物中的纤维素对人体毫无意义 | |
| B. | 煤气中毒主要是一氧化碳与血红蛋白结合,使血红蛋白失去输氧能力 | |
| C. | 作为健康饮食的一部分,每人每天都应当通过服用保健品补充各种营养素 | |
| D. | 低血糖发作时,吃馒头比喝葡萄糖水见效快 |
 应用所学知识,回答下列有关金属的问题:
应用所学知识,回答下列有关金属的问题:
