题目内容
A、B、C、D为中学化学中常见的物质,其中A为含三种元素的钠盐,其水溶液pH大于7.B可用作固体干燥剂.D是相对分子质量为100的白色不溶物.它们的相互关系如图所示:

请填写下列空白:
(1)A 、B 、D (填写化学式);
(2)D转化为B的反应类型为 (填基本反应类型);
(3)E中一定含有的溶质是 ,理由是 (用化学方程式表示)
(4)写出B在空气中变质的化学方程式 .

请填写下列空白:
(1)A
(2)D转化为B的反应类型为
(3)E中一定含有的溶质是
(4)写出B在空气中变质的化学方程式
考点:物质的鉴别、推断,盐的化学性质,反应类型的判定,书写化学方程式、文字表达式、电离方程式
专题:框图型推断题
分析:根据A、B、C、D为中学化学中常见的物质,A为含三种元素的钠盐,其水溶液pH大于7,B可用作固体干燥剂,D是相对分子质量为100的白色不溶物,所以D是碳酸钙,碳酸钙在高温的条件下生成氧化钙和二氧化碳,所以B是氧化钙,氧化钙和水反应生成氢氧化钙,碳酸钠和氢氧化钙反应生成碳酸钙白色沉淀和氢氧化钠,所以A是碳酸钠,C是氢氧化钙,E溶液中一定有氢氧化钠,然后将推出的物质进行验证即可.
解答:解:(1)A、B、C、D为中学化学中常见的物质,A为含三种元素的钠盐,其水溶液pH大于7,B可用作固体干燥剂,D是相对分子质量为100的白色不溶物,所以D是碳酸钙,碳酸钙在高温的条件下生成氧化钙和二氧化碳,所以B是氧化钙,氧化钙和水反应生成氢氧化钙,碳酸钠和氢氧化钙反应生成碳酸钙白色沉淀和氢氧化钠,所以A是碳酸钠,C是氢氧化钙,E溶液中一定有氢氧化钠,经过验证,推导正确,所以A是Na2CO3,B是CaO,D是CaCO3;
(2)D转化为B的反应是碳酸钙在高温的条件下生成氧化钙和二氧化碳,满足分解反应一变多的条件,所以反应类型为:分解反应;
(3)碳酸钠和氢氧化钙反应生成碳酸钙白色沉淀和氢氧化钠,因此E溶液中一定有氢氧化钠,化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(4)氧化钙在空气中变质是氧化钙和水反应生成氢氧化钙,氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,化学方程式为:CaO+H2O=Ca(OH)2,Ca(OH)2+CO2=CaCO3↓+H2O.
故答案为:(1)Na2CO3,CaO,CaCO3;
(2)分解反应;
(3)NaOH,Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(4)CaO+H2O=Ca(OH)2,Ca(OH)2+CO2=CaCO3↓+H2O.
(2)D转化为B的反应是碳酸钙在高温的条件下生成氧化钙和二氧化碳,满足分解反应一变多的条件,所以反应类型为:分解反应;
(3)碳酸钠和氢氧化钙反应生成碳酸钙白色沉淀和氢氧化钠,因此E溶液中一定有氢氧化钠,化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(4)氧化钙在空气中变质是氧化钙和水反应生成氢氧化钙,氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,化学方程式为:CaO+H2O=Ca(OH)2,Ca(OH)2+CO2=CaCO3↓+H2O.
故答案为:(1)Na2CO3,CaO,CaCO3;
(2)分解反应;
(3)NaOH,Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(4)CaO+H2O=Ca(OH)2,Ca(OH)2+CO2=CaCO3↓+H2O.
点评:在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
如图表示治理汽车尾气所涉及反应的微观过程.下列说法中,不正确的是( )

| A、反应物和生成物中共含有三种元素 |
| B、反应前后原子、分子个数都不变 |
| C、该反应使有毒气体转化为无毒气体 |
| D、反应物和生成物中只有一种单质 |
下列说法正确的是( )
| A、氢氧化钠是碱,碳酸钠是盐,所以可以用酚酞来区别它们的水溶液 |
| B、区别盐酸和硫酸既可以用氯化钡,也可以用硝酸银 |
| C、消石灰是氢氧化钠的俗名,可以用来中和酸性土壤 |
| D、生石灰、苛性钠都可以做干燥剂但不能干燥酸性气体 |
下列关于铁的说法,正确的是( )
A、炼铁的原理是Fe2O3+3CO
| ||||
| B、实验室炼铁时,会发现玻璃管中的粉末由黑色变为红色 | ||||
| C、铁生锈的主要条件是与空气中的二氧化碳直接接触 | ||||
| D、铁锈对铁制品有保护作用,不用清理 |
规范的操作是化学实验成功的保障.下列实验操作中,正确的是( )
A、 验满氧气 |
B、 倾倒液体 |
C、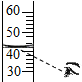 读取液体体积 |
D、 点燃酒精灯 |
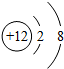 表示的是一种金属原子
表示的是一种金属原子  如图是某同学对二氧化碳部分知识构建的网络图(部分反应条件和生成物省略).
如图是某同学对二氧化碳部分知识构建的网络图(部分反应条件和生成物省略).