题目内容
实验室有一瓶标签破损的硫酸铜溶液,某化学兴趣小组的同学为测定其溶质质量分数,取出80g溶液,向其中逐滴加入溶质质量分数为10%的NaOH溶液.反应过程中生成沉淀的质量与所用NaOH溶液质量的关系如图所示.试求:

(1)这瓶硫酸铜溶液中溶质质量分数.
(2)请你为该瓶溶液制作一张标签.(填入图中)

(1)这瓶硫酸铜溶液中溶质质量分数.
(2)请你为该瓶溶液制作一张标签.(填入图中)
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:由图示可知,当加入NaOH溶液的质量是40g时,两者恰好完全反应.参加反应的NaOH的质量是(注意参加两个字)40g×10%,由参加反应的NaOH的质量就可以求出参加反应的硫酸铜的质量,然后求其质量分数.
解答:解:(1)解:设CuSO4的质量为x
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
160 80
x 40g×10%
=
x=8g
CuSO4%=
×100%=10%
答:这瓶硫酸铜溶液中溶质质量分数为10%.
(2)标签为:
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
160 80
x 40g×10%
| 160 |
| 80 |
| x |
| 40g×10% |
x=8g
CuSO4%=
| 8g |
| 80g |
答:这瓶硫酸铜溶液中溶质质量分数为10%.
(2)标签为:

点评:会从题目中获取信息是正确解决本题的关键.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
下列日常生活中的变化属于物理变化的是( )
| A、牛奶变酸 | B、木已成舟 |
| C、铁锅生锈 | D、烟花燃放 |

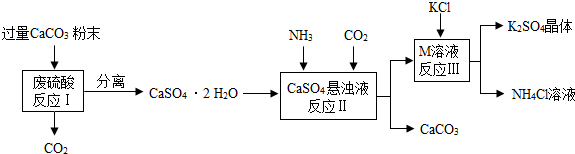
 实验室提供了①太平②量筒③烧杯④玻璃棒⑤胶头滴管等仪器,小华同学用固体硝酸钾配置150克10%的硝酸钾溶液,小亮同学用质量分数为20%盐酸(密度1.1g/cm3)配置110g 10%的稀盐酸.
实验室提供了①太平②量筒③烧杯④玻璃棒⑤胶头滴管等仪器,小华同学用固体硝酸钾配置150克10%的硝酸钾溶液,小亮同学用质量分数为20%盐酸(密度1.1g/cm3)配置110g 10%的稀盐酸.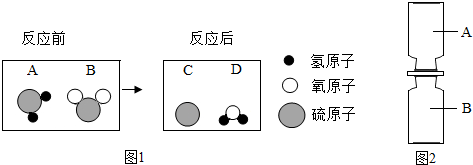
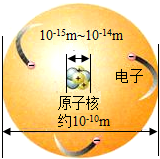 如图所示是锂原子的构成示意图,根据图示信息回答下列问题:
如图所示是锂原子的构成示意图,根据图示信息回答下列问题: 根据如图所示的溶解度曲线,回答下列问题.
根据如图所示的溶解度曲线,回答下列问题.