题目内容
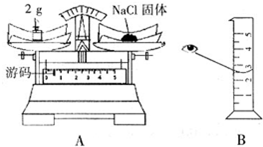 实验室欲配制5g质量分数为50%的NaCl溶液.试回答下列下列问题.分别说明图中A、B操作对实验结果的影响,并改正.
实验室欲配制5g质量分数为50%的NaCl溶液.试回答下列下列问题.分别说明图中A、B操作对实验结果的影响,并改正.
A操作导致所配溶液溶质的质量分数________,(填偏大、偏小或不变,下同)
B操作导致所配溶液溶质的质量分数________.
偏小 偏大
分析:使用托盘天平称量物品时,应该“左物右码”,且物体的质量=砝码的质量+游码的质量;
量筒度数时,应该视线与液面的最低处保持水平.仰视读数时,所量取的液体体积偏大;俯视读数时,所量取的液体体积偏小.
解答:A操作中:使用托盘天平称量NaCl固体时,物品与砝码的位置颠倒了,致使所称取的固体质量偏小,即配制的溶液的溶质质量偏小,则溶液溶质质量分数偏小;
B操作中,俯视读数,会使所量取的液体体积偏小,即配制的溶液的溶剂质量偏小,则溶质质量分数偏大.
故填:偏小;偏大.
点评:此题注意考查了配制一定质量分数的溶液的误差分析.实验是学习化学的基础,所以,必须科学的做实验,减小误差.
分析:使用托盘天平称量物品时,应该“左物右码”,且物体的质量=砝码的质量+游码的质量;
量筒度数时,应该视线与液面的最低处保持水平.仰视读数时,所量取的液体体积偏大;俯视读数时,所量取的液体体积偏小.
解答:A操作中:使用托盘天平称量NaCl固体时,物品与砝码的位置颠倒了,致使所称取的固体质量偏小,即配制的溶液的溶质质量偏小,则溶液溶质质量分数偏小;
B操作中,俯视读数,会使所量取的液体体积偏小,即配制的溶液的溶剂质量偏小,则溶质质量分数偏大.
故填:偏小;偏大.
点评:此题注意考查了配制一定质量分数的溶液的误差分析.实验是学习化学的基础,所以,必须科学的做实验,减小误差.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
 (2012?太原)某实验室欲配制一定溶质质量分数的KNO3溶液,现实验室只有含少量NaCl的KNO3固体药品.
(2012?太原)某实验室欲配制一定溶质质量分数的KNO3溶液,现实验室只有含少量NaCl的KNO3固体药品. 实验室欲配制5g质量分数为50%的NaCl溶液.试回答下列下列问题.分别说明图中A、B操作对实验结果的影响,并改正.
实验室欲配制5g质量分数为50%的NaCl溶液.试回答下列下列问题.分别说明图中A、B操作对实验结果的影响,并改正.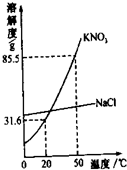 某实验室欲配制一定溶质质量分数的硝酸钾溶液,现实验室只有含少量NaCl的硝酸钾固体药品.
某实验室欲配制一定溶质质量分数的硝酸钾溶液,现实验室只有含少量NaCl的硝酸钾固体药品.