题目内容
2.海南东线高铁的开通,改善了人们的出行.铁轨通常由锰钢制作而成,锰钢属于( )| A. | 金属材料 | B. | 复合材料 | C. | 有机合成材料 | D. | 无机非金属材料 |
分析 金属材料包括铁、铝、铜等纯金属和合金.可以据此结合锰铜的成分来解答.
解答 解:锰铜是由锰和铜混合之后融合而成的混合物,所以属于合金,即属于金属材料,分析所给选项可以知道选项A是正确的.
故选A.
点评 解答这类题目时,首先,要熟记和理解金属材料及其应用等相关知识;然后根据所学的相关知识和技能,按照题目的要求认真地进行选择或解答即可.

练习册系列答案
相关题目
13. 在学习相对原子质量的时候,课本上引用了如图所示的模型图.根据相对原子质量的定义,盘中的每一小块表示的是( )
在学习相对原子质量的时候,课本上引用了如图所示的模型图.根据相对原子质量的定义,盘中的每一小块表示的是( )
 在学习相对原子质量的时候,课本上引用了如图所示的模型图.根据相对原子质量的定义,盘中的每一小块表示的是( )
在学习相对原子质量的时候,课本上引用了如图所示的模型图.根据相对原子质量的定义,盘中的每一小块表示的是( )| A. | 一个碳原子质量的 $\frac{1}{12}$ | B. | 一个氧原子质量的 $\frac{1}{16}$ | ||
| C. | 一个碳原子的质量 | D. | 一个氢原子的质量 |
10.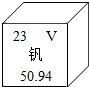 2015年2月,中德科学家成功合成了具有优异的电化学性能的钒的氧化物(V6O13),钒元素的相关信息如图.下列有关钒的说法错误的是( )
2015年2月,中德科学家成功合成了具有优异的电化学性能的钒的氧化物(V6O13),钒元素的相关信息如图.下列有关钒的说法错误的是( )
 2015年2月,中德科学家成功合成了具有优异的电化学性能的钒的氧化物(V6O13),钒元素的相关信息如图.下列有关钒的说法错误的是( )
2015年2月,中德科学家成功合成了具有优异的电化学性能的钒的氧化物(V6O13),钒元素的相关信息如图.下列有关钒的说法错误的是( )| A. | 原子的核外电子数是23 | B. | 原子核内的中子数是28 | ||
| C. | 相对原子质量为50.94 | D. | 属于稀有气体元素 |
7.同学们对制作糕点常用膨松剂Na2CO3或NaHCO3进行了下列探究.
【查阅资料】
表1
表2
【探究一】NaHCO3和Na2CO3性质差异的探究
(1)现有20℃时溶质质量分数为8%的Na2CO3和NaHCO3溶液酸碱性:取样于试管中,分别滴加紫色石蕊试液,均显蓝色;酸碱度:NaHCO3溶液<Na2CO3溶液(填“>”或”“<”).
(2)稳定性:按图1,实验中可观察乙烧杯中的石灰水变浑浊,对应试管中发生反应的化学方程式为:
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
结论:在受热条件下,碳酸钠比碳酸氢钠稳定性强(填“强”或“弱”).
(3)利用溶解度鉴别NaHCO3和Na2CO3:分别取Xg两种固体粉末加入20℃,10g水中充分溶解,通过观察溶解现象来区分,X可以是下列的A.(选填A、B或C)
A.2g B.0.96g C.0.5g
【问题讨论】
(4)实验结束时,应先B(选填A或B).
A.熄灭酒精灯 B.将甲、乙烧杯移开
(5)甲认为探究稳定性实验中,由于受热时两物质温度不同,不能得到(2)中的结论,经对装置设计讨论后一致认为可以得到上述结论,理由是碳酸氢钠的受热温度低于碳酸钠的受热温度.
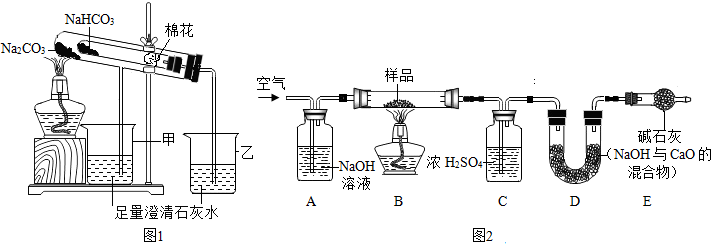
【探究二】测定NaHCO3和Na2CO3混合物10.0g中NaHCO3的质量分数(图2,夹持装置略)
【问题讨论】
(6)实验前先通一段时间的空气的目的是把装置中的二氧化碳排尽;
(7)A的作用是吸收空气中的二氧化碳,若没有装置E,NaHCO3的质量分数测定结果会偏大(填“偏大”、“不变”或“偏小”).
(8)停止加热后,仍继续通入空气一段时间,目的是把反应生成的二氧化碳完全排入D中.
【含量测定】
(9)测得装置D的质量实验前为122.2g,实验后为124.4g,计算该样品中NaHCO3的质量分数.(要有计算过程)
【知识拓展】
(10)向Na2CO3溶液中通入CO2气体可以生成NaHCO3,该反应的化学反应方程式为:Na2CO3+CO2+H2O=2NaHCO3.
【查阅资料】
表1
| 20℃ | 8%Na2CO3溶液 | 8%NaHCO3溶液 |
| pH | 10.6 | 8.0 |
| 溶解度 | 10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
(1)现有20℃时溶质质量分数为8%的Na2CO3和NaHCO3溶液酸碱性:取样于试管中,分别滴加紫色石蕊试液,均显蓝色;酸碱度:NaHCO3溶液<Na2CO3溶液(填“>”或”“<”).
(2)稳定性:按图1,实验中可观察乙烧杯中的石灰水变浑浊,对应试管中发生反应的化学方程式为:
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
结论:在受热条件下,碳酸钠比碳酸氢钠稳定性强(填“强”或“弱”).
(3)利用溶解度鉴别NaHCO3和Na2CO3:分别取Xg两种固体粉末加入20℃,10g水中充分溶解,通过观察溶解现象来区分,X可以是下列的A.(选填A、B或C)
A.2g B.0.96g C.0.5g
【问题讨论】
(4)实验结束时,应先B(选填A或B).
A.熄灭酒精灯 B.将甲、乙烧杯移开
(5)甲认为探究稳定性实验中,由于受热时两物质温度不同,不能得到(2)中的结论,经对装置设计讨论后一致认为可以得到上述结论,理由是碳酸氢钠的受热温度低于碳酸钠的受热温度.
【探究二】测定NaHCO3和Na2CO3混合物10.0g中NaHCO3的质量分数(图2,夹持装置略)

【问题讨论】
(6)实验前先通一段时间的空气的目的是把装置中的二氧化碳排尽;
(7)A的作用是吸收空气中的二氧化碳,若没有装置E,NaHCO3的质量分数测定结果会偏大(填“偏大”、“不变”或“偏小”).
(8)停止加热后,仍继续通入空气一段时间,目的是把反应生成的二氧化碳完全排入D中.
【含量测定】
(9)测得装置D的质量实验前为122.2g,实验后为124.4g,计算该样品中NaHCO3的质量分数.(要有计算过程)
【知识拓展】
(10)向Na2CO3溶液中通入CO2气体可以生成NaHCO3,该反应的化学反应方程式为:Na2CO3+CO2+H2O=2NaHCO3.
11.漂白粉的主要成分为次氯酸钙[Ca(ClO)2]和氯化钙,即可用作漂白剂,又可用作消毒剂.漂白粉中有效成分是
[Ca(ClO)2],漂白的原理是:Ca(ClO)2在空气中发生反应Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO;HClO是一种酸性比盐酸弱的酸,不稳定,具有漂白性,能使品红等有色物质褪色.
(1)漂白粉是一种混合物(填“纯净物”或“混合物”).
(2)HClO在常温下分解,反应为2HClO═2HCl+O2↑.某瓶HClO溶液放置一段时间后,溶液的pH减小(填“增大”或“减小”或“不变”).
(3)在漂白粉中滴加盐酸,能加快漂白的速率.写出漂白粉中加入盐酸反应的化学方程式Ca(ClO)2 +2HCl=2HClO+CaCl2.
(4)有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验.
【提出问题】长时间放置的漂白粉是否变质?
【猜想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为CaCl2、Ca(ClO)2、CaCO3;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3.
【实验探究】限选试剂及仪器:盐酸、石灰水、品红溶液、试管、带导管的单孔塞.
[Ca(ClO)2],漂白的原理是:Ca(ClO)2在空气中发生反应Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO;HClO是一种酸性比盐酸弱的酸,不稳定,具有漂白性,能使品红等有色物质褪色.
(1)漂白粉是一种混合物(填“纯净物”或“混合物”).
(2)HClO在常温下分解,反应为2HClO═2HCl+O2↑.某瓶HClO溶液放置一段时间后,溶液的pH减小(填“增大”或“减小”或“不变”).
(3)在漂白粉中滴加盐酸,能加快漂白的速率.写出漂白粉中加入盐酸反应的化学方程式Ca(ClO)2 +2HCl=2HClO+CaCl2.
(4)有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验.
【提出问题】长时间放置的漂白粉是否变质?
【猜想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为CaCl2、Ca(ClO)2、CaCO3;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3.
【实验探究】限选试剂及仪器:盐酸、石灰水、品红溶液、试管、带导管的单孔塞.
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,加入适量盐酸,塞上带导管的单孔塞 把导管插入另一试管里的石灰水中. | 有气体产生,气体使石灰水变浑浊. | 猜想2成立 |
| ②在上述反应后的试管中加少量品红溶液. | 品红溶液褪色. |
12.《科学》课本上是用图甲的装置来测定空气中氧气的体积分数.而小明通过查询资料对该实验进行改进,利用四硫化钠
(Na2S4)固体替代红磷进行实验,其反应原理为:
2Na2S4+O2+2H2O═8S↓+4NaOH.
实验步骤:
①将足量的四硫化钠(Na2S4)固体置于试管中,再加入适量的水并迅速塞紧橡胶塞,再充分振荡.
②测量液面至橡胶塞下沿的距离,记录数据h1(如图乙所示).
③将该试管插入水中(如图丙所示),取下橡胶塞,观察到试管内液面上升.
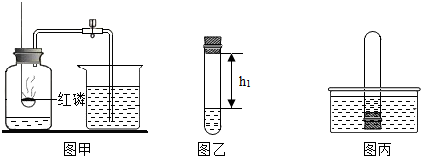
④当管内液面稳定时塞紧橡胶塞.将试管取出,倒转过来,测量液面至橡胶塞下沿的距离,记录数据h2.
⑤按照①~③再重复实验2次,3次实验数据如表所示.
(1)步骤①中进行充分振荡的目的是使反应物充分反应.
(2)根据3次实验数据,请你计算空气中氧气的体积分数为20.9%(结果精确到0.1%);
(3)小明设计的实验与课本上的实验相比,其优点是节能、装置简单、气密性好等.(写出2点)
(Na2S4)固体替代红磷进行实验,其反应原理为:
2Na2S4+O2+2H2O═8S↓+4NaOH.
实验步骤:
①将足量的四硫化钠(Na2S4)固体置于试管中,再加入适量的水并迅速塞紧橡胶塞,再充分振荡.
②测量液面至橡胶塞下沿的距离,记录数据h1(如图乙所示).
③将该试管插入水中(如图丙所示),取下橡胶塞,观察到试管内液面上升.

④当管内液面稳定时塞紧橡胶塞.将试管取出,倒转过来,测量液面至橡胶塞下沿的距离,记录数据h2.
⑤按照①~③再重复实验2次,3次实验数据如表所示.
| 第1次 | 第2次 | 第3次 | |
| h1/厘米 | 11.0 | 11.4 | 11.6 |
| h2/厘米 | 8.7 | 9.1 | 9.2 |
(2)根据3次实验数据,请你计算空气中氧气的体积分数为20.9%(结果精确到0.1%);
(3)小明设计的实验与课本上的实验相比,其优点是节能、装置简单、气密性好等.(写出2点)