题目内容
某合金可能由铜与镁、锌中的一种组成,现欲测定其组成,进行如下实验:取该合金样品30g放入烧杯中,然后将200g溶质质量分数为19.6%的稀硫酸平均分四次依次加入该烧杯中,每次均充分反应.实验数据如下: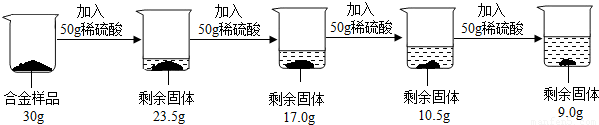
请计算:
(1)该合金中铜的质量分数为______.
(2)该合金除铜外,另一种金属是______.(写出过程)
(3)第三次加入稀硫酸充分反应后,所得溶液中溶质的质量分数.
【答案】分析:(1)由图中信息可以知道,在前三次加入稀硫酸时,固体质量均减少6.5g,但是第四次加入稀硫酸固体质量只减少了1.5g,说明第四次中稀硫酸有剩余,所以固体中铜的质量为9.0g,可以据此求算出铜的质量分数;
(2)由(1)的分析可以知道,6.5g金属和50g稀硫酸恰好完全反应,可以据此结合+2价的金属与酸反应的化学方程式,判断出金属种类;
(3)根据判断出的金属,写出化学方程式,求算出所生成的硫酸盐,然后结合溶质的质量分数的计算公式即可求算出反应后所得溶液中溶质的质量分数.
解答:解:(1)由图中信息可以知道,在前三次加入稀硫酸时,固体质量均减少6.5g,但是第四次加入稀硫酸固体质量只减少了1.5g,说明第四次中稀硫酸有剩余,所以固体中铜的质量为9.0g,所以铜的质量分数为: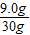 ×100%=30%;
×100%=30%;
(2)6.5g金属和50g稀硫酸恰好完全反应,其中硫酸的质量为:50g×19.6%=镁和锌在发生置换反应时都生成+2价的硫酸盐,故设金属的相对原子质量为X,则:
M+H2SO4═MSO4 +H2↑
X 98
6.5g 9.8g
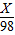 =
=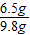
解得:X=65,
所以该金属为锌;
(3)第三次加入稀硫酸充分反应后,生成硫酸锌的质量为y,氢气的质量为z,则:
Zn+H2SO4═ZnSO4+H2↑
98 161 2
9.8g×3 y z
=29.4g
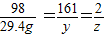
解得:y=48.3g,z=0.6g;
所得溶液中溶质的质量分数为: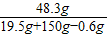 ×100%=28.6%.
×100%=28.6%.
答:第三次加入稀硫酸充分反应后,所得溶液中溶质的质量分数为28.6%.
故答案为:(1)30%;(2)锌;(3)28.6%.
点评:要想解答好这类题目,首先,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.然后,根据所给的问题情景或图表信息等,结合所学的相关知识和技能,细致地分析题意(或图表信息)等各种信息资源,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.
(2)由(1)的分析可以知道,6.5g金属和50g稀硫酸恰好完全反应,可以据此结合+2价的金属与酸反应的化学方程式,判断出金属种类;
(3)根据判断出的金属,写出化学方程式,求算出所生成的硫酸盐,然后结合溶质的质量分数的计算公式即可求算出反应后所得溶液中溶质的质量分数.
解答:解:(1)由图中信息可以知道,在前三次加入稀硫酸时,固体质量均减少6.5g,但是第四次加入稀硫酸固体质量只减少了1.5g,说明第四次中稀硫酸有剩余,所以固体中铜的质量为9.0g,所以铜的质量分数为:
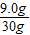 ×100%=30%;
×100%=30%;(2)6.5g金属和50g稀硫酸恰好完全反应,其中硫酸的质量为:50g×19.6%=镁和锌在发生置换反应时都生成+2价的硫酸盐,故设金属的相对原子质量为X,则:
M+H2SO4═MSO4 +H2↑
X 98
6.5g 9.8g
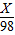 =
=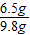
解得:X=65,
所以该金属为锌;
(3)第三次加入稀硫酸充分反应后,生成硫酸锌的质量为y,氢气的质量为z,则:
Zn+H2SO4═ZnSO4+H2↑
98 161 2
9.8g×3 y z
=29.4g
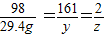
解得:y=48.3g,z=0.6g;
所得溶液中溶质的质量分数为:
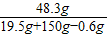 ×100%=28.6%.
×100%=28.6%.答:第三次加入稀硫酸充分反应后,所得溶液中溶质的质量分数为28.6%.
故答案为:(1)30%;(2)锌;(3)28.6%.
点评:要想解答好这类题目,首先,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.然后,根据所给的问题情景或图表信息等,结合所学的相关知识和技能,细致地分析题意(或图表信息)等各种信息资源,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
某合金可能由铜与镁、锌中的一种组成,现欲测定其组成,进行如下实验:取该合金样品10.0g放入烧杯中,然后将56.0g溶质质量分数为14.0%的稀硫酸平均分四次依次加入该烧杯中,每次均充分反应.实验数据记录如下表:
试求:
(1)该合金中铜的质量分数是 .
(2)该合金除了铜外,另一种金属的是什么呢?(写出过程)
(3)第三次加入硫酸充分反应后,所得溶液中溶质的质量分数是多少?(写出计算过程,结果精确到0.1%)
| 编 号 | 1 | 2 | 3 | 4 |
| 加入硫酸的质量/g | 14 | 14 | 14 | 14 |
| 剩余固体的质量/g | 8.7 | 7.4 | 6.1 | 6.0 |
(1)该合金中铜的质量分数是
(2)该合金除了铜外,另一种金属的是什么呢?(写出过程)
(3)第三次加入硫酸充分反应后,所得溶液中溶质的质量分数是多少?(写出计算过程,结果精确到0.1%)



