题目内容
碳酸氢钠是一种重要的盐类物质,在生活中用途广泛.小红同学设计实验对碳酸氢钠的性质进行了探究.请你参与她的探究活动.
【探究实验1】碳酸氢钠溶液的酸碱性.
【实验方案】取少量该固体加入试管中,加适量水溶解,再滴入几滴酚酞试液,振荡.
现象:溶液变成浅红色. 结论:
【探究实验2】能与酸反应.
【实验方案】取少量该固体加入试管中,滴加稀盐酸.
现象: 应的化学方程式为:
【探究实验3】碳酸氢钠的热稳定性.
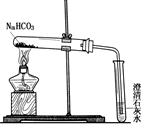
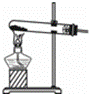
【实验方案】设计实验装置如图,并进行实验.
现象:试管口有水珠出现,澄清石灰水变浑浊.充分加热后,试管中留下白色固体.
结论:碳酸氢钠受热有二氧化碳、水和白色固体生成.
请你帮小红设计实验,证明试管中留下的白色固体是Na2CO3,而不是NaOH.(所选试剂不能用酸)
步骤: 象:
试写出碳酸氢钠受热发生反应的化学方程式:
【拓展应用】根据以上探究,请说出碳酸氢钠在日常生活中的一种用途
【考点】实验探究物质的性质或变化规律;常用盐的用途;盐的化学性质;书写化学方程式、文字表达式、电离方程式.
【专题】实验现象的观察和记录;科学探究.
【分析】【探究实验1】碱性溶液能使酚酞试液变红;
【探究实验2】碳酸盐和酸反应生成二氧化碳;
【探究实验3】根据反应物和生成物书写化学方程式;区分碳酸钠和氢氧化钠可用钙盐的溶液,根据生成沉淀区别;碳酸钙不溶于水;
【拓展应用】根据碳酸氢钠能和酸反应的性质填空.
【解答】解:【探究实验1】因为碱性溶液能使酚酞变红,所以此现象说明碳酸氢钠溶液呈碱性.
【探究实验2】碳酸氢钠和盐酸反应二氧化碳气体,会看到溶液中能产生气泡.③反应的化学方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑.
【探究实验3】碳酸钠能和氢氧化钙反应生成沉淀,而氢氧化钠和氢氧化钙不反应,故取少量该固体加入试管中,加适量水溶解,再滴入澄清石灰水;二氧化碳能使澄清石灰水溶液变浑浊;碳酸氢钠受热发生反应的化学方程式 2NaHCO3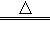 Na2CO3+H2O+CO2↑.
Na2CO3+H2O+CO2↑.
【拓展应用】碳酸氢钠能和酸反应生成二氧化碳,故可以用作治疗胃酸的药物(或用作发酵粉).
故答案为:【探究实验1】碳酸氢钠溶液呈碱性;
【探究实验2】产生气泡;
【探究实验3】NaHCO3+HCl=NaCl+H2O+CO2↑;取少量该固体加入试管中,加适量水溶解,再滴入澄清石灰水;
溶液变浑浊;2NaHCO3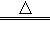 Na2CO3+H2O+CO2↑;
Na2CO3+H2O+CO2↑;
【拓展应用】治疗胃酸的药物(或用作发酵粉).
【点评】碳酸盐和酸反应放出二氧化碳气体,二氧化碳能使石灰水变浑浊,碳酸盐溶液能和钙盐溶液反应生成沉淀,这些都是解题的关键所在.

下列图示操作正确的是 ( )
|
| A. |
液体读数 | B. |
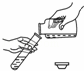
滴加液体 | C. |
加热固体 | D. |
倾倒液体 |
 B.
B. C.
C. D.
D.
 X产生.则X,Y,Z三种金属的活动性由强到弱的顺序为
X产生.则X,Y,Z三种金属的活动性由强到弱的顺序为