题目内容
一个碳-12原子的质量为1.993×10-26 千克,镁原子的相对原子质量为24,则一个镁原子的质量是( )
| A、24 千克 |
| B、24 |
| C、3.986×10-26 千克 |
| D、1.67×10-27 千克 |
考点:相对原子质量的概念及其计算方法
专题:物质的微观构成与物质的宏观组成
分析:以一种碳原子质量的
为标准,其他原子的质量跟它相比较所得到的比,作为这种原子的相对原子质量.
用公式表示为:某原子的相对原子质量=
,将数据代入公式计算.
| 1 |
| 12 |
用公式表示为:某原子的相对原子质量=
| 该原子的质量 | ||
碳原子质量×
|
解答:解:由相对原子质量═
,可知:镁原子的实际质量=24×1.993×10-26kg×
=3.986×10-26 kg;
故选C
| 该原子的质量 | ||
碳原子质量×
|
| 1 |
| 12 |
故选C
点评:解答有关相对原子质量的计算题时,要注意相对原子质量是一个比值,是原子的实际质量和碳原子质量的
之比,掌握此知识点就能轻松解题.
| 1 |
| 12 |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
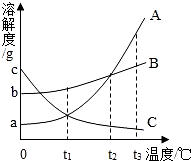 如图所示是A、B、C三种固体物质的溶解度曲线.下列说法正确的是( )
如图所示是A、B、C三种固体物质的溶解度曲线.下列说法正确的是( )| A、在t1℃时,A、B两种物质饱和溶液的溶质质量分数相等 |
| B、在t3℃时,若10g水最多能溶解3g B物质,则10g水最多能溶解A物质的质量小于3g |
| C、三种物质的溶解度关系为B>A>C时的温度为t℃,则t的取值范围是t1<t<t2 |
| D、将A、B、C三种物质的饱和溶液从t2℃降温到t1℃时,溶质质量分数保持不变的是A和B |
在一密闭容器中,有甲、乙、丙、丁四种物质,在一定的条件下,充分反应,测得反应前后各物质质量如下表:
则下列说法正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(g) | 23 | 27 | 0 | 19 |
| 反应后质量(g) | 待测 | 2 | 58 | 5 |
| A、反应后甲的质量为4克 |
| B、该反应的类型为化合反应 |
| C、反应中甲乙质量比为2:1 |
| D、丙物质一定是化合物 |
将一定量的乙醇和氧气置于一个完全封闭的容器中引燃,反应生成二氧化碳、水蒸气和一种未知物X.测得反应前后物质的质量如下表:
下列判断正确的是( )
| 物 质 | 乙醇 | 氧气 | 二氧化碳 | 水 | X |
| 反应前质量/g | 4.6 | 8 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 4.4 | 5.4 | m |
| A、表中m的值为2.8 |
| B、X可能是该反应的催化剂 |
| C、减少氧气的量可以减少X的生成 |
| D、物质X一定含有碳元素,可能含有氢元素 |
对比三个反应的异同点,对以下三个化学反应的分析正确的是( )
C+O2
CO2 P+O2
P2O5 CH4+O2
O2+H2O.
C+O2
| 点燃 |
| 点燃 |
| 点燃 |
| A、反应物均是单质 |
| B、都属于化合反应 |
| C、都属于氧化反应 |
| D、都属于分解反应 |
如图为初中化学常见气体的发生装置与收集装置,有关这些装置的说法不正确的是( )
A、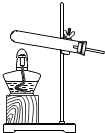 如图装置可作为加热固体制取气体的发生装置 |
B、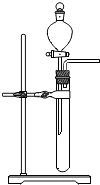 如图装置中分液漏斗的作用是方便添加液体药品 |
C、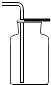 如图装置可用于收集H2、CO2 |
D、 如图装置可用于收集H2、O2 |
 某研究小组在学习氧气的化学性质时发现:铁丝在氧气中燃烧没有火焰,蜡烛燃烧却有明亮的火焰,该小组同学进行了如下探究.
某研究小组在学习氧气的化学性质时发现:铁丝在氧气中燃烧没有火焰,蜡烛燃烧却有明亮的火焰,该小组同学进行了如下探究.