题目内容
14. 请根据A、B两种固体物质的溶解度曲线回答下列问题.
请根据A、B两种固体物质的溶解度曲线回答下列问题.(1)温度为t1℃时,A与B物质的溶解度相等;
(2)在保持其中溶剂质量不变的条件下,将常温下B的不饱和溶液变成饱和溶液,可行的方法是加入溶质.
(3)现有一杯t1℃时含A、B两种物质且均饱和的混合溶液,若要从中分离出A,其操作方法是降温结晶.
(4)下列说法正确的是CD
A.t2℃时,A溶液中溶质的质量分数一定比B溶液中溶质的质量分数大
B.将t2℃时,A、B的饱和溶液分别降温至t1℃,此时两溶液中的质量分数相等
C.在t1℃时,用两份等量的水分别配制成A、B的饱和溶液,这两种溶液的质量相等
D.在t2℃时,用等量的A、B分别配制成两种饱和溶液,其质量分别mg和ng,则m<n.
分析 根据题目信息和溶解度曲线可知:A固体物质的溶解度,是随温度升高而增大,而B的溶解度随温度的升高而减少;温度为t1℃时,A与B物质的溶解度相等;在保持其中溶剂质量不变的条件下,将常温下B的不饱和溶液变成饱和溶液,可行的方法是加入溶质;若要从中分离出A,其操作方法是降温结晶;说法正确的是:在t1℃时,用两份等量的水分别配制成A、B的饱和溶液,这两种溶液的质量相等,因为该温度下它们有交点;在t2℃时,用等量的A、B分别配制成两种饱和溶液,其质量分别mg和ng,则m<n,因为该温度下A的溶解度大于B.
解答 解:(1)温度为t1℃时,A与B物质的溶解度相等,因为它们在该温度下有交点;故答案为:t1;
(2)在保持其中溶剂质量不变的条件下,将常温下B的不饱和溶液变成饱和溶液,可行的方法是加入溶质;故答案为:加入溶质;
(3)若要从中分离出A,其操作方法是降温结晶,因为A固体物质的溶解度,是随温度升高而增大,而B的溶解度随温度的升高而减少,故答案为:降温结晶;
(4)说法正确的是:在t1℃时,用两份等量的水分别配制成A、B的饱和溶液,这两种溶液的质量相等,因为该温度下它们有交点;在t2℃时,用等量的A、B分别配制成两种饱和溶液,其质量分别mg和ng,则m<n,因为该温度下A的溶解度大于B;t2℃时,A溶液中溶质的质量分数一定比B溶液中溶质的质量分数大错误,因为没有指明是饱和溶液;将t2℃时,A、B的饱和溶液分别降温至t1℃,此时两溶液中的质量分数相等错误,因为B的溶解度随温度的升高而减少;故答案为:CD;
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液结晶的方法和溶质质量分数的变化等,本考点主要出现在选择题和填空题中.

练习册系列答案
相关题目
13.下列实验方案不能达到实验目的是( )
| 实验目的 | 实验方案 | |
| A | 验证铝、铜、银三种金属的活动性顺序 | 将洁净的铜丝分别浸入硫酸铝溶液和硝酸银溶液中 |
| B | 用一种试剂一次性鉴别出稀硫酸、澄清石灰水和碳酸钠溶液 | 分别取样,滴加紫色石蕊试液 |
| C | 除去碳粉中混有的少量氧化铜 | 加入足量的稀硫酸,过滤、洗涤、干燥 |
| D | 检验露置的氢氧化钠是否变质 | 取样,加水溶解,滴加氯化钡溶液 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
5.物质在“潮湿的空气”中发生变化与空气中某些气体有关.下列说法不正确的是( )
| A. | 钢铁生锈与氧气、水蒸气有关 | |
| B. | 氢氧化钠固体潮解、变质,与水蒸气、二氧化碳有关 | |
| C. | 铜器表面生成铜绿[Cu2(OH)2CO3]与O2、CO2、水蒸气有关 | |
| D. | 生石灰堆放久了变质与氧气有关 |
9.根据实践经验,你认为下列课外实验不能成功的是( )
| A. | 制取氧气时用注射器代替分液漏斗 | B. | 用食盐水鉴别硬水和软水 | ||
| C. | 在塑料桶内配制农药波尔多液 | D. | 用点燃的方法鉴别羊毛和涤纶 |
19.下列区分各组物质的两种方案都合理的是( )
| 选项 | A | B | C | D |
| 物质 | 碳酸钠和氢氧化钠 | 空气和氧气 | 尿素和硫酸铵 | 木炭和二氧化锰 |
| 方案一 | 稀盐酸 | 带火星的木条 | 氢氧化钠溶液 | 观察颜色 |
| 方案二 | 酚酞试液 | 燃烧的木条 | 加水 | 加热 |
| A. | A | B. | B | C. | C | D. | D |
6.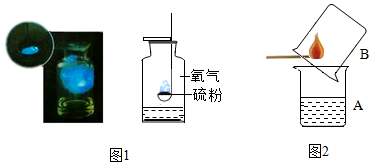 硫的外观为淡黄色脆性结晶或粉末,俗称硫磺.它有特殊臭味且不溶解于水,微溶于乙醇,易溶于二硫化碳.
硫的外观为淡黄色脆性结晶或粉末,俗称硫磺.它有特殊臭味且不溶解于水,微溶于乙醇,易溶于二硫化碳.
【实验1】在燃烧匙中放入少量硫粉,将燃烧匙放在酒精灯火焰上加热,观察到的现象是发出淡蓝色火焰,产生有刺激性气味的气体,放出热量;然后,将燃烧匙连燃着的硫一起伸入充满氧气的集气瓶中,这时你所能观察到的不同现象是燃烧更剧烈,发出明亮的蓝紫色火焰;上述实验中发生反应的化学方程式是S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.
【实验2】
(1)用一支50mL的注射器从充满二氧化硫的集气瓶中抽取40mL二氧化硫,再从小烧杯中抽取10mL滴有紫色石蕊试液的水溶液,用橡皮塞堵住注射器的针孔,慢慢压缩注射器栓塞,观察到的实验现象是溶液变为红色.
(2)将另一支50mL的注射器抽取40mL的空气,再从小烧杯中抽取10mL滴有紫色石蕊试液的水溶液,用橡皮塞堵住注射器的针孔,慢慢压缩注射器栓塞,所观察到的实验现象是无明显现象.
【实验3】如图2所示,先在小烧杯A中加入少量浅紫红色的稀高锰酸钾溶液,再取一根小木条,在一头蘸一些硫粉并点燃,迅速伸入烧杯B中,片刻后立即取出小木条,振荡烧杯A,观察发现高锰酸钾溶液褪色,化学方程式为:2KMnO4+5SO2+2H2O═K2O4+MnSO4+2H2SO4(标出有化合价发生变化的元素的化合价).
此反应用四种基本反应类型无法界定,但因其有元素化合价升降,称之为氧化-还原反应.
 硫的外观为淡黄色脆性结晶或粉末,俗称硫磺.它有特殊臭味且不溶解于水,微溶于乙醇,易溶于二硫化碳.
硫的外观为淡黄色脆性结晶或粉末,俗称硫磺.它有特殊臭味且不溶解于水,微溶于乙醇,易溶于二硫化碳.【实验1】在燃烧匙中放入少量硫粉,将燃烧匙放在酒精灯火焰上加热,观察到的现象是发出淡蓝色火焰,产生有刺激性气味的气体,放出热量;然后,将燃烧匙连燃着的硫一起伸入充满氧气的集气瓶中,这时你所能观察到的不同现象是燃烧更剧烈,发出明亮的蓝紫色火焰;上述实验中发生反应的化学方程式是S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.
【实验2】
(1)用一支50mL的注射器从充满二氧化硫的集气瓶中抽取40mL二氧化硫,再从小烧杯中抽取10mL滴有紫色石蕊试液的水溶液,用橡皮塞堵住注射器的针孔,慢慢压缩注射器栓塞,观察到的实验现象是溶液变为红色.
(2)将另一支50mL的注射器抽取40mL的空气,再从小烧杯中抽取10mL滴有紫色石蕊试液的水溶液,用橡皮塞堵住注射器的针孔,慢慢压缩注射器栓塞,所观察到的实验现象是无明显现象.
【实验3】如图2所示,先在小烧杯A中加入少量浅紫红色的稀高锰酸钾溶液,再取一根小木条,在一头蘸一些硫粉并点燃,迅速伸入烧杯B中,片刻后立即取出小木条,振荡烧杯A,观察发现高锰酸钾溶液褪色,化学方程式为:2KMnO4+5SO2+2H2O═K2O4+MnSO4+2H2SO4(标出有化合价发生变化的元素的化合价).
| Mn化合价 | +7 | +6 | +4 | +2 | 0 |
| 化学式 | KMnO4 | K2MnO4 | MnO2 | MnSO4 | Mn |
| 类别 | 盐 | 盐 | 氧化物 | 盐 | 单质 |
4.选择下列部分实验操作可完成两个实验,甲实验为除去粗盐中难溶性的杂质,乙实验为配制溶质质量分数为10%的氯化钠溶液.下列说法正确的是( )


| A. | 操作①和⑤中玻璃棒的作用是相同的 | |
| B. | 甲实验和乙实验都要用到的实验操作① | |
| C. | 甲实验在操作⑤时,将水全部蒸发后停止加热 | |
| D. | 乙实验在操作③时,若俯视读数,会使所配制溶液的溶质质量分数偏小 |
