题目内容
19.某同学用锌和稀硫酸制取氢气.向气体发生装置中加入一定量的锌粒,将30g稀硫酸分三次加入,每次生成气体的质量如表.| 次数 | 第一次 | 第二次 | 第三次 |
| 加入稀硫酸质量/g | 10 | 10 | 10 |
| 生成氢气质量/g | 0.04 | 0.04 | 0.02 |
(2)所用稀硫酸的溶质质量分数.
(3)反应前后,装置内锌元素的质量不变(填“增大”“不变”或“变小)
分析 根据表格提供的信息结合锌与硫酸的反应进行分析解答即可,锌能与稀硫酸反应生成硫酸锌和氢气,据此解答.
解答 解:(1)根据表格可以看出,生成的氢气的质量=0.04g+0.04+0.02g=0.1g,故填0.1;
(2)利用第一次或第二次反应生成氢气的质量结合锌与硫酸反应的化学方程式,可计算出H2SO4的质量,设10g硫酸中含有溶质的质量为x
Zn+H2SO4=ZnSO4+H2↑
98 2
x 0.04g
$\frac{98}{x}=\frac{2}{0.04g}$
x=1.96g
稀硫酸的溶质质量分数=$\frac{1.96g}{10g}$×100%=19.6%
(3)锌元素在反应前没有损失,故反应前后,锌元素的质量不变.
答案:
(1)0.1
(2)稀硫酸的溶质质量分数为19.6%.
(3)不变.
点评 本题考查的是根据化学方程式的计算的知识,完成此题,可以依据题干提供的数据结合已有的知识进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列各组物质能相互反应且反应后溶液质量增加的是( )
| A. | 二氧化碳和澄清石灰水 | B. | 硝酸钡溶液和硫酸钠溶液 | ||
| C. | 碳酸镁和稀盐酸 | D. | 钢丝和硫酸锌溶液 |
9.以下实验现象的描述,正确的是( )
| A. | 铁丝在空气中剧烈燃烧,火星四射,生成黑色固体 | |
| B. | 碳在氧气中燃烧发出白光,放出大量的热,生成无色无味的气体 | |
| C. | 硫在氧气中燃烧产生微弱的淡蓝色火焰,并生成刺激性气味的气体 | |
| D. | 红磷在氧气中燃烧发出耀眼的白光,并产生大量的白雾 |
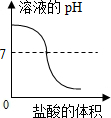
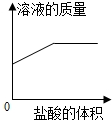
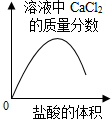
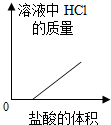
 A~E是盐酸、氢氧化钠、氢氧化钙、碳酸钠、二氧化碳中的一种.其中A是人体胃液的主要成分.它们相互间发生反应或转化的关系如图所示(“-”表面两种物质间能发生反应,“→”表示两种物质间的转化关系).
A~E是盐酸、氢氧化钠、氢氧化钙、碳酸钠、二氧化碳中的一种.其中A是人体胃液的主要成分.它们相互间发生反应或转化的关系如图所示(“-”表面两种物质间能发生反应,“→”表示两种物质间的转化关系).