题目内容
10.以下为制备纳米CaCO3的一种流程: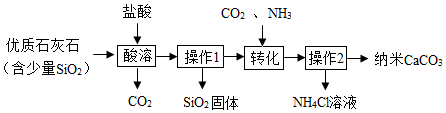
(1)实验室中进行操作1、2时,所用玻璃仪器有漏斗、玻璃棒和烧杯.
(2)过程中的生成物可直接应用于流程的是二氧化碳.
(3)为了提高“转化”速率,可采取的措施有ab(选填序号).
a、搅拌溶液 b、适当增大通入气体的速率 c、加热溶液至100℃
(4)操作2所得固体用蒸馏水洗涤.检验固体已洗净的方法是取最后一次洗涤后的滤液,滴加硝酸银溶液,无现象.
分析 (1)根据过滤的仪器进行分析;
(2)从图中可以看出过程中的生成物可直接应用于流程的是二氧化碳;
(3)为了提高“转化”速率,可采取的措施有搅拌溶液,适当增大通入气体的速率;
(4)根据溶液中的成分选择检验方法.
解答 解:(1)实验室中进行操作过滤时,所用玻璃仪器有漏斗、玻璃棒和烧杯,故填:漏斗.
(2)从图中可以看出过程中的生成物可直接应用于流程的是二氧化碳,故填:二氧化碳.
(3)为了提高“转化”速率,可采取的措施有搅拌溶液,适当增大通入气体的速率,故填:ab.
(4)检验固体已洗净的方法是取最后一次洗涤后的滤液,滴加硝酸银溶液,无现象,说明已洗净,故填:取最后一次洗涤后的滤液,滴加硝酸银溶液,无现象.
点评 此题难度不大,掌握过滤操作以及物质的性质等即可顺利解答.

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案
相关题目
20.某同学用量筒量取液体,视线与量筒内液体的凹液面最低处保持水平,读数为30毫升;倒出部分液体后,仰视读数为18毫升.则该学生实际倒出的液体体积( )
| A. | 小于12毫升 | B. | 等于12毫升 | C. | 大于12毫升 | D. | 无法确定范围 |
18.皮蛋又称松花蛋,因其风味独特,深受人们喜爱.某兴趣小组在市场上获得了少许腌制皮蛋的原料.拿到实验室进行实验.将该固体混合物放于烧杯中,缓慢加入足量的蒸馏水,充分溶解后过滤,得到白色沉淀A和无色澄清滤液B.
【提出问题】(1)白色沉淀A是什么?
(2)无色滤液B中的溶质有哪些?
【查阅资料】腌制皮蛋的原料配方是少量NaCl、CaO和过量Na2CO3的固体混合物.
【理论推理】(1)白色沉淀A是CaCO3,请写出生成该沉淀的化学方程式Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
(2)滤液B中含有Na2CO3、NaOH、NaCl三种溶质.
【实验验证】为证明滤液B中存在的三种溶质,同学们进行了如下实验.
【拓展提升】
(1)向步骤 I中加入过量Ba(NO3)2溶液的目的是验证并除去溶液中的Na2CO3.
(2)小妮同学认为若将步骤I中的Ba(NO3)2溶液换为BaCl2溶液,进行以上实验,最终也能证明滤液B中存在的三种溶质.你认为是否合理不合理(填“合理”或“不合理”).
(3)小轩同学认为向滤液B中先加入酚酞溶液,后加入过量的Ba(NO3)2溶液,也能得出滤液B的溶质中含有Na2CO3和NaOH的结论,你是否同意他的观点并说明理由同意;加入Ba(NO3)2溶液后,若产生白色沉淀且溶液红色不褪去,就证明溶质中含有Na2CO3和NaOH.
【提出问题】(1)白色沉淀A是什么?
(2)无色滤液B中的溶质有哪些?
【查阅资料】腌制皮蛋的原料配方是少量NaCl、CaO和过量Na2CO3的固体混合物.
【理论推理】(1)白色沉淀A是CaCO3,请写出生成该沉淀的化学方程式Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
(2)滤液B中含有Na2CO3、NaOH、NaCl三种溶质.
【实验验证】为证明滤液B中存在的三种溶质,同学们进行了如下实验.
| 步骤 | 实验操作 | 实验现象 | 实验结论 |
| I | 取少量滤液B于试管中,加入过量的Ba(NO3)2溶液,过滤 | 产生白色沉淀 | 滤液B中含有Na2CO3、NaOH、NaCl |
| II | 取少量步骤 I中所得滤液于试管中,加入酚酞溶液 | 溶液由无色变成红色 | |
| III | 另取少量步骤 I中所得滤液于试管中,先加入足量的稀硫酸,再加入硝酸银溶液 | 产生白色沉淀 |
(1)向步骤 I中加入过量Ba(NO3)2溶液的目的是验证并除去溶液中的Na2CO3.
(2)小妮同学认为若将步骤I中的Ba(NO3)2溶液换为BaCl2溶液,进行以上实验,最终也能证明滤液B中存在的三种溶质.你认为是否合理不合理(填“合理”或“不合理”).
(3)小轩同学认为向滤液B中先加入酚酞溶液,后加入过量的Ba(NO3)2溶液,也能得出滤液B的溶质中含有Na2CO3和NaOH的结论,你是否同意他的观点并说明理由同意;加入Ba(NO3)2溶液后,若产生白色沉淀且溶液红色不褪去,就证明溶质中含有Na2CO3和NaOH.
15.在现代生活中,人们越来越注重微量元素的摄取.碘元素对人体健康有着至关重要的作用.下表是某地市场销售的一种“加碘食盐”包装袋上的部分说明.请回答下列问题:
(1)由食用方法和贮藏指南可推测碘酸钾(KIO3)的化学性质之一是:见光、受热易分解;
(2)计算碘酸钾(KIO3)中,钾元素、碘元素、氧元素的质量比是39:127:48;
(3)计算碘酸钾(KIO3)中,碘元素的质量分数为59.3%(计算结果精确到0.01%).
| 配料 | 氯化钠、碘酸钾(KIO3) |
| 含碘量 | (20~30mg)∕1kg |
| 保质期 | 18个月 |
| 食用方法 | 勿长时间炖炒 |
| 贮藏指南 | 避光、避热、密封、防潮 |
(2)计算碘酸钾(KIO3)中,钾元素、碘元素、氧元素的质量比是39:127:48;
(3)计算碘酸钾(KIO3)中,碘元素的质量分数为59.3%(计算结果精确到0.01%).
10.下列关于质量守恒定律的说法正确的是( )
| A. | 化学反应前后,反应物的分子总数一定等于生成物的分子总数 | |
| B. | 化学反应的实质就是分子间的重新组合 | |
| C. | 参加反应的各物质的总质量一定等于反应后生成的各物质的总质量 | |
| D. | 对于有气体参加的化学反应,反应前后的体积一定不变 |