题目内容
16.人们可从铁钛矿(主要成分是FeTiO3)制取金属钛(Ti),其在一定条件下的主要反应有:①FeTiO3+H2=Fe+TiO2+H2O;②Ti02+2C+2Cl2=X+2CO;③TiCl4+2Mg=2MgCl2+Ti.
下列叙述不正确的是( )
| A. | 反应①中的H2被氧化 | B. | 反应②Cl2中的氯元素为一1价 | ||
| C. | 反应②中x为TiCl4 | D. | 反应③说明Mg的金属活动性比Ti强 |
分析 A.根据氢气的性质来分析;
B.根据单质中元素的化合价为零来分析;
C.根据质量守恒定律来分析;
D.根据金属的活动性顺序来分析.
解答 解:A.反应①中的氢气将FeTiO3还原为Fe,氢气被氧化,故正确;
B.氯气是单质,所以Cl2中的氯元素为0价,故错误;
C.反应前后,原子的种类与数目不标明,在TiO2+2C+2Cl2=X+2CO中,反应前有:1个钛原子、2个氧原子、2个碳原子和4个氯原子;反应后有:2个碳原子、2个氧原子,所以每个X分子中含有1个钛原子和4个氯原子,即化学式为TiCl4;故正确;
D.活泼性的金属能将活泼性差的元素从其盐溶液中置换出来,由TiCl4+2Mg=2MgCl2+Ti可知,Mg的金属活动性比Ti强,故正确.
故选B.
点评 本题考查了物质的性质、元素的化合价、质量守恒定律及其应用、金属的活动性,难度不大.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
4.金属钛(Ti)抗腐蚀性能好,露置于空气中数年,仍光亮如初,以金红石(主要成分是TiO2)为原料生产金属钛的步骤主要有:①在高温下,向金红石与焦炭的混合物中通入氯气(Cl2),得到TiCl4和一种可燃性气体;②在稀有气体环境和加热条件下,用Mg和TiCl4反应得到Ti和MgCl2,下列说法正确的是( )
| A. | ①中的反应TiO2+C+2Cl2$\frac{\underline{\;高温\;}}{\;}$TiCl4+CO2 | |
| B. | ②中的稀有气体的作用是隔绝空气 | |
| C. | ②中发生的反应为置换反应 | |
| D. | 金属钛在常温下易与O2反应 |
1.保护环境,刻不容缓.下列做法有利于保护环境的是( )
| A. | 用清洁能源代替化石燃料 | B. | 露天焚烧伪劣产品 | ||
| C. | 倡导家家买汽车,尽快淘汰自行车 | D. | 集中掩埋处理生活垃圾 |
8.下列实验操作中,正确的是( )
| A. | 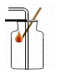 CO2验满 | B. |  检查气密性 | C. |  滴加液体 | D. |  点燃酒精灯 |
6.在化学晚会上表演如下魔术:用毛笔蘸取一种无色液体在一张白纸上书写了“化学魔术”四字,然后再喷上一种无色液体,白纸上立即出现了红色的“化学魔术”四字,然后再喷上一种无色液体,白纸上立即出现了红色的“化学魔术”四字.该生先后所用的无色液体可能是( )
| A. | 石蕊溶液、稀硫酸 | B. | 酚酞溶液、“雪碧”饮料 | ||
| C. | NaOH溶液、酚酞溶液 | D. | CuSO4溶液、NaOH溶液 |