题目内容
18. 向盛有100g稀硫酸的烧杯中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入NaOH溶液,所得沉淀质量与加入NaOH溶液的质量关系如图所示.
向盛有100g稀硫酸的烧杯中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入NaOH溶液,所得沉淀质量与加入NaOH溶液的质量关系如图所示.(1)加入80g氢氧化钠溶液,烧杯内溶液中的阴离子是硫酸根离子.
(2)计算氢氧化钠溶液中溶质的质量分数.
分析 镁和稀硫酸反应生成硫酸镁和氢气,氢氧化钠和稀硫酸反应生成硫酸钠和水,氢氧化钠和硫酸镁反应生成白色沉淀氢氧化镁和硫酸钠,根据反应的化学方程式和提供的数据可以计算氢氧化钠溶液中溶质的质量分数.
解答 解:(1)加入80g氢氧化钠溶液时,氢氧化钠和稀硫酸反应生成硫酸钠和水,烧杯内溶液中含有的溶质是硫酸钠和硫酸镁,其中的阴离子是硫酸根离子.
故填:硫酸根离子.
(2)设40g氢氧化钠溶液中氢氧化钠质量为x,
2NaOH+MgSO4═Na2SO4+Mg(OH)2↓,
80 58
x 8.7g
$\frac{80}{x}$=$\frac{58}{8.7g}$,
x=12g,
氢氧化钠溶液中溶质的质量分数为:$\frac{12g}{40g}$×100%=30%,
答:氢氧化钠溶液中溶质的质量分数为30%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
10.有X、Y、Z三种金属,可以发生如下反应:
①X+Z(NO3)2=X(NO3)2+Z ②X+YSO4=XSO4+Y ③Z+YSO4=ZSO4+Y
则这三种金属的活动性由强到弱的顺序是( )
①X+Z(NO3)2=X(NO3)2+Z ②X+YSO4=XSO4+Y ③Z+YSO4=ZSO4+Y
则这三种金属的活动性由强到弱的顺序是( )
| A. | X>Z>Y | B. | Z>Y>X | C. | X>Y>Z | D. | Y>Z>X |
18.某化学兴趣小组的同学用一瓶已经过滤的澄淸透明海水为原料,在实验室中模拟“侯氏制碱法”的制碱过程.
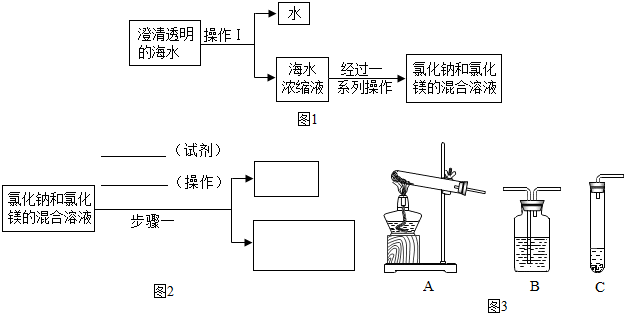
(1)从海水中分别得到纯净的水和氯化钠固体(其流程如图1),其中,操作I的名称是蒸发;完成这一操作实验,除了胶塞、导管、收集容器和铁架台外,还需要的主要仪器之一是酒精灯(只要求写出其中一种仪器名称).
(2)请完成实验设计思路图(图2),目的是从氯化钠和氯化镁的混合溶液中除去氯化镁,得到较纯净的氯化钠固体.(要求:①在图2箭头上/下方写出相应的试剂和实验操作;②在方框内写出相应的化学式;③可根据需要,仿照步骤1的写法将此图延伸.)
(3)已知有四种物质在30℃时的溶解度如表所示:
请根据溶解度表所提供的信息,用这四种物质分别作为反应物和生成物,写出一道复分解反应的化 学方程式.
NaCl+NH4HCO3=NaHCO3↓+NH4Cl.
“侯氏制碱法”既是向饱和氯化钠溶液中先后通入氨气〔NH4)和二氧化碳(CO2),使溶液中发生上述反应.
同学们利用图3装置B完成这一反应后,取其中的一种生成物,再利用装置A进行加热分解就得到了最后的产品Na2CO3(填化学式).

(1)从海水中分别得到纯净的水和氯化钠固体(其流程如图1),其中,操作I的名称是蒸发;完成这一操作实验,除了胶塞、导管、收集容器和铁架台外,还需要的主要仪器之一是酒精灯(只要求写出其中一种仪器名称).
(2)请完成实验设计思路图(图2),目的是从氯化钠和氯化镁的混合溶液中除去氯化镁,得到较纯净的氯化钠固体.(要求:①在图2箭头上/下方写出相应的试剂和实验操作;②在方框内写出相应的化学式;③可根据需要,仿照步骤1的写法将此图延伸.)
(3)已知有四种物质在30℃时的溶解度如表所示:
| 温度 | NaCl | NH4HCO3 | NaHCO3 | NH4Cl |
| 30℃ | 36.3g | 27.0g | 11.1g | 41.1g |
NaCl+NH4HCO3=NaHCO3↓+NH4Cl.
“侯氏制碱法”既是向饱和氯化钠溶液中先后通入氨气〔NH4)和二氧化碳(CO2),使溶液中发生上述反应.
同学们利用图3装置B完成这一反应后,取其中的一种生成物,再利用装置A进行加热分解就得到了最后的产品Na2CO3(填化学式).
 请看图回答下列问题:
请看图回答下列问题:
 .
. 构建物质之间相互反应的知识网络是提高学习效率的有效方法,如图中的甲、乙、丙、丁是初中化学常见的四种不同类别的物质,相邻两种物质可发生化学反应,生成A、B、C、D四种物质(部分生成物已略去).其中乙是应用最广泛的金属,丙是一种蓝色溶液,B为硫酸盐,C为单质,请回答下列问题:
构建物质之间相互反应的知识网络是提高学习效率的有效方法,如图中的甲、乙、丙、丁是初中化学常见的四种不同类别的物质,相邻两种物质可发生化学反应,生成A、B、C、D四种物质(部分生成物已略去).其中乙是应用最广泛的金属,丙是一种蓝色溶液,B为硫酸盐,C为单质,请回答下列问题: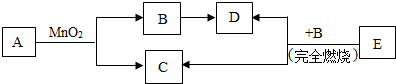 已知A、B、C、D、E五种物质之间存在以下的转化关系,其中A、C两种物质的组成元素相同,且常温下为液体.
已知A、B、C、D、E五种物质之间存在以下的转化关系,其中A、C两种物质的组成元素相同,且常温下为液体.