题目内容
某学校的学习小组对当地的石灰石矿区进行调查,测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品16g,把80g稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的二氧化硅等杂质不溶于水,不与稀盐酸反应)。
|
序号 |
加入稀盐酸的质量/g |
剩余固体的质量/g |
|
第1次 |
20 |
11 |
|
第2次 |
20 |
6 |
|
第3次 |
20 |
2.8 |
|
第4次 |
20 |
n |
请计算:(1)上表中n的数值为________;
(2)求样品中碳酸钙的质量分数;
(3)求盐酸中溶质的质量分数。
【答案】
(1)2.8(2)82.5%(3)14.6%
【解析】(1)根据图表数据可知,第1、2次反应后固体物质减少的质量都为5g,而第3次反应后固体物质减少的质量为3.2g,说明此时碳酸钙已反应完,不再产生气体,故表中n的数值为2.8.
(2)样品中碳酸钙的质量分数=(16g-2.8g) /8g ×100%=82.5%.
答:样品中碳酸钙的质量分数为82.5%.
(3)由试题分析20g稀盐酸恰好能与石灰石中的5g碳酸钙完全反应
解:设第一次参与反应的HCl质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73
5g x
∴100 /5g =73 /x ,
解之得:x=3.65g,
盐酸中溶质的质量分数为:3.65g /10g ×100%=18.25%.
答:盐酸中溶质的质量分数为18.25%.

练习册系列答案
相关题目
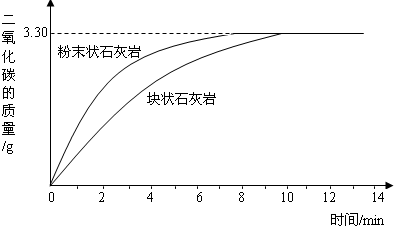
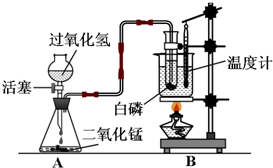 某学校化学学习小组设计出右图所示装置,并进行白磷燃烧实验.
某学校化学学习小组设计出右图所示装置,并进行白磷燃烧实验.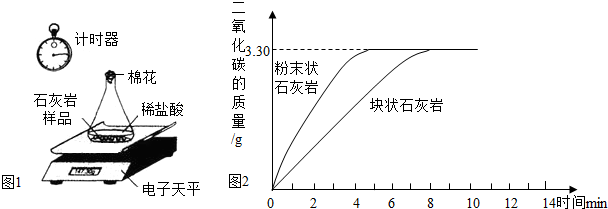
 某学校化学学习小组设计出右图所示装置,并进行白磷燃烧实验.
某学校化学学习小组设计出右图所示装置,并进行白磷燃烧实验.