题目内容
 为测定锌铜合金中锌的含量,取该合金放入如图 14 盛有稀硫酸的锥形瓶中,发生反应: Zn+H2SO4=ZnSO4+H2↑ 。多次实验后,取平均值所得数据如下表:
为测定锌铜合金中锌的含量,取该合金放入如图 14 盛有稀硫酸的锥形瓶中,发生反应: Zn+H2SO4=ZnSO4+H2↑ 。多次实验后,取平均值所得数据如下表:
| 反应前 | 充分反应后装置及反应剩余物质质量 | |
| 装置和足量的稀硫酸质量 | 锌铜合金质量 | |
| 342.10g | 16.00g | 357.70g |
若不考虑干燥剂吸收空气中的水蒸气,计算:
(1)根据质量守恒定律求生成氢气的质量。
(2)该合金中锌的质量分数。
(1)解:依题意可得
氢气的质量=342.10g+16.00g-357.70g
=0.4g
答:氢气的质量为0.4g
(2)解:设该合金中锌的质量分数为x。
Zn + H2SO4=ZnSO4+H2↑
65 2
16.00g×x 0.4g
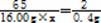
x=81.25%
答:该合金中锌的质量分数为81.25%

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某化学兴趣小组同学为测定锌铜合金中锌的质量分数,称取8.0克合金样品,将60.0克稀硫酸分6次加入样品中,充分反应后过滤、洗涤、干燥、称量.得到实验数据如下.
| 稀H2SO4用量 | 剩余固体质量 |
| 第一次加入10.0克 | m |
| 第二次加入10.0克 | 5.4克 |
| 第三次加入10.0克 | 4.1克 |
| 第四次加入10.0克 | 2.8克 |
| 第五次加入10.0克 | 1.6克 |
| 第六次加入10.0克 | 1.6克 |
(2)该锌铜合金锌的质量分数为________.
(3)计算所用稀H2SO4中溶质的质量分数.(请写出计算过程,结果精确到0.1%)
某化学兴趣小组同学为测定锌铜合金中锌的质量分数,称取8.0克合金样品,将60.0克稀硫酸分6次加入样品中,充分反应后过滤、洗涤、干燥、称量.得到实验数据如下.
| 稀H2SO4用量 | 剩余固体质量 |
| 第一次加入10.0克 | m |
| 第二次加入10.0克 | 5.4克 |
| 第三次加入10.0克 | 4.1克 |
| 第四次加入10.0克 | 2.8克 |
| 第五次加入10.0克 | 1.6克 |
| 第六次加入10.0克 | 1.6克 |
(1)表格中,m= 克.
(2)该锌铜合金锌的质量分数为 .
(3)计算所用稀H2SO4中溶质的质量分数.(请写出计算过程,结果精确到0.1%)
某化学兴趣小组同学为测定锌铜合金中锌的质量分数,称取8.0克合金样品,将60.0克稀硫酸分6次加入样品中,充分反应后过滤、洗涤、干燥、称量.得到实验数据如下.
(1)表格中,m=______克.
(2)该锌铜合金锌的质量分数为______.
(3)计算所用稀H2SO4中溶质的质量分数.(请写出计算过程,结果精确到0.1%)
| 稀H2SO4用量 | 剩余固体质量 |
| 第一次加入10.0克 | m |
| 第二次加入10.0克 | 5.4克 |
| 第三次加入10.0克 | 4.1克 |
| 第四次加入10.0克 | 2.8克 |
| 第五次加入10.0克 | 1.6克 |
| 第六次加入10.0克 | 1.6克 |
(2)该锌铜合金锌的质量分数为______.
(3)计算所用稀H2SO4中溶质的质量分数.(请写出计算过程,结果精确到0.1%)
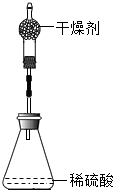 (2013?厦门)为测定锌铜合金中锌的含量,取该合金放入如图 盛有稀硫酸的锥形瓶中,发生反应:Zn+H2SO4=ZnSO4+H2↑.多次实验后,取平均值所得数据如下表:
(2013?厦门)为测定锌铜合金中锌的含量,取该合金放入如图 盛有稀硫酸的锥形瓶中,发生反应:Zn+H2SO4=ZnSO4+H2↑.多次实验后,取平均值所得数据如下表: