23.(10分)(1)将6.62 g铁矿石样品投入适量的盐酸中(充分反应),过滤,然后在滤液中加过量的NaOH溶液,充分反应后,过滤、洗涤、灼烧得4.80 g Fe2O3。现以该铁矿石为原料炼铁,若生产过程中铁元素损失4%,计算每生产1.00 t生铁(含铁96%),至少需要这种铁矿石________吨。(保留两位小数)
(2)取某钢样粉末28.12 g(假设只含Fe和C),在氧气流中充分反应,得到CO2气体224 mL(标准状况)。
① 计算此钢样粉末中铁和碳的物质的量之比______________。
② 再取三份不同质量的钢样粉末分别加到100 mL相同浓度的H2SO4溶液中,充分反应后,测得的实验数据如下表所示:
|
实验序号 |
Ⅰ |
Ⅱ |
Ⅲ |
|
加入钢样粉末的质量/g |
2.812 |
5.624 |
8.436 |
|
生成气体的体积/L(标准状况) |
1.120 |
2.240 |
2.800 |
计算硫酸溶液的物质的量浓度为_______________________。
③ 若在实验Ⅱ中继续加入m g钢样粉末,反应结束后剩余的固体质量可能为__________________________________________________________________________ 。(用含m的代数式表示)
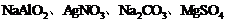 ;②Na2SO4、MgCl2、Al2(SO4)3、NH4Cl均能用一种试剂区别,区别①的试剂是 ;区别②的试剂是 。
;②Na2SO4、MgCl2、Al2(SO4)3、NH4Cl均能用一种试剂区别,区别①的试剂是 ;区别②的试剂是 。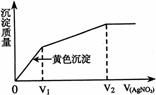 A.140 mL B.120 mL C.100 mL D.80 mL
A.140 mL B.120 mL C.100 mL D.80 mL