网址:http://m.1010jiajiao.com/timu_id_93011[举报]
一、选择题(本大题共10题,每小题2分,共20分)每小题给出的四个选项中,只有一个最符合题意,请将其序号涂在答题卡上。
题号
1
2
3
4
5
6
7
8
9
10
答案
A
B
D
A
D
D
C
D
B
C
二、选择题(本大题共5题,每小题2分,共10分)每小题给出的四个选项中,有1~2个符合题意。只有一个选项符合题意的多选不给分;有2个选项符合题意的只选一个且符合题意给1分,若选2个有一个不符合题意则不给分。
题号
11
12
13
14
15
答案
D
C
AB
B
BC
三、(本大题共5题 共15分)
16.(5分)(每空1分) (1)① (2)③ (3)⑤ (4)② (5)④
17.(4分)(每空1分) 降低 吸水性 硝酸银溶液 稀硝酸
18.(1分)(每空1分) 碱
19.(2分)(每空1分) (1)碱性氧化物 碱 (2)酸性氧化物 酸 盐
20.(3分)(每空1分) Fe Cu Ag ;Fe2+ Zn2+ ;Ag+ Cu2+
四、(本大题共4题 共18分)
21.(8分)每个化学方程式1分,每空1分。化学方程式略。中和反应是(3)
22.(3分)每个化学方程式1分,化学方程式略。
23.(5分)(每空1分)(1)CuSO4 (2)Na2CO3 (3)BaSO4 (4)NaCl H2SO4和NaNO3 或H2SO4和Na2SO4
24.(2分)(每个正确答案1分)②③
五、(本大题共2题 共12分)
25.(6分)(每空1分) (1)化学方程式略 (2)C (3)铜 (4)CuSO4和H2SO4 (5)A
26.(6分)(每空1分) (1)二 (2)稀硝酸 确定溶液中是否存在碳酸根离子 硝酸钡 确定溶液中是否含有硫酸根离子 硝酸银
六、(本大题共3题 共15分)
27.(4分)(每空1分) 稀盐酸 稀盐酸 碳酸根离子 硫酸钡
28.(6分)(每空1分)
A Fe2O3 D Fe(OH)3 E
CO F CO
29.(5分)(每空1分)
A BaSO4 B
Ba(OH)
七、(本大题共2题 共10分)
30.(3分)解:设反应的硫酸铜质量为x
CuSO4+2NaOH====Cu(OH)2↓+Na2SO4
160 98
X

 X
X
X=
硫酸铜溶液的质量分数为
答:略。
31.(7分)
(1) 同意。 ………………1分
(2) Cu―Ag ………………1分
解:设合金中银的质量为X
Cu+2AgNO3====Cu(NO3)2+2Ag
64 216
64 216


X=
铜和银的质量比为(9.6-6.4)g :
(3)解:设参与反应的硝酸银的质量为X
Cu+2AgNO3====Cu(NO3)2+2Ag
64 340
64 340


Y=
硝酸银溶液的溶质质量分数为
答:略。
本资料由《七彩教育网》www.7caiedu.cn 提供!
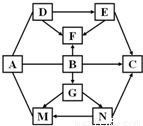
 如图,方框中的物质都是九年级化学中所学的物质,其中属于盐的是B、C、M、N,属于氧化物的是F、G,胃液中含有适量A可以帮助消化,C是家庭中重要的调味品之一,D可以由生石灰加水制得,且D和N可以用来制取烧碱.图中“→”表示物质之间在转化的关系,“-”表示两端物质之间能发生化学反应.(部分反应物生成物已略去.)
如图,方框中的物质都是九年级化学中所学的物质,其中属于盐的是B、C、M、N,属于氧化物的是F、G,胃液中含有适量A可以帮助消化,C是家庭中重要的调味品之一,D可以由生石灰加水制得,且D和N可以用来制取烧碱.图中“→”表示物质之间在转化的关系,“-”表示两端物质之间能发生化学反应.(部分反应物生成物已略去.)(1)物质E的化学式是
(2)G→M的反应在实验室的用途
(3)写出D→E的化学方程式
(4)F和G在一定条件下可以反应得到氧气,其化学方程式是
| ||
| 叶绿体 |
| ||
| 叶绿体 |
如图,方框中的物质都是九年级化学中所学的物质,其中属于盐的是B、C、M、N,属于氧化物的是F、G,胃液中含有适量A可以帮助消化,C是家庭中重要的调味品之一,D可以由生石灰加水制得,且D和N可以用来制取烧碱。图中“→”表示物质之间在转化的关系,“—”表示两端物质之间能发生化学反应。(部分反应物生成物已略去。)

(1)物质E的化学式是 ,物质B的俗名是
。
(2)G→M的反应在实验室的用途 。
(3)写出D→E的化学方程式 。
(4)F和G在一定条件下可以反应得到氧气,其化学方程式是 。
查看习题详情和答案>>(1)物质E的化学式是______,物质B的俗名是______.
(2)G→M的反应在实验室的用途______.
(3)写出D→E的化学方程式______.
(4)F和G在一定条件下可以反应得到氧气,其化学方程式是______叶绿体C6H12O6+6O2
 查看习题详情和答案>>
查看习题详情和答案>>
(2)无水碳酸钠的工业制法主要有氨碱法和联合制碱法两种.氨碱法即以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气(极易溶于水)为原料来制取纯碱.工业上是用N2和H2在高温、高压和催化剂条件下合成氨的.实验室一般用氯化铵和消石灰共热来制备少量的氨气,该反应的化学方程式为
(3)某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验,取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 烧杯及所盛物质的总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
①第一次加入稀盐酸充分反应后,生成二氧化碳的质量是
②该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%) 查看习题详情和答案>>
(1)碳酸钠是玻璃、造纸、肥皂、洗涤剂、纺织、制革等工业的重要原料,它属于
______(填“酸”、“碱”或“盐”),它的俗名叫纯碱的原因是______.
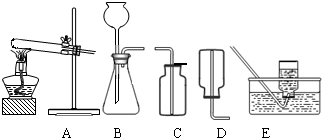
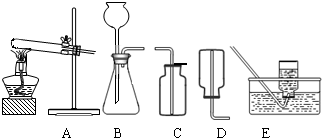
(2)无水碳酸钠的工业制法主要有氨碱法和联合制碱法两种.氨碱法即以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气(极易溶于水)为原料来制取纯碱.工业上是用N2和H2在高温、高压和催化剂条件下合成氨的.实验室一般用氯化铵和消石灰共热来制备少量的氨气,该反应的化学方程式为______,制取和收集氨气可用下图中的______和______装置.
(3)某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验,取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 烧杯及所盛物质的总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
①第一次加入稀盐酸充分反应后,生成二氧化碳的质量是______g.
②该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%) 查看习题详情和答案>>
