题目内容
(1)碳酸钠是玻璃、造纸、肥皂、洗涤剂、纺织、制革等工业的重要原料,它属于(2)无水碳酸钠的工业制法主要有氨碱法和联合制碱法两种.氨碱法即以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气(极易溶于水)为原料来制取纯碱.工业上是用N2和H2在高温、高压和催化剂条件下合成氨的.实验室一般用氯化铵和消石灰共热来制备少量的氨气,该反应的化学方程式为
(3)某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验,取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 烧杯及所盛物质的总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
①第一次加入稀盐酸充分反应后,生成二氧化碳的质量是
②该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
分析:(1)欲知碳酸钠属于哪一类,须熟知酸碱盐的概念,欲知它的俗名叫纯碱的原因,须知它的水溶液的性质.
(2)必须知道消石灰的化学式,才能正确书写反应方程式.
(3)①第一次加入稀盐酸充分反应后,生成的二氧化碳逸出,因此生成的二氧化碳质量应该是参加反应的物质质量之和,减去反应后物质质量之和.
②因其产品包装袋上注明:碳酸钠≥96%,故该产品中碳酸钠的质量分数只要≥96%,就是合格.所以应先求出该产品中碳酸钠的质量分数,再通过比较,就可知是否合格.
(2)必须知道消石灰的化学式,才能正确书写反应方程式.
(3)①第一次加入稀盐酸充分反应后,生成的二氧化碳逸出,因此生成的二氧化碳质量应该是参加反应的物质质量之和,减去反应后物质质量之和.
②因其产品包装袋上注明:碳酸钠≥96%,故该产品中碳酸钠的质量分数只要≥96%,就是合格.所以应先求出该产品中碳酸钠的质量分数,再通过比较,就可知是否合格.
解答:解:(1)酸指电离时产生的阳离子全部都是氢离子的化合物;碱指电离时产生的阴离子全部都是氢氧根离子的化合物;盐指电离时生成金属阳离子(或NH4)和酸根离子的化合物.故碳酸钠(Na2CO3)属于盐,它的俗名叫纯碱是因为碳酸钠的水溶液显碱性.
(2)①消石灰的化学式为Ca(OH)2,因此氯化铵和消石灰反应的化学方程式为Ca(OH)2+2NH4Cl=CaCl2+2NH3↑+2H2O;
②由题意可知,实验室一般用氯化铵和消石灰共热来制备少量的氨气,所以要用A装置来进行加热,又因为NH3的密度比空气小,且易溶于水,故用D向下排空气法收集,故答案为A、D;
(3)①第一次加入稀盐酸充分反应后,生成的二氧化碳逸出,因此生成的二氧化碳质量应该是参加反应的物质质量之和,减去反应后物质质量之和.第一次加入稀盐酸是100g÷4=25g,烧杯及所盛纯碱样品的总质量为158.0g,因此烧杯及参加反应物质的质量之和为158g+25g=183g,充分反应后烧杯及所盛物质的总质量为181.2g,故生成的二氧化碳的质量为183g-181.2g=1.8g.
②共生成二氧化碳的质量为158g+100g-253.6g=4.4g
设样品中Na2CO3的质量为x.
Na2CO3+2HCl=2NaCl+CO2↑+H2O
106 44
x 4.4g
=
,解得:x=10.6g
样品中Na2CO3的质量分数=
×100%=96.4%>96%,
所以产品中Na2CO3的质量分数合格.
答:该产品中碳酸钠的质量分数合格.
(2)①消石灰的化学式为Ca(OH)2,因此氯化铵和消石灰反应的化学方程式为Ca(OH)2+2NH4Cl=CaCl2+2NH3↑+2H2O;
②由题意可知,实验室一般用氯化铵和消石灰共热来制备少量的氨气,所以要用A装置来进行加热,又因为NH3的密度比空气小,且易溶于水,故用D向下排空气法收集,故答案为A、D;
(3)①第一次加入稀盐酸充分反应后,生成的二氧化碳逸出,因此生成的二氧化碳质量应该是参加反应的物质质量之和,减去反应后物质质量之和.第一次加入稀盐酸是100g÷4=25g,烧杯及所盛纯碱样品的总质量为158.0g,因此烧杯及参加反应物质的质量之和为158g+25g=183g,充分反应后烧杯及所盛物质的总质量为181.2g,故生成的二氧化碳的质量为183g-181.2g=1.8g.
②共生成二氧化碳的质量为158g+100g-253.6g=4.4g
设样品中Na2CO3的质量为x.
Na2CO3+2HCl=2NaCl+CO2↑+H2O
106 44
x 4.4g
| 106 |
| x |
| 44 |
| 4.4g |
样品中Na2CO3的质量分数=
| 10.6g |
| 11.0g |
所以产品中Na2CO3的质量分数合格.
答:该产品中碳酸钠的质量分数合格.
点评:本题覆盖的知识面较广,它要求学生要熟记酸碱盐的概念,对常见物质的化学式能正确书写,并且能理解充分反应的概念,还要熟练掌握质量分数的计算方法,才能正确答题.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
(1)碳酸钠是玻璃、造纸、肥皂、洗涤剂、纺织、制革等工业的重要原料,它属于
______(填“酸”、“碱”或“盐”),它的俗名叫纯碱的原因是______.
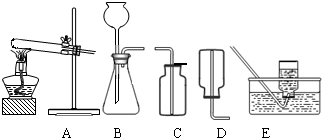
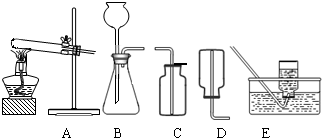
(2)无水碳酸钠的工业制法主要有氨碱法和联合制碱法两种.氨碱法即以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气(极易溶于水)为原料来制取纯碱.工业上是用N2和H2在高温、高压和催化剂条件下合成氨的.实验室一般用氯化铵和消石灰共热来制备少量的氨气,该反应的化学方程式为______,制取和收集氨气可用下图中的______和______装置.
(3)某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验,取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 烧杯及所盛物质的总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
①第一次加入稀盐酸充分反应后,生成二氧化碳的质量是______g.
②该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
(1)碳酸钠是玻璃、造纸、肥皂、洗涤剂、纺织、制革等工业的重要原料,它属于
______(填“酸”、“碱”或“盐”),它的俗名叫纯碱的原因是______.
(2)无水碳酸钠的工业制法主要有氨碱法和联合制碱法两种.氨碱法即以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气(极易溶于水)为原料来制取纯碱.工业上是用N2和H2在高温、高压和催化剂条件下合成氨的.实验室一般用氯化铵和消石灰共热来制备少量的氨气,该反应的化学方程式为______,制取和收集氨气可用下图中的______和______装置.
(3)某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验,取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
请你据此分析计算:
①第一次加入稀盐酸充分反应后,生成二氧化碳的质量是______g.
②该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
______(填“酸”、“碱”或“盐”),它的俗名叫纯碱的原因是______.
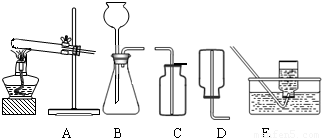
(2)无水碳酸钠的工业制法主要有氨碱法和联合制碱法两种.氨碱法即以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气(极易溶于水)为原料来制取纯碱.工业上是用N2和H2在高温、高压和催化剂条件下合成氨的.实验室一般用氯化铵和消石灰共热来制备少量的氨气,该反应的化学方程式为______,制取和收集氨气可用下图中的______和______装置.

(3)某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验,取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 烧杯及所盛物质的总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
①第一次加入稀盐酸充分反应后,生成二氧化碳的质量是______g.
②该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
(1)碳酸钠是玻璃、造纸、肥皂、洗涤剂、纺织、制革等工业的重要原料,它属于
______(填“酸”、“碱”或“盐”),它的俗名叫纯碱的原因是______.
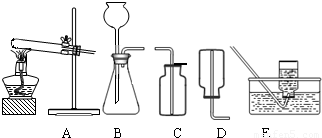
(2)无水碳酸钠的工业制法主要有氨碱法和联合制碱法两种.氨碱法即以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气(极易溶于水)为原料来制取纯碱.工业上是用N2和H2在高温、高压和催化剂条件下合成氨的.实验室一般用氯化铵和消石灰共热来制备少量的氨气,该反应的化学方程式为______,制取和收集氨气可用下图中的______和______装置.
(3)某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验,取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
请你据此分析计算:
①第一次加入稀盐酸充分反应后,生成二氧化碳的质量是______g.
②该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
______(填“酸”、“碱”或“盐”),它的俗名叫纯碱的原因是______.
(2)无水碳酸钠的工业制法主要有氨碱法和联合制碱法两种.氨碱法即以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气(极易溶于水)为原料来制取纯碱.工业上是用N2和H2在高温、高压和催化剂条件下合成氨的.实验室一般用氯化铵和消石灰共热来制备少量的氨气,该反应的化学方程式为______,制取和收集氨气可用下图中的______和______装置.

(3)某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验,取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 烧杯及所盛物质的总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
①第一次加入稀盐酸充分反应后,生成二氧化碳的质量是______g.
②该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
(1)碳酸钠是玻璃、造纸、肥皂、洗涤剂、纺织、制革等工业的重要原料,它属于
______(填“酸”、“碱”或“盐”),它的俗名叫纯碱的原因是______.
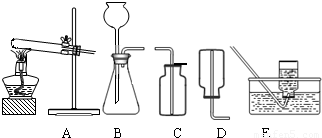
(2)无水碳酸钠的工业制法主要有氨碱法和联合制碱法两种.氨碱法即以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气(极易溶于水)为原料来制取纯碱.工业上是用N2和H2在高温、高压和催化剂条件下合成氨的.实验室一般用氯化铵和消石灰共热来制备少量的氨气,该反应的化学方程式为______,制取和收集氨气可用下图中的______和______装置.
(3)某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验,取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
请你据此分析计算:
①第一次加入稀盐酸充分反应后,生成二氧化碳的质量是______g.
②该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
______(填“酸”、“碱”或“盐”),它的俗名叫纯碱的原因是______.
(2)无水碳酸钠的工业制法主要有氨碱法和联合制碱法两种.氨碱法即以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气(极易溶于水)为原料来制取纯碱.工业上是用N2和H2在高温、高压和催化剂条件下合成氨的.实验室一般用氯化铵和消石灰共热来制备少量的氨气,该反应的化学方程式为______,制取和收集氨气可用下图中的______和______装置.

(3)某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验,取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 烧杯及所盛物质的总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
①第一次加入稀盐酸充分反应后,生成二氧化碳的质量是______g.
②该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)