摘要:A中含有碳氧双键.与A相关的反应如图所示:
网址:http://m.1010jiajiao.com/timu_id_923752[举报]
硫酸钠是制造纸浆、染料稀释剂、医药品等的重要原料.某硫酸钠粗品中含有少量CaCl2和
MgCl2,实验室进行提纯的流程如图所示:回答下列问题:
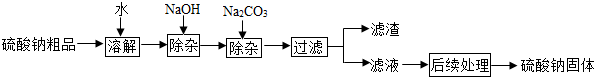
①溶解过程需要的玻璃仪器有烧杯和 .
②用NaOH除杂时,反应的化学方程式为 .
③NaOH和Na2CO3如果添加过量了,可加入适量 溶液除去.
④“后续处理”的主要操作是蒸发,为了获得纯净的硫酸钠,应蒸发至 (填序号).
A.完全蒸干时停止加热 B.有较多固体析出时停止加热,利用余热蒸干
C.有大量固体析出时停止加热,过滤弃去剩余的少量溶液. 查看习题详情和答案>>
MgCl2,实验室进行提纯的流程如图所示:回答下列问题:

①溶解过程需要的玻璃仪器有烧杯和
②用NaOH除杂时,反应的化学方程式为
③NaOH和Na2CO3如果添加过量了,可加入适量
④“后续处理”的主要操作是蒸发,为了获得纯净的硫酸钠,应蒸发至
A.完全蒸干时停止加热 B.有较多固体析出时停止加热,利用余热蒸干
C.有大量固体析出时停止加热,过滤弃去剩余的少量溶液. 查看习题详情和答案>>
(2012?湘潭)在研究酸和碱的化学性质时,某小组同学想证明:稀H2SO4与NaOH溶液混合后,虽然仍为无色溶液,但确实发生了化学反应.请与他们一起完成实验方案设计、实施和评价.
(1)方案一:测定稀H2SO4与NaOH溶液混合前后的pH(常温下)他们先测定出某NaOH溶液的pH
结论:稀H2SO4与NaOH溶液发生了化学反应,并且
(2)方案二:利用酸碱指示剂
①探究稀H2SO4与NaOH溶液的反应
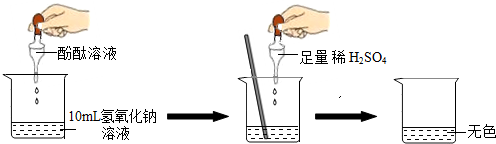
如图所示进行实验.当滴入几滴酚酞溶液后,溶液由无色变为
②探究上述稀H2SO4与NaOH溶液反应后烧杯中的硫酸是否过量
根据上述反应过程中溶液变成无色,不能确定稀H2SO4是否过量,同学们又分别选取BaCl2溶液与、紫色石蕊溶液、Na2CO3粉末设计实验方案,请你判断并分析:
方案三中反应的化学方程式为
查看习题详情和答案>>
(1)方案一:测定稀H2SO4与NaOH溶液混合前后的pH(常温下)他们先测定出某NaOH溶液的pH
大于
大于
7(填“大于”、“等于”或“小于”),然后将一定量的稀H2SO4加入该NaOH溶液中,混合均匀后再测定其pH,发现其pH小于7.结论:稀H2SO4与NaOH溶液发生了化学反应,并且
稀硫酸
稀硫酸
过量.(2)方案二:利用酸碱指示剂
①探究稀H2SO4与NaOH溶液的反应

如图所示进行实验.当滴入几滴酚酞溶液后,溶液由无色变为
红
红
色.根据上述过程中的颜色变化,确定稀H2SO4与NaOH溶液发生了反应,该反应的化学方程式为2NaOH+H2SO4═Na2SO4+2H2O
2NaOH+H2SO4═Na2SO4+2H2O
.②探究上述稀H2SO4与NaOH溶液反应后烧杯中的硫酸是否过量
根据上述反应过程中溶液变成无色,不能确定稀H2SO4是否过量,同学们又分别选取BaCl2溶液与、紫色石蕊溶液、Na2CO3粉末设计实验方案,请你判断并分析:
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 方案一 | 取样,滴入适量的BaCl2溶液 | 出现白色沉淀 | 稀H2SO4过量 |
| 方案二 | 取样,滴入几滴紫色石蕊溶液 | 溶液变红 | 稀H2SO4过量 |
| 方案三 | 取样,加入Na2CO3粉末 | 有气体产生 | 稀H2SO4过量 |
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
.上述设计的实验方案中,不正确的是方案一
方案一
(填“方案一”、“方案二”或“方案三”).错误的原因是即使硫酸不过量,先前生成的硫酸钠也能和氯化钡反应生成白色沉淀
即使硫酸不过量,先前生成的硫酸钠也能和氯化钡反应生成白色沉淀
.请你再设计一个实验方案确定稀H2SO4是否过量,你选用加入氧化铜,观察溶液的颜色变化,若显示为蓝色,则硫酸过量
加入氧化铜,观察溶液的颜色变化,若显示为蓝色,则硫酸过量
(填药品或者方法).
在研究酸和碱的化学性质时,某小组同学想证明:稀H2SO4与NaOH溶液混合后,虽然仍为无色溶液,但确实发生了化学反应.请与他们一起完成实验方案设计、实施和评价.
(1)方案一:测定稀H2SO4与NaOH溶液混合前后的pH(常温下)他们先测定出某NaOH溶液的pH 7(填“大于”、“等于”或“小于”),然后将一定量的稀H2SO4加入该NaOH溶液中,混合均匀后再测定其pH,发现其pH小于7.
结论:稀H2SO4与NaOH溶液发生了化学反应,并且 过量.
(2)方案二:利用酸碱指示剂
①探究稀H2SO4与NaOH溶液的反应
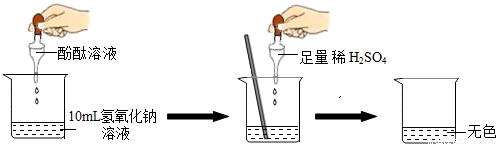
如图所示进行实验.当滴入几滴酚酞溶液后,溶液由无色变为 色.根据上述过程中的颜色变化,确定稀H2SO4与NaOH溶液发生了反应,该反应的化学方程式为 .
②探究上述稀H2SO4与NaOH溶液反应后烧杯中的硫酸是否过量
根据上述反应过程中溶液变成无色,不能确定稀H2SO4是否过量,同学们又分别选取BaCl2溶液与、紫色石蕊溶液、Na2CO3粉末设计实验方案,请你判断并分析:
方案三中反应的化学方程式为 .上述设计的实验方案中,不正确的是 (填“方案一”、“方案二”或“方案三”).错误的原因是 .请你再设计一个实验方案确定稀H2SO4是否过量,你选用 (填药品或者方法).
查看习题详情和答案>>
(1)方案一:测定稀H2SO4与NaOH溶液混合前后的pH(常温下)他们先测定出某NaOH溶液的pH 7(填“大于”、“等于”或“小于”),然后将一定量的稀H2SO4加入该NaOH溶液中,混合均匀后再测定其pH,发现其pH小于7.
结论:稀H2SO4与NaOH溶液发生了化学反应,并且 过量.
(2)方案二:利用酸碱指示剂
①探究稀H2SO4与NaOH溶液的反应

如图所示进行实验.当滴入几滴酚酞溶液后,溶液由无色变为 色.根据上述过程中的颜色变化,确定稀H2SO4与NaOH溶液发生了反应,该反应的化学方程式为 .
②探究上述稀H2SO4与NaOH溶液反应后烧杯中的硫酸是否过量
根据上述反应过程中溶液变成无色,不能确定稀H2SO4是否过量,同学们又分别选取BaCl2溶液与、紫色石蕊溶液、Na2CO3粉末设计实验方案,请你判断并分析:
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 方案一 | 取样,滴入适量的BaCl2溶液 | 出现白色沉淀 | 稀H2SO4过量 |
| 方案二 | 取样,滴入几滴紫色石蕊溶液 | 溶液变红 | 稀H2SO4过量 |
| 方案三 | 取样,加入Na2CO3粉末 | 有气体产生 | 稀H2SO4过量 |
在研究酸和碱的化学性质时,某小组同学想证明:稀H2SO4与NaOH溶液混合后,虽然仍为无色溶液,但确实发生了化学反应.请与他们一起完成实验方案设计、实施和评价.
(1)方案一:测定稀H2SO4与NaOH溶液混合前后的pH(常温下)他们先测定出某NaOH溶液的pH______7(填“大于”、“等于”或“小于”),然后将一定量的稀H2SO4加入该NaOH溶液中,混合均匀后再测定其pH,发现其pH小于7.
结论:稀H2SO4与NaOH溶液发生了化学反应,并且______过量.
(2)方案二:利用酸碱指示剂
①探究稀H2SO4与NaOH溶液的反应

如图所示进行实验.当滴入几滴酚酞溶液后,溶液由无色变为______色.根据上述过程中的颜色变化,确定稀H2SO4与NaOH溶液发生了反应,该反应的化学方程式为______.
②探究上述稀H2SO4与NaOH溶液反应后烧杯中的硫酸是否过量
根据上述反应过程中溶液变成无色,不能确定稀H2SO4是否过量,同学们又分别选取BaCl2溶液与、紫色石蕊溶液、Na2CO3粉末设计实验方案,请你判断并分析:
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 方案一 | 取样,滴入适量的BaCl2溶液 | 出现白色沉淀 | 稀H2SO4过量 |
| 方案二 | 取样,滴入几滴紫色石蕊溶液 | 溶液变红 | 稀H2SO4过量 |
| 方案三 | 取样,加入Na2CO3粉末 | 有气体产生 | 稀H2SO4过量 |
 溶液A中含有一种阳离子和一种阴离子,A与有关物质的关系如图所示:
溶液A中含有一种阳离子和一种阴离子,A与有关物质的关系如图所示: