摘要:B.碳酸钠+盐酸氯化钠+水+二氧化碳
网址:http://m.1010jiajiao.com/timu_id_922031[举报]
二氧化碳是一种奇妙的气体,在实验室可以很方便的制取.
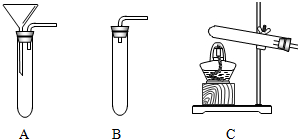
(1)实验室经常选用稀盐酸和
(2)组装好仪器后,将导管末端浸末在水中,用手捂试管,发现导管口有气泡,放手后,会
(3)用排空法收集二氧化碳,验满时可用
(4)甲同学现用某浓盐酸与石灰石制得的二氧化碳通入澄清石灰水中,则澄清石灰水
(5)要除去收集到的二氧化碳中混有的少量氯化氢气体,最好用
(6)测出该废液pH<7,则废液中大量存在的阳离子为
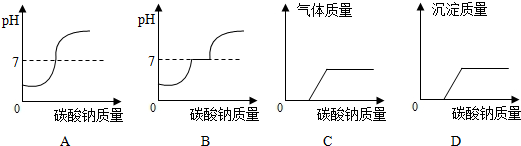
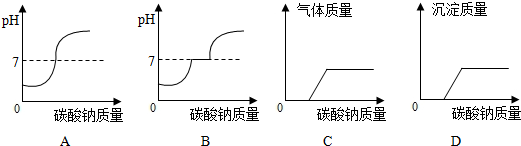
(7)向此废液滴加碳酸钠溶液至过量,则下图表示正确的为
查看习题详情和答案>>

(1)实验室经常选用稀盐酸和
大理石或石灰石
大理石或石灰石
作为反应物,发生装置可选用如上图中的B
B
(填字母),化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
;(2)组装好仪器后,将导管末端浸末在水中,用手捂试管,发现导管口有气泡,放手后,会
有水进入导管
有水进入导管
,说明气密性良好;(3)用排空法收集二氧化碳,验满时可用
AC
AC
方法(填字母)A.燃着木条 B.带火星木条 C.沾有澄清石灰水的玻璃棒 D.涂有酚酞的玻璃片;(4)甲同学现用某浓盐酸与石灰石制得的二氧化碳通入澄清石灰水中,则澄清石灰水
不一定
不一定
会变浑浊(填“一定”或“不一定”);(5)要除去收集到的二氧化碳中混有的少量氯化氢气体,最好用
C
C
(填字母)A.氢氧化钠 B.氢氧化钙 C.碳酸氢钠 D.浓硫酸;(6)测出该废液pH<7,则废液中大量存在的阳离子为
Ca2+、H+
Ca2+、H+
;(7)向此废液滴加碳酸钠溶液至过量,则下图表示正确的为
BD
BD
.
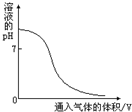 二氧化碳的水溶液的pH=5.6,氨气是碱性气体且能与氯化氢气体化合.向下列物质的水溶液中通入某种气体,溶液的pH随通入气体体积变化的曲线如图所示的是
二氧化碳的水溶液的pH=5.6,氨气是碱性气体且能与氯化氢气体化合.向下列物质的水溶液中通入某种气体,溶液的pH随通入气体体积变化的曲线如图所示的是( )
| A、向氯化钠溶液中通入氯化氢气体 | B、向石灰水中通入二氧化碳气体 | C、向稀盐酸中通入氨气 | D、向碳酸钠溶液中通入氯化氢气体 |
二氧化碳是一种奇妙的气体,在实验室可以很方便的制取.
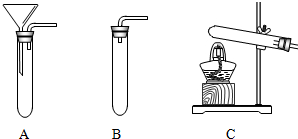
(1)实验室经常选用稀盐酸和______作为反应物,发生装置可选用如上图中的______(填字母),化学方程式为______;
(2)组装好仪器后,将导管末端浸末在水中,用手捂试管,发现导管口有气泡,放手后,会______,说明气密性良好;
(3)用排空法收集二氧化碳,验满时可用______方法(填字母)A.燃着木条 B.带火星木条 C.沾有澄清石灰水的玻璃棒 D.涂有酚酞的玻璃片;
(4)甲同学现用某浓盐酸与石灰石制得的二氧化碳通入澄清石灰水中,则澄清石灰水______会变浑浊(填“一定”或“不一定”);
(5)要除去收集到的二氧化碳中混有的少量氯化氢气体,最好用______(填字母)A.氢氧化钠 B.氢氧化钙 C.碳酸氢钠 D.浓硫酸;
(6)测出该废液pH<7,则废液中大量存在的阳离子为______;
(7)向此废液滴加碳酸钠溶液至过量,则下图表示正确的为______.
查看习题详情和答案>>
过碳酸钠(Na2CO4)在洗涤、印染、纺织、造纸、医药卫生等领域有大量应用,某化学研究性学习小组设计并完成了如下实验.
测定过碳酸钠样品(含有的杂质不溶于水且不与酸反应)的纯度.
实验原理2Na2CO4+4HCl═4NaCl+2CO2↑+O2↑+2H2O
实验装置
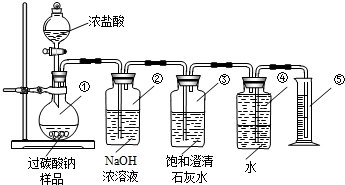
交流与讨论
Ⅰ.甲同学认为测定产物中O2的体积即可测定样品的纯度.
(1)装置②的作用是: ;
(2)装置③的作用是: ;
(3)称取适量样品与足量浓盐酸充分反应后,收集到的氧气的体积为0.25L(已知该实验条件下氧气的密度为1.28g/L),则称取的样品质量应大于 g;
Ⅱ.乙同学认为测定产物中CO2的质量(即反应前后装置②的质量差)就可测定样品的纯度.但利用上述实验装置测得CO2的质量并计算样品的纯度,结果会偏高,你认为原因可能是 ;(填序号
A.浓盐酸易挥发,产生的氯化氢气体被装置②吸收
B.二氧化碳气体逸出时带出的水蒸气在装置②中冷凝而被吸收
C.装置①、②内空气中的二氧化碳被装置②吸收
Ⅲ.丙同学提出了一种新方案,得到了大家的一致认可:称取样品12.5g,滴加足量浓盐酸至样品反应完全,再将烧瓶中所有的液体蒸发、结晶、烘干,称得氯化钠固体11.7g.则该样品的纯度为 .
查看习题详情和答案>>
测定过碳酸钠样品(含有的杂质不溶于水且不与酸反应)的纯度.
实验原理2Na2CO4+4HCl═4NaCl+2CO2↑+O2↑+2H2O
实验装置

交流与讨论
Ⅰ.甲同学认为测定产物中O2的体积即可测定样品的纯度.
(1)装置②的作用是:
(2)装置③的作用是:
(3)称取适量样品与足量浓盐酸充分反应后,收集到的氧气的体积为0.25L(已知该实验条件下氧气的密度为1.28g/L),则称取的样品质量应大于
Ⅱ.乙同学认为测定产物中CO2的质量(即反应前后装置②的质量差)就可测定样品的纯度.但利用上述实验装置测得CO2的质量并计算样品的纯度,结果会偏高,你认为原因可能是
A.浓盐酸易挥发,产生的氯化氢气体被装置②吸收
B.二氧化碳气体逸出时带出的水蒸气在装置②中冷凝而被吸收
C.装置①、②内空气中的二氧化碳被装置②吸收
Ⅲ.丙同学提出了一种新方案,得到了大家的一致认可:称取样品12.5g,滴加足量浓盐酸至样品反应完全,再将烧瓶中所有的液体蒸发、结晶、烘干,称得氯化钠固体11.7g.则该样品的纯度为
过碳酸钠(Na2CO4)在洗涤、印染、纺织、造纸、医药卫生等领域有大量应用,某化学研究性学习小组设计并完成了如下实验。
【实验目的】测定过碳酸钠样品(含有的杂质不溶于水且不与酸反应)的纯度。
【实验原理】2Na2CO4+ 4HCl → 4NaCl + 2CO2↑+ O2↑+ 2H2O
【实验装置】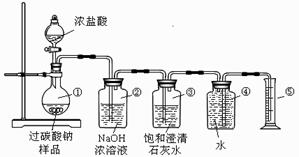
【交流与讨论】
①甲同学认为测定产物中O2的体积即可测定样品的纯度。装置②的作用是:(15);装置③的作用是:(16);
②乙同学认为测定产物中CO2的质量(即反应前后装置②的质量差)就可测定样品的纯度。但利用上述实验装置测得CO2的质量并计算样品的纯度,结果会偏高,你认为原因可能是;(17)(填序号)
A.浓盐酸易挥发,产生的氯化氢气体被装置②吸收
B.二氧化碳气体逸出时带出的水蒸气在装置②中冷凝而被吸收
C.装置①、②内空气中的二氧化碳被装置②吸收
③丙同学提出了一种新方案,得到了大家的一致认可:称取样品12.5g,滴加足量浓盐酸至样品反应完全,再将烧瓶中所有的液体蒸发、结晶、烘干,得到0.2mol氯化钠。则该样品的中过碳酸钠的质量分数为多少?(写出计算过程)