题目内容
二氧化碳是一种奇妙的气体,在实验室可以很方便的制取.

(1)实验室经常选用稀盐酸和
(2)组装好仪器后,将导管末端浸末在水中,用手捂试管,发现导管口有气泡,放手后,会
(3)用排空法收集二氧化碳,验满时可用
(4)甲同学现用某浓盐酸与石灰石制得的二氧化碳通入澄清石灰水中,则澄清石灰水
(5)要除去收集到的二氧化碳中混有的少量氯化氢气体,最好用
(6)测出该废液pH<7,则废液中大量存在的阳离子为
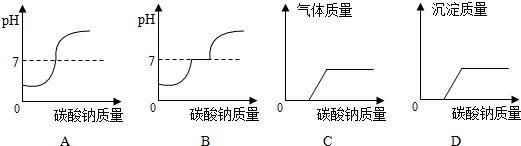
(7)向此废液滴加碳酸钠溶液至过量,则下图表示正确的为

(1)实验室经常选用稀盐酸和
大理石或石灰石
大理石或石灰石
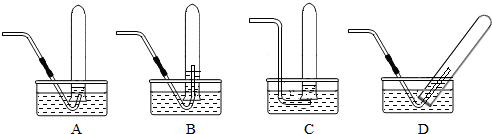
作为反应物,发生装置可选用如上图中的B
B
(填字母),化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
;(2)组装好仪器后,将导管末端浸末在水中,用手捂试管,发现导管口有气泡,放手后,会
有水进入导管
有水进入导管
,说明气密性良好;(3)用排空法收集二氧化碳,验满时可用
AC
AC
方法(填字母)A.燃着木条 B.带火星木条 C.沾有澄清石灰水的玻璃棒 D.涂有酚酞的玻璃片;(4)甲同学现用某浓盐酸与石灰石制得的二氧化碳通入澄清石灰水中,则澄清石灰水
不一定
不一定
会变浑浊(填“一定”或“不一定”);(5)要除去收集到的二氧化碳中混有的少量氯化氢气体,最好用
C
C
(填字母)A.氢氧化钠 B.氢氧化钙 C.碳酸氢钠 D.浓硫酸;(6)测出该废液pH<7,则废液中大量存在的阳离子为
Ca2+、H+
Ca2+、H+
;(7)向此废液滴加碳酸钠溶液至过量,则下图表示正确的为
BD
BD
.
分析:(1)实验室中通常是用大理石或石灰石和稀盐酸反应制取二氧化碳;
(2)制取气体或有气体参加的反应都要检验装置的气密性;
(3)二氧化碳不能燃烧、不支持燃烧,能使澄清的石灰水变浑浊;
(4)碳酸钙能和稀盐酸反应生成氯化钙、水和二氧化碳;
(5)二氧化碳不能和碳酸氢钠反应,氯化氢能和碳酸氢钠反应生成氯化钠、水和二氧化碳;
(6)稀盐酸和碳酸钙反应后,溶液显酸性,说明稀盐酸过量;
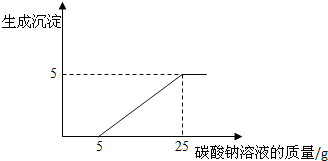
(7)废液中含有氯化钙和稀盐酸,加入碳酸钠溶液时,先和稀盐酸反应生成氯化钠、水和二氧化碳,当稀盐酸完全反应后,再和氯化钙反应生成碳酸钙沉淀和氯化钠.
(2)制取气体或有气体参加的反应都要检验装置的气密性;
(3)二氧化碳不能燃烧、不支持燃烧,能使澄清的石灰水变浑浊;
(4)碳酸钙能和稀盐酸反应生成氯化钙、水和二氧化碳;
(5)二氧化碳不能和碳酸氢钠反应,氯化氢能和碳酸氢钠反应生成氯化钠、水和二氧化碳;
(6)稀盐酸和碳酸钙反应后,溶液显酸性,说明稀盐酸过量;
(7)废液中含有氯化钙和稀盐酸,加入碳酸钠溶液时,先和稀盐酸反应生成氯化钠、水和二氧化碳,当稀盐酸完全反应后,再和氯化钙反应生成碳酸钙沉淀和氯化钠.
解答:解:(1)实验室经常选用稀盐酸和大理石或石灰石反应来制取二氧化碳,发生装置应该用B装置,因为反应不需要加热,A装置中生成的二氧化碳会从漏斗中逸出,大理石或石灰石的主要成分是碳酸钙,碳酸钙和稀盐酸反应能生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑.
故填:大理石或石灰石;B;CaCO3+2HCl=CaCl2+H2O+CO2↑.
(2)组装好仪器后,将导管末端浸末在水中,用手捂试管,发现导管口有气泡,放手后,会有水进入导管,说明气密性良好.
故填:有水进入导管.
(3)用排空法收集二氧化碳,验满时可用燃烧的木条或沾有澄清石灰水的玻璃棒,把燃烧的木条或沾有澄清石灰水的玻璃棒放在集气瓶口时,如果燃烧的木条熄灭,或澄清的石灰水变浑浊,说明已经收集满.
故填:AC.
(4)用某浓盐酸与石灰石制得的二氧化碳通入澄清石灰水中,则澄清石灰水不一定变浑浊,因为浓盐酸易挥发,挥发出的氯化氢气体随二氧化碳进入石灰水中,能和石灰水中的氢氧化钙反应生成氯化钙和水.
故填:不一定.
(5)要除去收集到的二氧化碳中混有的少量氯化氢气体,最好用碳酸氢钠溶液,因为二氧化碳不能和碳酸氢钠反应,氯化氢能和碳酸氢钠反应生成氯化钠、水和二氧化碳,而氢氧化钠和氢氧化钙既能够和二氧化碳反应,也能够和氯化氢反应;用浓硫酸不能除去氯化氢气体.
故填:C.
(6)测出该废液pH<7,说明稀盐酸过量,则废液中大量存在的阳离子为钙离子和氢离子,符号分别是Ca2+、H+.
故填:Ca2+、H+.
(7)向此废液滴加碳酸钠溶液至过量,碳酸钠先和稀盐酸反应生成氯化钠、水和二氧化碳,当稀盐酸完全反应后,再和氯化钙反应生成碳酸钙沉淀和氯化钠,B和D符合题意.
故填:BD.
故填:大理石或石灰石;B;CaCO3+2HCl=CaCl2+H2O+CO2↑.
(2)组装好仪器后,将导管末端浸末在水中,用手捂试管,发现导管口有气泡,放手后,会有水进入导管,说明气密性良好.
故填:有水进入导管.
(3)用排空法收集二氧化碳,验满时可用燃烧的木条或沾有澄清石灰水的玻璃棒,把燃烧的木条或沾有澄清石灰水的玻璃棒放在集气瓶口时,如果燃烧的木条熄灭,或澄清的石灰水变浑浊,说明已经收集满.
故填:AC.
(4)用某浓盐酸与石灰石制得的二氧化碳通入澄清石灰水中,则澄清石灰水不一定变浑浊,因为浓盐酸易挥发,挥发出的氯化氢气体随二氧化碳进入石灰水中,能和石灰水中的氢氧化钙反应生成氯化钙和水.
故填:不一定.
(5)要除去收集到的二氧化碳中混有的少量氯化氢气体,最好用碳酸氢钠溶液,因为二氧化碳不能和碳酸氢钠反应,氯化氢能和碳酸氢钠反应生成氯化钠、水和二氧化碳,而氢氧化钠和氢氧化钙既能够和二氧化碳反应,也能够和氯化氢反应;用浓硫酸不能除去氯化氢气体.
故填:C.
(6)测出该废液pH<7,说明稀盐酸过量,则废液中大量存在的阳离子为钙离子和氢离子,符号分别是Ca2+、H+.
故填:Ca2+、H+.
(7)向此废液滴加碳酸钠溶液至过量,碳酸钠先和稀盐酸反应生成氯化钠、水和二氧化碳,当稀盐酸完全反应后,再和氯化钙反应生成碳酸钙沉淀和氯化钠,B和D符合题意.
故填:BD.
点评:化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相互之间的反应关系,有助于提高观察实验、进行实验的能力.所以,对化学实验不仅要认真观察,还应掌握设计实验、观察实验现象的方法.

练习册系列答案
相关题目
 二氧化碳是一种奇妙的气体,在实验室可以很方便的制取.
二氧化碳是一种奇妙的气体,在实验室可以很方便的制取.

