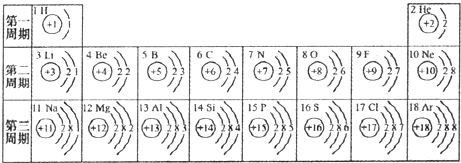
摘要:元素周期表是我们学习化学和研究化学的重要工具.下表是元素周期表中1-18号元素原子核外电子排布.我对它进行研究:
网址:http://m.1010jiajiao.com/timu_id_922007[举报]
元素周期表是我们学习化学和研究化学的重要工具.下表是元素周期表中1~18号元素原子的核外电子排布,请回答:
(1)第13号元素名称是
(2)原子序数为11、17的元素组成化合物的化学式
(3)对1~18号元素的原子结构示意图进行分析,可以发现许多规律,如第一周期元素的原子核外只有一个电子层.请再总结出其他规律,并写出其中两条:
①

查看习题详情和答案>>
(1)第13号元素名称是
铝
铝
,它属于金属
金属
(填“金属”或“非金属”)元素,它在化学反应中容易失去
失去
电子,它的离子符号为Al3+
Al3+
.(2)原子序数为11、17的元素组成化合物的化学式
NaCl
NaCl
.(3)对1~18号元素的原子结构示意图进行分析,可以发现许多规律,如第一周期元素的原子核外只有一个电子层.请再总结出其他规律,并写出其中两条:
①
每一周期元素的原子的核外电子层数相同
每一周期元素的原子的核外电子层数相同
;②每一周期元素原子的最外层电子数从左到右逐渐增加
每一周期元素原子的最外层电子数从左到右逐渐增加
.
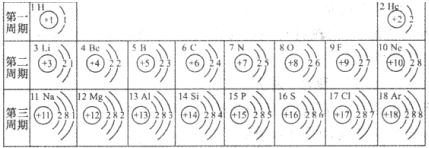
元素周期表是我们学习化学和研究化学的重要工具.如图所示是元素周期表中1~18号元素原子核外电子排布,请你对它进行研究:

(1)稀有气体原子最外层电子数为
(2)第11号元素名称是
查看习题详情和答案>>

(1)稀有气体原子最外层电子数为
8
8
个(He除外,为2个),达到稳定结构,所以稀有气体化学性质稳定;金属原子最外层电子数一般<4个,容易失去
失去
电子,变成阳
阳
离子;非金属原子的最外层电子数一般≥4个,容易得到
得到
电子,变成阴
阴
离子.(2)第11号元素名称是
钠
钠
,它在化学反应中容易失去
失去
电子,它的离子符号为Na+
Na+
;第17号元素名称是氯
氯
,它在化学反应中容易得到
得到
电子,它的离子符号为Cl-
Cl-
.这两种离子相互作用就形成了氯化钠
氯化钠
(填一种具体物质的名称)元素周期表是我们学习化学和研究化学的重要工具.下表是元素周期表中1~18号元素原子核外电子排布,我对它进行研究:
| 第一周期 | 1 H | 2 He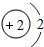 | ||||||
| 第二周期 | 3 Li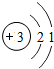 | 4 Be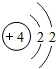 | 5 B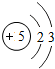 | 6 C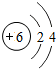 | 7 N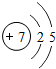 | 8 O | 9 F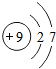 | 10 Ne |
| 第三周期 | 11 Na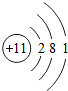 | 12 Mg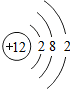 | 13 Al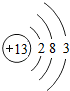 | 14 Si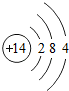 | 15 P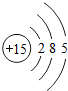 | 16 S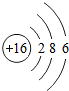 | 17 Cl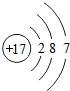 | 18 Ar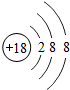 |
(2)从上表中我探究出以下规律:在原子里核电荷数=原子序数=______.
(3)我通过细致地分析,还可以总结出元素周期表的一些规律:如______. 查看习题详情和答案>>