网址:http://m.1010jiajiao.com/timu_id_920837[举报]

(1)吃火锅用的锅体是由铜合金制造的,主要是因为铜合金具有很好的
A.导电性 B.导热性 C.延展性
(2)金属锈蚀造成浪费.铁制品锈蚀的过程,实际上是铁与空气中的氧气、
(3)目前世界上已有50%以上的废钢铁得到回收利用,其目的是
A.节约金属资源 B.合理开采矿物 C.防止钢铁生锈
(4)实验室有锌片、铁片、铜片、稀硫酸、硫酸锌溶液、硫酸亚铁溶液和硫酸铜溶液7种物质,小红选择合适的物质,设计了以下三种方法对锌、铜、铁的金属活动性顺序进行验证.
①方法一所选用的3种物质是
②方法二所选用的3种物质是锌片、铜片和
③方法三所选用4种物质是锌片、铁片、铜片和稀硫酸,能验证锌、铁、铜的金属活动性顺序的实验现象是
(5)炼铁的原理是利用一氧化碳与氧化铁反应.在实验室里,可用如图1所示装置进行实验:实验中玻璃管内的粉末由红色变为
| ||
| ||
(6)向CuSO4溶液中加入Zn、Fe、Mg混合物,充分搅拌后过滤,得浅绿色溶液A,将滤渣放入稀盐酸中,产生无色气体.由以上事实可推知滤液A中含有的溶质是
(7)为探究铁和锌两种金属与酸反应的状况,将等质量的两种金属分别与等质量的溶质质量分数相同的稀硫酸反应,产生氢气的质量与反应时间的函数关系如图2、3所示.下列相关判断中,正确的是
A.甲是铁,乙是锌 B.甲是锌,乙是铁
C.图2表示稀硫酸足量,图3表示稀硫酸不足量
D.图2表示金属一定有剩余,图3表示金属一定没有剩余.
 铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关.
铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关.(1)在空气中
(2)现有这三种金属,用下列试剂验证金属活动性顺序,能达到目的是
A.氯化铜溶液 B.氯化亚铁溶液 C.氯化铝溶液
(3)金属与酸反应的剧烈程度与许多因素有关.如图是20℃时相同质量的铁粉、铁片、铝粉、铝片分别与足量稀盐酸完全反应,产生氢气的质量与时间的关系图.
①写出铝与15%的盐酸反应的化学方程式
②根据上图推测,金属A是
a.铝片 b.铝粉 c. 铁片 d.铁粉
③金属B与10%的稀盐酸反应的现象是:产生气泡、固体量减少、
④图中铝片、铁片分别与15%的稀盐酸完全反应,产生的氢气质量之比为
由此可以分析、归纳出影响金属与酸反应速率的因素有:金属的种类、
(4)某钢铁厂每天需消耗5000t含Fe2O380%的赤铁矿石,该厂理论上可日产含铁98%的生铁的质量是多少?(精确到小数点后1位)计算过程
(10分)铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关。
(1)在空气中 制品(填“铝”或“铁”)更耐腐蚀,原因是 。
(2)现有这三种金属,用下列试剂验证金属活动性顺序,能达到目的是 (填
序号)。
A.氯化铜溶液 B.氯化亚铁溶液 C.氯化铝溶液
(3)金属与酸反应的剧烈程度与许多因素有关。下图是20℃时相同质量的铁粉、铁片、
铝粉、铝片分别与足量稀盐酸完全反应,产生氢气的质量与时间的关系图。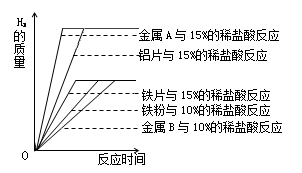
①写出铝与15%的盐酸反应的化学方程式 。
②根据上图推测,金属A是 (填字母序号)。
a.铝片 b.铝粉 c. 铁片 d.铁粉
③金属B与10%的稀盐酸反应的现象是:产生气泡、固体量减少、 。
④图中铝片、铁片分别与15%的稀盐酸完全反应,产生的氢气质量之比为 。
由此可以分析、归纳出影响金属与酸反应速率的因素有:金属的种类、 和酸的浓度。
(4)某钢铁厂每天需消耗5000t含Fe2O380%的赤铁矿石,该厂理论上可日产含铁98%的生铁的质量是多少?(精确到小数点后1位)计算过程 。
(10分)铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关。
(1)在空气中 制品(填“铝”或“铁”)更耐腐蚀,原因是 。
(2)现有这三种金属,用下列试剂验证金属活动性顺序,能达到目的是 (填
序号)。
A.氯化铜溶液 B.氯化亚铁溶液 C.氯化铝溶液
(3)金属与酸反应的剧烈程度与许多因素有关。下图是20℃时相同质量的铁粉、铁片、
铝粉、铝片分别与足量稀盐酸完全反应,产生氢气的质量与时间的关系图。

①写出铝与15%的盐酸反应的化学方程式 。
②根据上图推测,金属A是 (填字母序号)。
a.铝片 b.铝粉 c. 铁片 d.铁粉
③金属B与10%的稀盐酸反应的现象是:产生气泡、固体量减少、 。
④图中铝片、铁片分别与15%的稀盐酸完全反应,产生的氢气质量之比为 。
由此可以分析、归纳出影响金属与酸反应速率的因素有:金属的种类、 和酸的浓度。
(4)某钢铁厂每天需消耗5000t含Fe2O380%的赤铁矿石,该厂理论上可日产含铁98%的生铁的质量是多少?(精确到小数点后1位)计算过程 。
查看习题详情和答案>>
 铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关.
铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关.