摘要:30.某兴趣小组同学对于实验室制得的烧碱粗产品(杂质为Na2CO3和NaCl)进行了测定分析.取20.0g烧碱粗产品.逐滴滴入10%的盐酸至过量.消耗的稀盐酸与生成CO2的质量关系如下图所示(不考虑二氧化碳气体的溶解)
网址:http://m.1010jiajiao.com/timu_id_912045[举报]
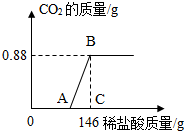 某兴趣小组同学对于实验室制得的烧碱粗产品(杂质为Na2CO3和NaCl)进行了测定分析.取20.0g烧碱粗产品,逐滴滴入10%的盐酸至过量,消耗的稀盐酸与生成CO2的质量关系如下图所示(不考虑二氧化碳气体的溶解)
某兴趣小组同学对于实验室制得的烧碱粗产品(杂质为Na2CO3和NaCl)进行了测定分析.取20.0g烧碱粗产品,逐滴滴入10%的盐酸至过量,消耗的稀盐酸与生成CO2的质量关系如下图所示(不考虑二氧化碳气体的溶解)(1)关系图中OA段、AB段对应的过程中发生反应的化学方程式分别为:
(2)计算出A点对应的数值及粗产品中氢氧化钠的质量.(计算结果保留两位小数) 查看习题详情和答案>>
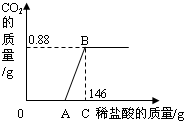 某兴趣小组同学对于实验室制得的烧碱粗产品(杂质为Na2CO3和NaCl)进行了测定分析.取20.0g烧碱粗产品,逐滴滴入10%的盐酸至过量,消耗的稀盐酸与生成CO2的质量关系如下图所示(不考虑二氧化碳气体的溶解)
某兴趣小组同学对于实验室制得的烧碱粗产品(杂质为Na2CO3和NaCl)进行了测定分析.取20.0g烧碱粗产品,逐滴滴入10%的盐酸至过量,消耗的稀盐酸与生成CO2的质量关系如下图所示(不考虑二氧化碳气体的溶解)
(1)关系图中OA段、AB段对应的过程中发生反应的化学方程式分别为:______,______;
(2)计算出A点对应的数值及粗产品中氢氧化钠的质量.(计算结果保留两位小数)
查看习题详情和答案>>
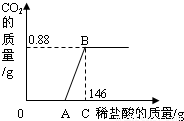
某兴趣小组同学对于实验室制得的烧碱粗产品(杂质为Na2CO3和NaCl)进行了测定分析.取20.0g烧碱粗产品,逐滴滴入10%的盐酸至过量,消耗的稀盐酸与生成CO2的质量关系如下图所示(不考虑二氧化碳气体的溶解)
(1)关系图中OA段、AB段对应的过程中发生反应的化学方程式分别为:______,______;
(2)计算出A点对应的数值及粗产品中氢氧化钠的质量.(计算结果保留两位小数)
 查看习题详情和答案>>
查看习题详情和答案>>
(1)关系图中OA段、AB段对应的过程中发生反应的化学方程式分别为:______,______;
(2)计算出A点对应的数值及粗产品中氢氧化钠的质量.(计算结果保留两位小数)
 查看习题详情和答案>>
查看习题详情和答案>>
某兴趣小组同学对实验室制取氧气的条件进行如下探究实验.
(1)已知2KClO3
2KCl+3O2↑,CuO也可作氯酸钾分解的催化剂.甲同学为探究催化剂的种类对氯酸钾分解速率的影响,设计了以下对比试验:
I.将xgKClO3与1.0gMnO2均匀混合加热 II.将3.0gKClO3与1.0gCuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.
①I中x的值为
(2)乙同学探究了影响双氧水分解速度的某种因素,实验数据记录如表:
【数据处理及结论】
①本实验中,测量O2体积的装置是
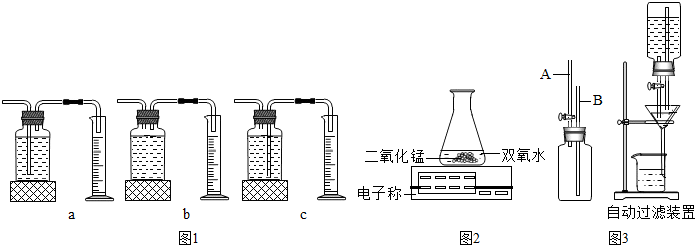
②实验结论:在相同条件下,
③丙用如图2装置进行实验,通过比较
(3)用氯酸钾和二氧化锰的混合物制取O2,完全反应后的固体残渣,经以下四步实验操作,可回收得到较纯净的二氧化锰(残渣中只有二氧化锰难于水).正确操作的先后顺序是
a.烘干 b.溶解 c.过滤 d.洗涤
(4)某同学根据所学知识设计了一个自动加液过滤装置:在普通过滤装置的漏斗上安装一个自动加液装置(图3).使用时,滤液不会溢出,过滤又较快,整个过程无须人照顾.自动加液装置中A管为“液体流出管”,B管为“空气导入管”. A管上口高出B管口约1cm.试回答问题:A管上口高出B管上口的理由是
查看习题详情和答案>>
(1)已知2KClO3
| ||
| △ |
I.将xgKClO3与1.0gMnO2均匀混合加热 II.将3.0gKClO3与1.0gCuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.
①I中x的值为
3.0
3.0
;②II中的CuO与稀盐酸反应的方程式为CuO+2HCl=CuCl2+H2O
CuO+2HCl=CuCl2+H2O
.(2)乙同学探究了影响双氧水分解速度的某种因素,实验数据记录如表:
| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2的体积 | |
| I | 50.0g | 1% | 0.1g | 9mL |
| II | 50.0g | 2% | 0.1g | 16mL |
| III | 50.0g | 4% | 0.1g | 31mL |
①本实验中,测量O2体积的装置是
C
C
(填编号).
②实验结论:在相同条件下,
双氧水浓度越大
双氧水浓度越大
,双氧水分解得快.③丙用如图2装置进行实验,通过比较
相同时间天平读数差值大小
相同时间天平读数差值大小
也能达到实验目的.(3)用氯酸钾和二氧化锰的混合物制取O2,完全反应后的固体残渣,经以下四步实验操作,可回收得到较纯净的二氧化锰(残渣中只有二氧化锰难于水).正确操作的先后顺序是
bcda
bcda
(填写选项符号).a.烘干 b.溶解 c.过滤 d.洗涤
(4)某同学根据所学知识设计了一个自动加液过滤装置:在普通过滤装置的漏斗上安装一个自动加液装置(图3).使用时,滤液不会溢出,过滤又较快,整个过程无须人照顾.自动加液装置中A管为“液体流出管”,B管为“空气导入管”. A管上口高出B管口约1cm.试回答问题:A管上口高出B管上口的理由是
便于达到“自动过滤”的目的;若A管上口低于B管上口或与B管上口平齐都不能实现“自动过滤”的目的
便于达到“自动过滤”的目的;若A管上口低于B管上口或与B管上口平齐都不能实现“自动过滤”的目的
.某兴趣小组同学对实验室制备氧气的若干问题进行如下实验探究.
(1)为探究催化剂的种类对氯酸钾分解速度的影响,甲同学设计以下对比实验:
Ⅰ.将2.45g KClO3与1.0g MnO2均匀混合加热
Ⅱ.将 x g KClO3与1.0g CuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.通常采用的方法有:
①测相同时间内产生O2的体积
②测
Ⅰ中反应的文字表达式是
Ⅱ中x的值应为
(2)乙同学探究了影响双氧水分解速度的某种因素,实验数据记录如表:
【数据处理及结论】
I.本实验中,测量O2体积的装置是
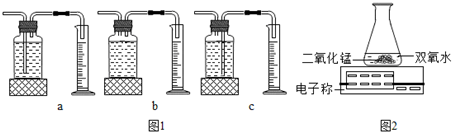
II.实验结论:在相同条件下,
III.丙用如图2装置进行实验,通过比较
(3)丙同学用KClO3和MnO2的混合物制取O2,完全反应后的固体残渣,经以下四步实验操作,回收得到了较纯净的MnO2(残渣中只有MnO2难于水).
他的正确操作先后顺序是
a.烘干 b.溶解 c.过滤 d.洗涤
步骤 c需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、
(4)丁同学在学习了质量守恒定律后,尝试计算了甲同学的实验中2.45g KClO3完全分解后生成O2的质量为
查看习题详情和答案>>
(1)为探究催化剂的种类对氯酸钾分解速度的影响,甲同学设计以下对比实验:
Ⅰ.将2.45g KClO3与1.0g MnO2均匀混合加热
Ⅱ.将 x g KClO3与1.0g CuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.通常采用的方法有:
①测相同时间内产生O2的体积
②测
收集相同体积O2所需的时间
收集相同体积O2所需的时间
;Ⅰ中反应的文字表达式是
氯酸钾
氯化钾+氧气
| 二氧化锰 |
| 加热 |
氯酸钾
氯化钾+氧气
;| 二氧化锰 |
| 加热 |
Ⅱ中x的值应为
2.45
2.45
.(2)乙同学探究了影响双氧水分解速度的某种因素,实验数据记录如表:
| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2的体积 | |
| I | 50.0g | 1% | 0.1g | 9mL |
| II | 50.0g | 2% | 0.1g | 16mL |
| III | 50.0g | 4% | 0.1g | 31mL |
I.本实验中,测量O2体积的装置是
c
c
(选填图1中“a”“b”“c”编号).
II.实验结论:在相同条件下,
双氧水浓度越大
双氧水浓度越大
,双氧水分解速率越快.III.丙用如图2装置进行实验,通过比较
相同时间天平读数差值大小(或电子称上示数减小的速度)
相同时间天平读数差值大小(或电子称上示数减小的速度)
也能达到实验目的.(3)丙同学用KClO3和MnO2的混合物制取O2,完全反应后的固体残渣,经以下四步实验操作,回收得到了较纯净的MnO2(残渣中只有MnO2难于水).
他的正确操作先后顺序是
bcda
bcda
(填写选项符号).a.烘干 b.溶解 c.过滤 d.洗涤
步骤 c需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、
玻璃棒
玻璃棒
,所填仪器在过滤操作中的作用是引流
引流
.(4)丁同学在学习了质量守恒定律后,尝试计算了甲同学的实验中2.45g KClO3完全分解后生成O2的质量为
0.96
0.96
g,标准状况下的O2体积为671.8
671.8
mL.(已知标准状况下,氧气密度为1.429g/L,结果精确到0.1mL)(无需写计算过程)