摘要:28.“观察.分析.归纳 是化学研究的重要步骤.有A.B.C.D四种物质.他们可能是Cu.CuO.CuSO4和FeSO4在小明的实验中可见到它们的踪影.实验Ⅰ:将黑色粉末A置于试管中.加入20 mL稀硫酸.A完全溶解.得到蓝色溶液B.实验Ⅱ:向蓝色溶液中加入过量铁粉.充分反应.产生红色固体C和浅绿色溶液D.且反应过程中还有氢气气泡产生. 试帮助小明分析.回答下列问题.(1)写出下列物质或溶质的化学式: A. B. C. D. .(2)能说明实验I中A与稀硫酸完全反应后.稀硫酸有剩余的实验现象是 .(3)写出一个反应物中有CuO的置换反应的化学方程式.
网址:http://m.1010jiajiao.com/timu_id_910120[举报]
“观察、分析、归纳”是化学研究的重要步骤.有A、B、C、D四种物质,他们可能是Cu、CuO、CuSO4和FeSO4在小明的实验中可见到它们的踪影.
实验Ⅰ:将黑色粉末A置于试管中,加入20mL稀硫酸,A完全溶解,得到蓝色溶液B.
实验Ⅱ:向蓝色溶液中加入过量铁粉,充分反应,产生红色固体C和浅绿色溶液D,且反应过程中还有氢气气泡产生.
试帮助小明分析、回答下列问题.
(1)写出下列物质或溶质的化学式:A. B. C. D. .
(2)能说明实验I中A与稀硫酸完全反应后,稀硫酸有剩余的实验现象是 .
(3)写出一个反应物中有CuO的置换反应的化学方程式. .
查看习题详情和答案>>
实验Ⅰ:将黑色粉末A置于试管中,加入20mL稀硫酸,A完全溶解,得到蓝色溶液B.
实验Ⅱ:向蓝色溶液中加入过量铁粉,充分反应,产生红色固体C和浅绿色溶液D,且反应过程中还有氢气气泡产生.
试帮助小明分析、回答下列问题.
(1)写出下列物质或溶质的化学式:A.
(2)能说明实验I中A与稀硫酸完全反应后,稀硫酸有剩余的实验现象是
(3)写出一个反应物中有CuO的置换反应的化学方程式.
“观察、分析、归纳”是化学研究的重要步骤.有A、B、C、D四种物质,他们可能是Cu、CuO、CuSO4和FeSO4在小明的实验中可见到它们的踪影.
实验Ⅰ:将黑色粉末A置于试管中,加入20mL稀硫酸,A完全溶解,得到蓝色溶液B.
实验Ⅱ:向蓝色溶液中加入过量铁粉,充分反应,产生红色固体C和浅绿色溶液D,且反应过程中还有氢气气泡产生.
试帮助小明分析、回答下列问题.
(1)写出下列物质或溶质的化学式:A.______B.______C.______D.______.
(2)能说明实验I中A与稀硫酸完全反应后,稀硫酸有剩余的实验现象是______.
(3)写出一个反应物中有CuO的置换反应的化学方程式.______.
查看习题详情和答案>>
分析与归纳是化学学习中重要的思想方法,小明同学在学习了物质的分类知识后,从宏观上得出了如图所示的知识结构:物质
请你参照它的做法,从微观上把构成物质的微粒之间的关系总结出来. 查看习题详情和答案>>
|
请你参照它的做法,从微观上把构成物质的微粒之间的关系总结出来. 查看习题详情和答案>>
(2012?陕西)分类归纳是化学学习的重要方法.下面是某同学对所学物质的分类归纳,请仔细分析并回答下列问题:
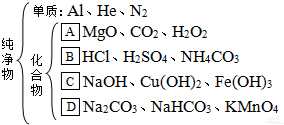
(1)写出C组物质所属的类别
(2)在分类所列举的物质中,有一种物质归类错误,这种物质是
(3)选择分类物质中的一种,写出一个有单质生成的分解反应的化学方程式(条件所需物质不受所列物质限制)
查看习题详情和答案>>
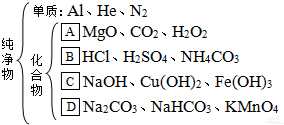
(1)写出C组物质所属的类别
碱
碱
.(2)在分类所列举的物质中,有一种物质归类错误,这种物质是
碳酸铵
碳酸铵
.(3)选择分类物质中的一种,写出一个有单质生成的分解反应的化学方程式(条件所需物质不受所列物质限制)
2KMnO4
K2MnO4+MnO2+O2↑
| ||
2KMnO4
K2MnO4+MnO2+O2↑
.
| ||
(2011?淄博)金属材料被广泛的应用于我们的生活中,不仅是因为其物理性能优良,还与它们的化学性质密切相关.下面是小明同学设计测定金属铁、铜和镁的活动性的探究实验过程和实验记录,请你一起探究.
【实验记录】测定金属铁、铜和镁的活动性强弱
【所用试剂】稀硫酸、硝酸银溶液、光亮的薄铁片、薄铜片、薄镁片
【实验过程】
步骤Ⅰ将铁片、铜片、镁片分别在空气中点燃片刻,观察燃烧现象;
步骤Ⅱ将铁片、铜片、镁片分别放入三只盛有溶质质量分数相同、体积相同的稀硫酸的试管中;
步骤Ⅲ将铁片、铜片、镁片分别放入三只盛有溶质质量分数相同、体积相同的硝酸银溶液的试管中.
【实验记录】用“√”表示能观察到实验现象,用“-”表示观察不到实验现象(见右表).
实验现象记录表
(1)通过步骤Ⅰ可以得出三种金属中镁的金属活动性最强,判断依据是
(2)运用“控制变量法”设计实验方案是化学研究的重要方法.步骤Ⅱ和步骤Ⅲ中,需要控制的实验条件除了金属的体积、溶液的体积、溶质质量分数以外,还需要控制的条件是
【实验结论】金属铁、铜和镁的活动性由强到弱的顺序是
【反思交流】若利用上述试剂制取氢气,小明认为应该选择金属铁和稀硫酸反应,而不选择金属镁和稀硫酸反应,他的理由是
查看习题详情和答案>>
【实验记录】测定金属铁、铜和镁的活动性强弱
【所用试剂】稀硫酸、硝酸银溶液、光亮的薄铁片、薄铜片、薄镁片
【实验过程】
步骤Ⅰ将铁片、铜片、镁片分别在空气中点燃片刻,观察燃烧现象;
步骤Ⅱ将铁片、铜片、镁片分别放入三只盛有溶质质量分数相同、体积相同的稀硫酸的试管中;
步骤Ⅲ将铁片、铜片、镁片分别放入三只盛有溶质质量分数相同、体积相同的硝酸银溶液的试管中.
【实验记录】用“√”表示能观察到实验现象,用“-”表示观察不到实验现象(见右表).
实验现象记录表
| 金属 | 空气 | 稀硫酸 | 硝酸银溶液 |
| 铁 | - | √ | √ |
| 铜 | - | - | √ |
| 镁 | √ | √ | √ |
在空气中,镁能和氧气反应的最剧烈
在空气中,镁能和氧气反应的最剧烈
(2)运用“控制变量法”设计实验方案是化学研究的重要方法.步骤Ⅱ和步骤Ⅲ中,需要控制的实验条件除了金属的体积、溶液的体积、溶质质量分数以外,还需要控制的条件是
溶液的种类
溶液的种类
.写出镁和稀硫酸反应的化学方程式Mg+H2SO4=MgSO4+H2↑
Mg+H2SO4=MgSO4+H2↑
,此反应属于置换反应
置换反应
.【实验结论】金属铁、铜和镁的活动性由强到弱的顺序是
Mg Fe Cu
Mg Fe Cu
(用元素符号表示)【反思交流】若利用上述试剂制取氢气,小明认为应该选择金属铁和稀硫酸反应,而不选择金属镁和稀硫酸反应,他的理由是
Mg和H2SO4反应速度太快,不易控制
Mg和H2SO4反应速度太快,不易控制
.