题目内容
“观察、分析、归纳”是化学研究的重要步骤.有A、B、C、D四种物质,他们可能是Cu、CuO、CuSO4和FeSO4在小明的实验中可见到它们的踪影.
实验Ⅰ:将黑色粉末A置于试管中,加入20mL稀硫酸,A完全溶解,得到蓝色溶液B.
实验Ⅱ:向蓝色溶液中加入过量铁粉,充分反应,产生红色固体C和浅绿色溶液D,且反应过程中还有氢气气泡产生.
试帮助小明分析、回答下列问题.
(1)写出下列物质或溶质的化学式:A. B. C. D. .
(2)能说明实验I中A与稀硫酸完全反应后,稀硫酸有剩余的实验现象是 .
(3)写出一个反应物中有CuO的置换反应的化学方程式. .
实验Ⅰ:将黑色粉末A置于试管中,加入20mL稀硫酸,A完全溶解,得到蓝色溶液B.
实验Ⅱ:向蓝色溶液中加入过量铁粉,充分反应,产生红色固体C和浅绿色溶液D,且反应过程中还有氢气气泡产生.
试帮助小明分析、回答下列问题.
(1)写出下列物质或溶质的化学式:A.
(2)能说明实验I中A与稀硫酸完全反应后,稀硫酸有剩余的实验现象是
(3)写出一个反应物中有CuO的置换反应的化学方程式.
分析:将黑色粉末A置于试管中,加入20mL稀硫酸,A完全溶解,得到蓝色溶液B,可以知道A中含有氧化铜,而蓝色溶液B为硫酸铜溶液,加入过量铁粉后得到的红色固体为铜,浅绿色溶液为硫酸亚铁溶液,而反应过程中产生气体,说明稀硫酸有剩余,可以据此结合体题中问题完成解答即可.
解答:解:(1)将黑色粉末A置于试管中,加入20mL稀硫酸,A完全溶解,得到蓝色溶液B,可以知道A中含有氧化铜,其化学式为CuO;而蓝色溶液B为硫酸铜溶液,其化学式为CuSO4;加入过量铁粉后得到的红色固体为铜,其化学式为Cu,浅绿色溶液D为硫酸亚铁溶液,其化学式为FeSO4;
(2)铁粉可以和稀硫酸反应生成气体,所以反应过程中产生气体,说明稀硫酸有剩余;
(3)生成物中能够和氧化铜发生反应的为氢气,该反应的化学方程式为:H2+CuO
Cu+H2O.
故答案为:(1)CuO;CuSO4;Cu;FeSO4;
(2)反应过程中产生气体;
(3)H2+CuO
Cu+H2O.
(2)铁粉可以和稀硫酸反应生成气体,所以反应过程中产生气体,说明稀硫酸有剩余;
(3)生成物中能够和氧化铜发生反应的为氢气,该反应的化学方程式为:H2+CuO
| ||
故答案为:(1)CuO;CuSO4;Cu;FeSO4;
(2)反应过程中产生气体;
(3)H2+CuO
| ||
点评:解答这类题目时,一定要先找突破口或题眼;然后再根据题意,结合所学的相关知识顺藤摸瓜即可.

练习册系列答案
相关题目
建立“问题意识“是提升化学思维的前提之一.小明在观察煤燃烧的过程中发现了几个问题,为解决这些问题,他建立了下表中的一种思维模型,请你帮他填写表中的相关内容.
| 观察发现 | 分析解释 | 知识归纳 | ||||
| (1)煤要用木柴等引燃 | 燃烧需要可燃物、氧气温度必须达到着火点 | |||||
| (2) |
一氧化碳在燃烧,化学方程式是 |
煤燃烧有CO生成,CO是许多气体燃料的主要成分 | ||||
| (3)通常在煤燃烧较旺时添加新煤 | C+CO2
|
从化学反应中伴随着能量变化看,该反应是 | ||||
| (4)蜂窝煤燃烧后的剩余固体质量比燃烧前的质量轻 | 煤燃烧生成了二氧化碳等气体 | 理论依据是 |
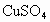 和
和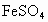 .在小明的实验中可见到它们的踪影.
.在小明的实验中可见到它们的踪影.