摘要:(4)经过过滤.洗涤.烘干.称量固体质量为1.165 mg.计算:1.165 mg硫酸钡中硫元素的质量为 mg,由质量守恒定律可知.2 L空气样品中SO2的质量为 mg,由空气质量标准可得出结论:该厂排放的SO2 .[发现新问题]考虑到空气中的各种气体成分.第一组认为第二组同学测出的SO2的含量偏大.其依据是 ,你提出的实验改进方案是 .[反思与应用] 为尽快改善该地区的空气质量.请你提出一条合理化建议: .
网址:http://m.1010jiajiao.com/timu_id_907944[举报]
氢氧化钠固体常因吸收空气中的二氧化碳而变质.某研究性学习小组为探究氢氧化钠固体样品中的碳酸钠的质量分数(仅考虑样品为NaOH和Na2CO3的混合物),设计了多种实验方案,请结合以下方案回答有关问题:
方案一:
称取一定量的氢氧化钠样品,加水溶解后,逐滴加入沉淀剂氢氧化钡溶液至不再产生沉淀为止.将沉淀过滤、洗涤、烘干、称量.
则:(1)沉淀洗涤的目的是 ,若不洗涤,则所测定的样品中碳酸钠的质量分数 (填“偏大”、“偏小”或“无影响”).证明沉淀已经洗涤干净的方法:向最后一次洗涤后的滤液中加入 试剂(填化学式),若无沉淀产生,说明洗涤干净.
方案二:
(2)利用下图装置测定氢氧化钠样品中 Na2CO3的质量分数,则必需的数据有:样品质量、反应前 锥形瓶及其中各物质的总质量、 .该方案有误差,请写出引起误差的一个原因: .
锥形瓶及其中各物质的总质量、 .该方案有误差,请写出引起误差的一个原因: .
方案三:
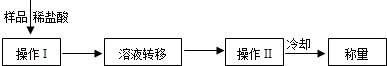
(3)操作Ⅰ中加入稀盐酸应过量的原因是 ,
操作Ⅱ中需要的仪器有铁架台(含铁圈)、玻璃棒、酒精灯和 ,若该方案中样品质量为9.3g,最终称量冷却后的晶体质量为11.7g.
为计算碳酸钠的质量分数,小刚同学通过列二元一次方程组的办法得到两个表达式:
解:设样品中NaOH的质量为x,Na2CO3的质量为y.
请判断这两个方程组中是否存在问题,若有错误,请将纠正后的方程写在横线上: .
经计算碳酸钠的质量分数为 .(写出计算过程)
查看习题详情和答案>>
方案一:
称取一定量的氢氧化钠样品,加水溶解后,逐滴加入沉淀剂氢氧化钡溶液至不再产生沉淀为止.将沉淀过滤、洗涤、烘干、称量.
则:(1)沉淀洗涤的目的是
方案二:
(2)利用下图装置测定氢氧化钠样品中 Na2CO3的质量分数,则必需的数据有:样品质量、反应前
 锥形瓶及其中各物质的总质量、
锥形瓶及其中各物质的总质量、方案三:

(3)操作Ⅰ中加入稀盐酸应过量的原因是
操作Ⅱ中需要的仪器有铁架台(含铁圈)、玻璃棒、酒精灯和
为计算碳酸钠的质量分数,小刚同学通过列二元一次方程组的办法得到两个表达式:
解:设样品中NaOH的质量为x,Na2CO3的质量为y.
|
请判断这两个方程组中是否存在问题,若有错误,请将纠正后的方程写在横线上:
经计算碳酸钠的质量分数为
氢氧化钠固体常因吸收空气中的二氧化碳而变质.某研究性学习小组为探究氢氧化钠固体样品中的碳酸钠的质量分数(仅考虑样品为NaOH和Na2CO3的混合物),设计了多种实验方案,请结合以下方案回答有关问题:
方案一:
称取一定量的氢氧化钠样品,加水溶解后,逐滴加入沉淀剂氢氧化钡溶液至不再产生沉淀为止.将沉淀过滤、洗涤、烘干、称量.
则:(1)沉淀洗涤的目的是________,若不洗涤,则所测定的样品中碳酸钠的质量分数________(填“偏大”、“偏小”或“无影响”).证明沉淀已经洗涤干净的方法:向最后一次洗涤后的滤液中加入________试剂(填化学式),若无沉淀产生,说明洗涤干净.
方案二:
(2)利用下图装置测定氢氧化钠样品中 Na2CO3的质量分数,则必需的数据有:样品质量、反应前 锥形瓶及其中各物质的总质量、________.该方案有误差,请写出引起误差的一个原因:________.
锥形瓶及其中各物质的总质量、________.该方案有误差,请写出引起误差的一个原因:________.
方案三:

(3)操作Ⅰ中加入稀盐酸应过量的原因是________,
操作Ⅱ中需要的仪器有铁架台(含铁圈)、玻璃棒、酒精灯和________,若该方案中样品质量为9.3g,最终称量冷却后的晶体质量为11.7g.
为计算碳酸钠的质量分数,小刚同学通过列二元一次方程组的办法得到两个表达式:
解:设样品中NaOH的质量为x,Na2CO3的质量为y.

请判断这两个方程组中是否存在问题,若有错误,请将纠正后的方程写在横线上:________.
经计算碳酸钠的质量分数为________.(写出计算过程)
查看习题详情和答案>>
氢氧化钠固体常因吸收空气中的二氧化碳而变质.某研究性学习小组为探究氢氧化钠固体样品中的碳酸钠的质量分数(仅考虑样品为NaOH和Na2CO3的混合物),设计了多种实验方案,请结合以下方案回答有关问题:
方案一:
称取一定量的氢氧化钠样品,加水溶解后,逐滴加入沉淀剂氢氧化钡溶液至不再产生沉淀为止.将沉淀过滤、洗涤、烘干、称量.
则:(1)沉淀洗涤的目的是______,若不洗涤,则所测定的样品中碳酸钠的质量分数______(填“偏大”、“偏小”或“无影响”).证明沉淀已经洗涤干净的方法:向最后一次洗涤后的滤液中加入______试剂(填化学式),若无沉淀产生,说明洗涤干净.
方案二:
(2)利用下图装置测定氢氧化钠样品中 Na2CO3的质量分数,则必需的数据有:样品质量、反应前
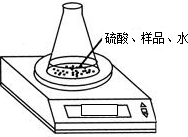
锥形瓶及其中各物质的总质量、______.该方案有误差,请写出引起误差的一个原因:______.
方案三:
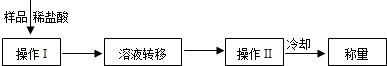
(3)操作Ⅰ中加入稀盐酸应过量的原因是______,
操作Ⅱ中需要的仪器有铁架台(含铁圈)、玻璃棒、酒精灯和______,若该方案中样品质量为9.3g,最终称量冷却后的晶体质量为11.7g.
为计算碳酸钠的质量分数,小刚同学通过列二元一次方程组的办法得到两个表达式:
设样品中NaOH的质量为x,Na2CO3的质量为y.
请判断这两个方程组中是否存在问题,若有错误,请将纠正后的方程写在横线上:______.
经计算碳酸钠的质量分数为______.(写出计算过程)
查看习题详情和答案>>
方案一:
称取一定量的氢氧化钠样品,加水溶解后,逐滴加入沉淀剂氢氧化钡溶液至不再产生沉淀为止.将沉淀过滤、洗涤、烘干、称量.
则:(1)沉淀洗涤的目的是______,若不洗涤,则所测定的样品中碳酸钠的质量分数______(填“偏大”、“偏小”或“无影响”).证明沉淀已经洗涤干净的方法:向最后一次洗涤后的滤液中加入______试剂(填化学式),若无沉淀产生,说明洗涤干净.
方案二:
(2)利用下图装置测定氢氧化钠样品中 Na2CO3的质量分数,则必需的数据有:样品质量、反应前

锥形瓶及其中各物质的总质量、______.该方案有误差,请写出引起误差的一个原因:______.
方案三:

(3)操作Ⅰ中加入稀盐酸应过量的原因是______,
操作Ⅱ中需要的仪器有铁架台(含铁圈)、玻璃棒、酒精灯和______,若该方案中样品质量为9.3g,最终称量冷却后的晶体质量为11.7g.
为计算碳酸钠的质量分数,小刚同学通过列二元一次方程组的办法得到两个表达式:
设样品中NaOH的质量为x,Na2CO3的质量为y.
|
请判断这两个方程组中是否存在问题,若有错误,请将纠正后的方程写在横线上:______.
经计算碳酸钠的质量分数为______.(写出计算过程)
氢氧化钠固体常因吸收空气中的二氧化碳而变质.某研究性学习小组为探究氢氧化钠固体样品中的碳酸钠的质量分数(仅考虑样品为NaOH和Na2CO3的混合物),设计了多种实验方案,请结合以下方案回答有关问题:
方案一:
称取一定量的氢氧化钠样品,加水溶解后,逐滴加入沉淀剂氢氧化钡溶液至不再产生沉淀为止.将沉淀过滤、洗涤、烘干、称量.
则:(1)沉淀洗涤的目的是______,若不洗涤,则所测定的样品中碳酸钠的质量分数______(填“偏大”、“偏小”或“无影响”).证明沉淀已经洗涤干净的方法:向最后一次洗涤后的滤液中加入______试剂(填化学式),若无沉淀产生,说明洗涤干净.
方案二:
(2)利用下图装置测定氢氧化钠样品中 Na2CO3的质量分数,则必需的数据有:样品质量、反应前锥形瓶及其中各物质的总质量、______.该方案有误差,请写出引起误差的一个原因:______.
方案三:
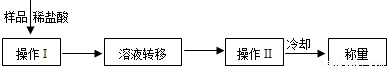
(3)操作Ⅰ中加入稀盐酸应过量的原因是______,
操作Ⅱ中需要的仪器有铁架台(含铁圈)、玻璃棒、酒精灯和______,若该方案中样品质量为9.3g,最终称量冷却后的晶体质量为11.7g.
为计算碳酸钠的质量分数,小刚同学通过列二元一次方程组的办法得到两个表达式:
解:设样品中NaOH的质量为x,Na2CO3的质量为y.
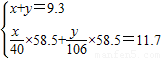
请判断这两个方程组中是否存在问题,若有错误,请将纠正后的方程写在横线上:______.
经计算碳酸钠的质量分数为______.(写出计算过程)
 查看习题详情和答案>>
查看习题详情和答案>>
方案一:
称取一定量的氢氧化钠样品,加水溶解后,逐滴加入沉淀剂氢氧化钡溶液至不再产生沉淀为止.将沉淀过滤、洗涤、烘干、称量.
则:(1)沉淀洗涤的目的是______,若不洗涤,则所测定的样品中碳酸钠的质量分数______(填“偏大”、“偏小”或“无影响”).证明沉淀已经洗涤干净的方法:向最后一次洗涤后的滤液中加入______试剂(填化学式),若无沉淀产生,说明洗涤干净.
方案二:
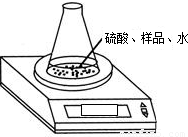
(2)利用下图装置测定氢氧化钠样品中 Na2CO3的质量分数,则必需的数据有:样品质量、反应前锥形瓶及其中各物质的总质量、______.该方案有误差,请写出引起误差的一个原因:______.
方案三:

(3)操作Ⅰ中加入稀盐酸应过量的原因是______,
操作Ⅱ中需要的仪器有铁架台(含铁圈)、玻璃棒、酒精灯和______,若该方案中样品质量为9.3g,最终称量冷却后的晶体质量为11.7g.
为计算碳酸钠的质量分数,小刚同学通过列二元一次方程组的办法得到两个表达式:
解:设样品中NaOH的质量为x,Na2CO3的质量为y.
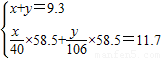
请判断这两个方程组中是否存在问题,若有错误,请将纠正后的方程写在横线上:______.
经计算碳酸钠的质量分数为______.(写出计算过程)
 查看习题详情和答案>>
查看习题详情和答案>>
氢氧化钠固体常因吸收空气中的二氧化碳而变质.某研究性学习小组为探究氢氧化钠固体样品中的碳酸钠的质量分数(仅考虑样品为NaOH和Na2CO3的混合物),设计了多种实验方案,请结合以下方案回答有关问题:
方案一:
称取一定量的氢氧化钠样品,加水溶解后,逐滴加入沉淀剂氢氧化钡溶液至不再产生沉淀为止.将沉淀过滤、洗涤、烘干、称量.
则:(1)沉淀洗涤的目的是______,若不洗涤,则所测定的样品中碳酸钠的质量分数______(填“偏大”、“偏小”或“无影响”).证明沉淀已经洗涤干净的方法:向最后一次洗涤后的滤液中加入______试剂(填化学式),若无沉淀产生,说明洗涤干净.
方案二:
(2)利用下图装置测定氢氧化钠样品中 Na2CO3的质量分数,则必需的数据有:样品质量、反应前锥形瓶及其中各物质的总质量、______.该方案有误差,请写出引起误差的一个原因:______.
方案三:

(3)操作Ⅰ中加入稀盐酸应过量的原因是______,
操作Ⅱ中需要的仪器有铁架台(含铁圈)、玻璃棒、酒精灯和______,若该方案中样品质量为9.3g,最终称量冷却后的晶体质量为11.7g.
为计算碳酸钠的质量分数,小刚同学通过列二元一次方程组的办法得到两个表达式:
解:设样品中NaOH的质量为x,Na2CO3的质量为y.

请判断这两个方程组中是否存在问题,若有错误,请将纠正后的方程写在横线上:______.
经计算碳酸钠的质量分数为______.(写出计算过程)
 查看习题详情和答案>>
查看习题详情和答案>>
方案一:
称取一定量的氢氧化钠样品,加水溶解后,逐滴加入沉淀剂氢氧化钡溶液至不再产生沉淀为止.将沉淀过滤、洗涤、烘干、称量.
则:(1)沉淀洗涤的目的是______,若不洗涤,则所测定的样品中碳酸钠的质量分数______(填“偏大”、“偏小”或“无影响”).证明沉淀已经洗涤干净的方法:向最后一次洗涤后的滤液中加入______试剂(填化学式),若无沉淀产生,说明洗涤干净.
方案二:
(2)利用下图装置测定氢氧化钠样品中 Na2CO3的质量分数,则必需的数据有:样品质量、反应前锥形瓶及其中各物质的总质量、______.该方案有误差,请写出引起误差的一个原因:______.
方案三:

(3)操作Ⅰ中加入稀盐酸应过量的原因是______,
操作Ⅱ中需要的仪器有铁架台(含铁圈)、玻璃棒、酒精灯和______,若该方案中样品质量为9.3g,最终称量冷却后的晶体质量为11.7g.
为计算碳酸钠的质量分数,小刚同学通过列二元一次方程组的办法得到两个表达式:
解:设样品中NaOH的质量为x,Na2CO3的质量为y.

请判断这两个方程组中是否存在问题,若有错误,请将纠正后的方程写在横线上:______.
经计算碳酸钠的质量分数为______.(写出计算过程)
 查看习题详情和答案>>
查看习题详情和答案>>