网址:http://m.1010jiajiao.com/timu_id_902204[举报]
在金属活动性顺序里,钠位于铜之前。某化学兴趣小组发现,将钠投入硫酸铜溶液中,产生无色气体和蓝色沉淀,却未置换出红色的铜。该小组同学对此现象进行了如下探究:
【查阅资料】钠的化学性质非常活泼,常温下就能被空气中的氧气氧化,且能与水迅速反应。
【分析与讨论】
(1)在实验室中通常将钠保存在煤油里,煤油的作用是 。
(2)已知:在一个化学反应中,如果有元素化合价的升高,同时就有元素化合价降低。对于钠与水反应的生成物,甲同学猜想是NaOH和H2,乙同学猜想是NaOH和O2,你认为 同学的猜想不合理,请从化合价的角度解释原因: 。
【进行实验】该小组同学通过实验验证钠与水反应的产物,装置如下图: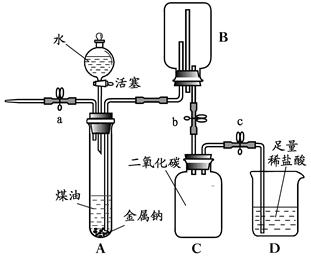
注:煤油的密度为0.8g/mL,与水不互溶。
| | 实验操作 | 实验现象及分析 |
| ① | 打开止水夹a及分液漏斗活塞,待液体充满大试管后,关闭止水夹a及分液漏斗活塞。 | 实验现象为:液体分层,钠熔成银白色小球,在液体分层的界面上跳动,产生大量气泡,下层液体逐渐被压入B中。 钠的物理性质有: (任写两条)。 |
| ② | 打开止水夹b,待B中部分液体进入C中,迅速关闭止水夹b。 | 发生反应的化学方程式为: 。 |
| ③ | 打开止水夹c。 | 实验现象为:D中液体 ,C中产生气泡。 |
| ④ | 打开止水夹a,通过分液漏斗向大试管中逐滴加水,将燃着的木条伸至装置左端尖嘴导管口。 | 实验现象为:气体燃烧,产生 色火焰。 |
| ⑤ | 在火焰上方罩一个干冷的烧杯。 | 实验现象为:烧杯内壁出现 。 |
在金属活动性顺序里,钠位于铜之前。某化学兴趣小组发现,将钠投入硫酸铜溶液中,产生无色气体和蓝色沉淀,却未置换出红色的铜。该小组同学对此现象进行了如下探究:
【查阅资料】钠的化学性质非常活泼,常温下就能被空气中的氧气氧化,且能与水迅速反应。
【分析与讨论】
(1)在实验室中通常将钠保存在煤油里,煤油的作用是 。
(2)已知:在一个化学反应中,如果有元素化合价的升高,同时就有元素化合价降低。对于钠与水反应的生成物,甲同学猜想是NaOH和H2,乙同学猜想是NaOH和O2,你认为 同学的猜想不合理,请从化合价的角度解释原因: 。
【进行实验】该小组同学通过实验验证钠与水反应的产物,装置如下图:
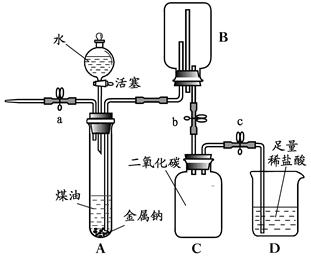
注:煤油的密度为0.8g/mL,与水不互溶。
|
|
实验操作 |
实验现象及分析 |
|
① |
打开止水夹a及分液漏斗活塞,待液体充满大试管后,关闭止水夹a及分液漏斗活塞。 |
实验现象为:液体分层,钠熔成银白色小球,在液体分层的界面上跳动,产生大量气泡,下层液体逐渐被压入B中。 钠的物理性质有: (任写两条)。 |
|
② |
打开止水夹b,待B中部分液体进入C中,迅速关闭止水夹b。 |
发生反应的化学方程式为: 。 |
|
③ |
打开止水夹c。 |
实验现象为:D中液体 ,C中产生气泡。 |
|
④ |
打开止水夹a,通过分液漏斗向大试管中逐滴加水,将燃着的木条伸至装置左端尖嘴导管口。 |
实验现象为:气体燃烧,产生 色火焰。 |
|
⑤ |
在火焰上方罩一个干冷的烧杯。 |
实验现象为:烧杯内壁出现 。 |
【解释与结论】将钠投入硫酸铜溶液中,产生无色气体和蓝色沉淀,写出发生反应的化学方程式(分两步写): , 。
查看习题详情和答案>>
【查阅资料】钠的化学性质非常活泼,常温下就能被空气中的氧气氧化,且能与水迅速反应。
【分析与讨论】
(1)在实验室中通常将钠保存在煤油里,煤油的作用是 。
(2)已知:在一个化学反应中,如果有元素化合价的升高,同时就有元素化合价降低。对于钠与水反应的生成物,甲同学猜想是NaOH和H2,乙同学猜想是NaOH和O2,你认为 同学的猜想不合理,请从化合价的角度解释原因: 。
【进行实验】该小组同学通过实验验证钠与水反应的产物,装置如下图:

注:煤油的密度为0.8g/mL,与水不互溶。
| | 实验操作 | 实验现象及分析 |
| ① | 打开止水夹a及分液漏斗活塞,待液体充满大试管后,关闭止水夹a及分液漏斗活塞。 | 实验现象为:液体分层,钠熔成银白色小球,在液体分层的界面上跳动,产生大量气泡,下层液体逐渐被压入B中。 钠的物理性质有: (任写两条)。 |
| ② | 打开止水夹b,待B中部分液体进入C中,迅速关闭止水夹b。 | 发生反应的化学方程式为: 。 |
| ③ | 打开止水夹c。 | 实验现象为:D中液体 ,C中产生气泡。 |
| ④ | 打开止水夹a,通过分液漏斗向大试管中逐滴加水,将燃着的木条伸至装置左端尖嘴导管口。 | 实验现象为:气体燃烧,产生 色火焰。 |
| ⑤ | 在火焰上方罩一个干冷的烧杯。 | 实验现象为:烧杯内壁出现 。 |

[提出问题]为何钠不能置换出硫酸铜溶液里的铜呢?为何会出现蓝色絮状沉淀?
[猜想假设]查阅资料可知,钠可能先与盐溶液中的水发生反应,然后再与硫酸铜发生反应.
[设计实验]
①先切一小块钠(绿豆大),用刺了小孔的铝箔包好;
②用镊子夹住,放在图中的试管口下(试管已装满水);
③等试管集满气体时,用大拇指堵住试管口并从溶液中取出,移近酒精灯点燃;
④最后向烧杯中滴加无色的酚酞试液.
[实验现象]反应过程中,有气泡逸出;试管中的气体点燃时能听到轻微的爆鸣声;滴加酚酞溶液后,镕液呈红色.
[实验结论]金属钠与水反应,生成了氢气和氢氧化钠.
[进一步推论]将实验与老师的演示实验相比较,可推理出钠与硫酸铜反应时确实是由钠与水先反应,然后生成的氢氧化钠与硫酸铜产生了蓝色絮状沉淀.
根据以上实验过程,回答下列问题:
(1)请根据张老师的演示实验现象,归纳金属钠的物理性质______(至少答两点);
(2)钠粒用刺了小孔的铝箔包好,并用镊子夹住的目的是:______;
(3)金属钠与水反应生成的气体应该是氢气,而不可能是甲烷或者一氧化碳,理由是______;
(4)请写出硫酸铜与氢氧化钠反应的化学方程式:______;
(5)根据实验结论,有同学认为实验步骤③中有不符合安全要求的操作,你能找出来么?______.
查看习题详情和答案>>
 27、在金属活动性顺序中,活动性较强的金属一般可以将位于其后面的金属从它们的盐溶液中置换出来.张老师在做钠与硫酸铜溶液反应的演示实验时,观察到的现象是:钠块在液面上很快融成一个银白色小球,并四处游动,溶液中出现蓝色絮状沉淀,小球很快停在絮状沉淀集中处燃烧起来,并伴随有轻微的爆炸声,却始终没有发现在钠表面有红色固体析出.对此,同学们展开了如下探究:
27、在金属活动性顺序中,活动性较强的金属一般可以将位于其后面的金属从它们的盐溶液中置换出来.张老师在做钠与硫酸铜溶液反应的演示实验时,观察到的现象是:钠块在液面上很快融成一个银白色小球,并四处游动,溶液中出现蓝色絮状沉淀,小球很快停在絮状沉淀集中处燃烧起来,并伴随有轻微的爆炸声,却始终没有发现在钠表面有红色固体析出.对此,同学们展开了如下探究:[提出问题]为何钠不能置换出硫酸铜溶液里的铜呢?为何会出现蓝色絮状沉淀?
[猜想假设]查阅资料可知,钠可能先与盐溶液中的水发生反应,然后再与硫酸铜发生反应.
[设计实验]
①先切一小块钠(绿豆大),用刺了小孔的铝箔包好;
②用镊子夹住,放在图中的试管口下(试管已装满水);
③等试管集满气体时,用大拇指堵住试管口并从溶液中取出,移近酒精灯点燃;
④最后向烧杯中滴加无色的酚酞试液.
[实验现象]反应过程中,有气泡逸出;试管中的气体点燃时能听到轻微的爆鸣声;滴加酚酞溶液后,镕液呈红色.
[实验结论]金属钠与水反应,生成了氢气和氢氧化钠.
[进一步推论]将实验与老师的演示实验相比较,可推理出钠与硫酸铜反应时确实是由钠与水先反应,然后生成的氢氧化钠与硫酸铜产生了蓝色絮状沉淀.
根据以上实验过程,回答下列问题:
(1)请根据张老师的演示实验现象,归纳金属钠的物理性质
(2)钠粒用刺了小孔的铝箔包好,并用镊子夹住的目的是:
(3)金属钠与水反应生成的气体应该是氢气,而不可能是甲烷或者一氧化碳,理由是
(4)请写出硫酸铜与氢氧化钠反应的化学方程式:
(5)根据实验结论,有同学认为实验步骤③中有不符合安全要求的操作,你能找出来么?