摘要:(1)若A在常温下是一种无色液体.且D是CuO.则A的化学式为 .写出化学反应方程式:A→B ,B→D (2)若A在常温下是一种不溶于水的白色固体.且C是形成温室效应的主要气体之一.则:A的化学式为 .写出化学反应方程式:A→B .
网址:http://m.1010jiajiao.com/timu_id_897287[举报]
被称为“绿色氧化剂”的过氧化氢(H2O2),俗称双氧水,是一种无色液体,常用作氧化剂、消毒杀菌剂和漂白剂等.在较低温度下和少量催化剂(如MnO2)条件下,它能迅速分解,生成氧气和水.
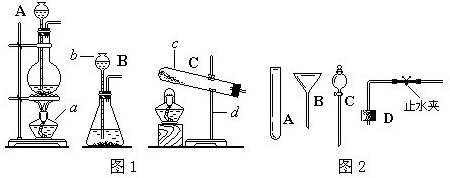
请回答下列问题:
(1)写出图1中标号仪器的名称:a
(2)若实验室用过氧化氢代替氯酸钾制取氧气,可采用上面的哪种发生装置?(填序号),主要理由是
(3)当过氧化氢接触二氧化锰后,反应便立即开始并不能人为控制其速度.如果稍改变你所选择的装置,便可控制其反应的速度.请从图2的仪器中选择一种仪器更换你选择的装置中的一种仪器,以达到控制反应速度的目的.你选择的仪器是
查看习题详情和答案>>

请回答下列问题:
(1)写出图1中标号仪器的名称:a
酒精灯
酒精灯
b长颈漏斗
长颈漏斗
c试管
试管
d铁架台
铁架台
.(2)若实验室用过氧化氢代替氯酸钾制取氧气,可采用上面的哪种发生装置?(填序号),主要理由是
B;因为反应物是过氧化氢,二氧化锰作催化剂,且不需加热,属于固液常温制取气体
B;因为反应物是过氧化氢,二氧化锰作催化剂,且不需加热,属于固液常温制取气体
.(3)当过氧化氢接触二氧化锰后,反应便立即开始并不能人为控制其速度.如果稍改变你所选择的装置,便可控制其反应的速度.请从图2的仪器中选择一种仪器更换你选择的装置中的一种仪器,以达到控制反应速度的目的.你选择的仪器是
C
C
(填序号),它更换原装置中的.控制反应速度的原理是分液漏斗可通过逐滴滴加过氧化氢溶液,控制液体的滴加速度,从而控制反应速率
分液漏斗可通过逐滴滴加过氧化氢溶液,控制液体的滴加速度,从而控制反应速率
.利用下面提供的仪器或装置完成实验室制取气体的实践与研究.
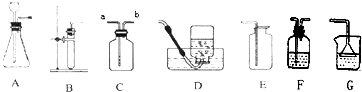
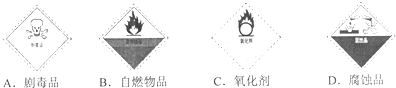
(1)过氧化氢是一种无色透明的无毒液体,过氧化氢溶液俗称“双氧水”,具有强氧化性.贮运过氧化氢的试剂箱上最适合粘贴的一张标识是
(2)过氧化氢溶液常用于实验室制取氧气.
①要收集干燥的氧气,整套装置的连接顺序为(由气体发生装置开始)
②加入药品通常采用“把过氧化氢溶液缓缓加入盛有少量MnO2的反应容器中”,优点是
③MnO2可以连续反应使用,理由是
(3)硫化氢(H2S)是一种有毒气体,其密度比空气的密度大,且能溶于水形成氢硫酸.实验室通常用块状固体硫化亚铁(FeS)和稀硫酸混合,在常温下通过发生复分解反应制得硫化氢气体.试回答:
①实验室制取硫化氢的化学反应方程式为:
②制取硫化氢气体的发生装置可以选用
③为了验证硫化氢的水溶液呈酸性,可以将该气体通入装置F,F中所盛的试剂应该是
④做上述实验时,为了防止多余的硫化氢逸出污染环境,可以将其通入装置G吸收,G中的试剂应该为
查看习题详情和答案>>

(1)过氧化氢是一种无色透明的无毒液体,过氧化氢溶液俗称“双氧水”,具有强氧化性.贮运过氧化氢的试剂箱上最适合粘贴的一张标识是
C
C
(从下图中选填字母序号).
(2)过氧化氢溶液常用于实验室制取氧气.
①要收集干燥的氧气,整套装置的连接顺序为(由气体发生装置开始)
AFE或BFE
AFE或BFE
(选填字母A~E);反应的化学方程式为2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
;
| ||
②加入药品通常采用“把过氧化氢溶液缓缓加入盛有少量MnO2的反应容器中”,优点是
能获得平稳的氧气流
能获得平稳的氧气流
;③MnO2可以连续反应使用,理由是
MnO2是催化剂
MnO2是催化剂
;(3)硫化氢(H2S)是一种有毒气体,其密度比空气的密度大,且能溶于水形成氢硫酸.实验室通常用块状固体硫化亚铁(FeS)和稀硫酸混合,在常温下通过发生复分解反应制得硫化氢气体.试回答:
①实验室制取硫化氢的化学反应方程式为:
FeS+H2SO4=FeSO4+H2S↑
FeS+H2SO4=FeSO4+H2S↑
;②制取硫化氢气体的发生装置可以选用
A或B
A或B
,若用C装置收集硫化氢气体,进气口应为a
a
,原因是密度比空气大
密度比空气大
;③为了验证硫化氢的水溶液呈酸性,可以将该气体通入装置F,F中所盛的试剂应该是
紫色石蕊试液
紫色石蕊试液
,现象是变红色
变红色
;④做上述实验时,为了防止多余的硫化氢逸出污染环境,可以将其通入装置G吸收,G中的试剂应该为
氢氧化钠溶液
氢氧化钠溶液
.利用下面提供的仪器或装置完成实验室制取气体的实践与研究.

(1)过氧化氢是一种无色透明的无毒液体,过氧化氢溶液俗称“双氧水”,具有强氧化性.贮运过氧化氢的试剂箱上最适合粘贴的一张标识是________(从下图中选填字母序号).
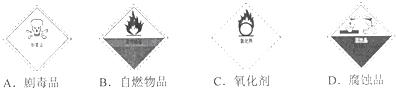
(2)过氧化氢溶液常用于实验室制取氧气.
①要收集干燥的氧气,整套装置的连接顺序为(由气体发生装置开始)________(选填字母A~E);反应的化学方程式为________;
②加入药品通常采用“把过氧化氢溶液缓缓加入盛有少量MnO2的反应容器中”,优点是________;
③MnO2可以连续反应使用,理由是________;
(3)硫化氢(H2S)是一种有毒气体,其密度比空气的密度大,且能溶于水形成氢硫酸.实验室通常用块状固体硫化亚铁(FeS)和稀硫酸混合,在常温下通过发生复分解反应制得硫化氢气体.试回答:
①实验室制取硫化氢的化学反应方程式为:________;
②制取硫化氢气体的发生装置可以选用________,若用C装置收集硫化氢气体,进气口应为________,原因是________;
③为了验证硫化氢的水溶液呈酸性,可以将该气体通入装置F,F中所盛的试剂应该是________,现象是________;
④做上述实验时,为了防止多余的硫化氢逸出污染环境,可以将其通入装置G吸收,G中的试剂应该为________.
查看习题详情和答案>>
某化学活动兴趣小组的同学进行木炭还原CuO的探究实验,生成物是红色固体和无色气体.他们查阅资料后得知氧化亚铜(Cu2O)为红色固体,猜测反应物比例不同,产物也会不同.因此,生成物中有CO2、CO和Cu,固体还可能有Cu2O.又知Cu2O能和常见的酸(HNO3除外)反应生成Cu2+和Cu.为此,请你和他们一起进行如下探究.
(1)探究气体中是否有CO气体.甲同学设计的方案是:先将气体通过足量的NaOH溶液,干燥后再通过灼热的CuO,未反应完的气体直接排放到空气中.
①甲同学实验后如果有 色固体生成,说明一定含有CO气体;
②上述实验方案中可选用的一种气体干燥剂是 ;
③甲同学设计的实验方案有无不足之处?若有,请你指出有何不良后果,并提出改进方案;若没有,该问不需作答. .
(2)探究红色固体中是否有Cu2O.
①在如下方法中:a.上网查询 b.实验 c.请教老师
你认为最能解决实际问题的方法是 (填字母序号).
②请你设计一个简便的实验方案,检验红色固体中是否有Cu2O.
(3)为探究红色固体产物的组成及质量分数,兴趣小组的同学另取一份CuO与木炭组成的混合物8.48g,高温下充分反应后,剩余固体呈红色(氧化铜全部被还原),其质量为6.72g,且反应后产生的气体能全部被足量的澄清石灰水吸收,将所得的沉淀过滤、洗涤、干燥、称量得4.00g.请通过计算帮助他们分析固体产物的组成及质量分数.
查看习题详情和答案>>
(1)探究气体中是否有CO气体.甲同学设计的方案是:先将气体通过足量的NaOH溶液,干燥后再通过灼热的CuO,未反应完的气体直接排放到空气中.
①甲同学实验后如果有
②上述实验方案中可选用的一种气体干燥剂是
③甲同学设计的实验方案有无不足之处?若有,请你指出有何不良后果,并提出改进方案;若没有,该问不需作答.
(2)探究红色固体中是否有Cu2O.
①在如下方法中:a.上网查询 b.实验 c.请教老师
你认为最能解决实际问题的方法是
②请你设计一个简便的实验方案,检验红色固体中是否有Cu2O.
| 实验步骤 | |
| 实验现象与结论 | |
| 化学反应方程式 |
某化学活动兴趣小组的同学进行木炭还原CuO的探究实验,生成物是红色固体和无色气体.他们查阅资料后得知氧化亚铜(Cu2O)为红色固体,猜测反应物比例不同,产物也会不同.因此,生成物中有CO2、CO和Cu,固体还可能有Cu2O.又知Cu2O能和常见的酸(HNO3除外)反应生成Cu2+和Cu.为此,请你和他们一起进行如下探究.
(1)探究气体中是否有CO气体.甲同学设计的方案是:先将气体通过足量的NaOH溶液,干燥后再通过灼热的CuO,未反应完的气体直接排放到空气中.
①甲同学实验后如果有________色固体生成,说明一定含有CO气体;
②上述实验方案中可选用的一种气体干燥剂是________;
③甲同学设计的实验方案有无不足之处?若有,请你指出有何不良后果,并提出改进方案;若没有,该问不需作答.________.
(2)探究红色固体中是否有Cu2O.
①在如下方法中:a.上网查询 b.实验 c.请教老师
你认为最能解决实际问题的方法是________(填字母序号).
②请你设计一个简便的实验方案,检验红色固体中是否有Cu2O.
| 实验步骤 | ________ |
| 实验现象与结论 | ________ |
| 化学反应方程式 | ________ |