摘要:A.碳酸钠和稀硫酸制取二氧化碳 B.锌粉和稀硫酸制取氢气 C.铁粉和稀硫酸制取氢气 D.大理石和稀硫酸制取二氧化碳
网址:http://m.1010jiajiao.com/timu_id_895380[举报]
二氧化碳是一种奇妙的气体,在实验室可以很方便的制取.

(1)实验室经常选用稀盐酸和
(2)组装好仪器后,将导管末端浸末在水中,用手捂试管,发现导管口有气泡,放手后,会
(3)用排空法收集二氧化碳,验满时可用
(4)甲同学现用某浓盐酸与石灰石制得的二氧化碳通入澄清石灰水中,则澄清石灰水
(5)要除去收集到的二氧化碳中混有的少量氯化氢气体,最好用
(6)测出该废液pH<7,则废液中大量存在的阳离子为
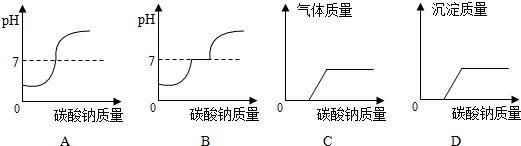
(7)向此废液滴加碳酸钠溶液至过量,则下图表示正确的为
查看习题详情和答案>>

(1)实验室经常选用稀盐酸和
大理石或石灰石
大理石或石灰石
作为反应物,发生装置可选用如上图中的B
B
(填字母),化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
;(2)组装好仪器后,将导管末端浸末在水中,用手捂试管,发现导管口有气泡,放手后,会
有水进入导管
有水进入导管
,说明气密性良好;(3)用排空法收集二氧化碳,验满时可用
AC
AC
方法(填字母)A.燃着木条 B.带火星木条 C.沾有澄清石灰水的玻璃棒 D.涂有酚酞的玻璃片;(4)甲同学现用某浓盐酸与石灰石制得的二氧化碳通入澄清石灰水中,则澄清石灰水
不一定
不一定
会变浑浊(填“一定”或“不一定”);(5)要除去收集到的二氧化碳中混有的少量氯化氢气体,最好用
C
C
(填字母)A.氢氧化钠 B.氢氧化钙 C.碳酸氢钠 D.浓硫酸;(6)测出该废液pH<7,则废液中大量存在的阳离子为
Ca2+、H+
Ca2+、H+
;(7)向此废液滴加碳酸钠溶液至过量,则下图表示正确的为
BD
BD
.
二氧化碳是一种奇妙的气体,在实验室可以很方便的制取.

(1)实验室经常选用稀盐酸和______作为反应物,发生装置可选用如上图中的______(填字母),化学方程式为______;
(2)组装好仪器后,将导管末端浸末在水中,用手捂试管,发现导管口有气泡,放手后,会______,说明气密性良好;
(3)用排空法收集二氧化碳,验满时可用______方法(填字母)A.燃着木条 B.带火星木条 C.沾有澄清石灰水的玻璃棒 D.涂有酚酞的玻璃片;
(4)甲同学现用某浓盐酸与石灰石制得的二氧化碳通入澄清石灰水中,则澄清石灰水______会变浑浊(填“一定”或“不一定”);
(5)要除去收集到的二氧化碳中混有的少量氯化氢气体,最好用______(填字母)A.氢氧化钠 B.氢氧化钙 C.碳酸氢钠 D.浓硫酸;
(6)测出该废液pH<7,则废液中大量存在的阳离子为______;
(7)向此废液滴加碳酸钠溶液至过量,则下图表示正确的为______.

查看习题详情和答案>>
碳酸钠,化学式Na2CO3,俗称纯碱.“纯碱中常常会混有少量的氯化钠”.某研究性学习小组以一包纯碱(若有杂质,只考虑为氯化钠)为研究对象,探究该纯碱样品中碳酸钠的含量.请你参与他们的活动.
【小组讨论】
观点Ⅰ:纯碱样品中只含有碳酸钠
观点Ⅱ:纯碱样品是由碳酸钠和少量氯化钠组成的混合物
【实验设计】
甲方案
Ⅰ设计思路:根据样品与石灰水反应生成沉淀碳酸钙的质量,求出碳酸钠的质量,再计算样品中碳酸钠的质量分数.
Ⅱ操作步骤:称取13.25g纯碱样品,加入过量的澄清石灰水,充分搅拌.过滤、洗涤、干燥,得到白色沉淀10.00g
Ⅲ数据处理:请根据上述实验数据,计算该样品中碳酸钠的质量分数.
计算过程:
Ⅳ实验结论: .
乙方案
Ⅰ设计思路:根据样品(质量为a g)与稀硫酸完全反应生成二氧化碳的质量(质量为b g),求出碳酸钠的质量,再计算样品中碳酸钠的质量分数.
Ⅱ实验结论:
(1)当a、b的质量关系满足 (填写含a、b字母的表达式,下同)时,纯碱样品中只含有碳酸钠,样品中碳酸钠的质量分数是100%.
(2)当a、b的质量关系满足 时,纯碱样品是由碳酸钠和少量氯化钠组成的混合物,样品中碳酸钠的质量分数是 .
【实验评价】
误差分析:(1)甲方案中,白色沉淀的质量在过滤、干燥等操作过程中会有所损耗,造成计算结果与实际值相比偏小.
(2)乙方案中,有部分生成的二氧化碳气体因溶解于水而没有全部逸出,造成计算结果与实际值相比 (填写“偏大”、“偏小”或“不变”).
【交流反思】
(1)实验过程中,需用玻璃棒不断搅拌,该操作的目的是 .
(2)甲方案实验操作中,对沉淀洗涤的目的是: .
(3)乙方案中,需用一定质量的19.6%的稀硫酸.现有一瓶98%的浓硫酸(密度为1.84g/cm3),配制乙方案中实验所用稀硫酸,至少需要浓硫酸的体积是 mL(填写含字母的表达式).浓硫酸稀释的正确操作是 .
查看习题详情和答案>>
【小组讨论】
观点Ⅰ:纯碱样品中只含有碳酸钠
观点Ⅱ:纯碱样品是由碳酸钠和少量氯化钠组成的混合物
【实验设计】
甲方案
Ⅰ设计思路:根据样品与石灰水反应生成沉淀碳酸钙的质量,求出碳酸钠的质量,再计算样品中碳酸钠的质量分数.
Ⅱ操作步骤:称取13.25g纯碱样品,加入过量的澄清石灰水,充分搅拌.过滤、洗涤、干燥,得到白色沉淀10.00g
Ⅲ数据处理:请根据上述实验数据,计算该样品中碳酸钠的质量分数.
计算过程:
Ⅳ实验结论:
乙方案
Ⅰ设计思路:根据样品(质量为a g)与稀硫酸完全反应生成二氧化碳的质量(质量为b g),求出碳酸钠的质量,再计算样品中碳酸钠的质量分数.
Ⅱ实验结论:
(1)当a、b的质量关系满足
(2)当a、b的质量关系满足
【实验评价】
误差分析:(1)甲方案中,白色沉淀的质量在过滤、干燥等操作过程中会有所损耗,造成计算结果与实际值相比偏小.
(2)乙方案中,有部分生成的二氧化碳气体因溶解于水而没有全部逸出,造成计算结果与实际值相比
【交流反思】
(1)实验过程中,需用玻璃棒不断搅拌,该操作的目的是
(2)甲方案实验操作中,对沉淀洗涤的目的是:
(3)乙方案中,需用一定质量的19.6%的稀硫酸.现有一瓶98%的浓硫酸(密度为1.84g/cm3),配制乙方案中实验所用稀硫酸,至少需要浓硫酸的体积是