摘要:3.实验室用一定量的过氧化氢和二氧化锰制氧气.反应前后二氧化锰的质量A.不变 B.变小 C.变大 D.不能确定
网址:http://m.1010jiajiao.com/timu_id_893726[举报]
实验室用一定质量分数的过氧化氢溶液50 g和2 g二氧化锰混合反应,完全反应后称得剩余物的质量为48.8 g,则反应中放出氧气的质量是
- A.1.2 g
- B.1.6 g
- C.2 g
- D.3.2 g
实验室用一定质量分数的过氧化氢溶液50 g和2 g二氧化锰混合反应,完全反应后称得剩余物的质量为48.8 g,则反应中放出氧气的质量是
[ ]
A.1.2 g
B.1.6 g
C.2 g
D.3.2 g
实验室用食盐制纯碱的操作步骤是:(1)向浓氨水中加入足量食盐晶体制取饱和氨盐水; (2)向饱和氨盐水中通入足量的二氧化碳气体至有大量晶体析出; (3)将操作(2)中产生的晶体过滤出来;(4)将滤纸上的晶体转移至坩埚中,加热至不再有水蒸气产生,所得固体即为碳酸钠.对上述信息的有关理解中,正确的是( )
查看习题详情和答案>>
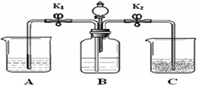 实验室用下图装置进行碳酸钠的性质实验,烧杯A中是澄清石灰水并滴加了酚酞,C中是石灰乳.实验开始前,称取10.6g纯碱置于B中,关闭开关K1打开K2,并加入一定量的稀硫酸.
实验室用下图装置进行碳酸钠的性质实验,烧杯A中是澄清石灰水并滴加了酚酞,C中是石灰乳.实验开始前,称取10.6g纯碱置于B中,关闭开关K1打开K2,并加入一定量的稀硫酸.①烧杯C中并没有明显现象,为了证明B中的确产生了CO2,现将C中悬浊液进行固液分离,过滤后滤液能使酚酞试液变红,则滤液中的主要溶质是
氢氧化钙
氢氧化钙
,该现象不能
不能
(填写“能”或“不能”)说明产生了CO2.②上述过滤后的滤渣可能存在Ca(OH)2和CaCO3.某同学为证明该两种物质同时存在,在一支试管中取少量样品,经过两个步骤完成了检验.若所有检验实验均在该支试管中进行,请完成实验报告:
| 实验步骤 | 所用的试剂或检验方法 | 结 论 |
| 步骤一 | 取样滴加酚酞试液,溶液变红 取样滴加酚酞试液,溶液变红 |
证明 含Ca(OH)2存在 |
| 步骤二 | 继续滴加盐酸,有气泡产生 继续滴加盐酸,有气泡产生 |
证明 CaCO3 CaCO3 存在 |
| 预测的反应现象 | B中反应后,溶液中溶质的化学式 | 烧杯A中发生的主要反应的化学方程式 |
| A中溶液产生大量的白色沉淀产生,红色不褪去. | Na2CO3、Na2SO4 Na2CO3、Na2SO4 |
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH Na2CO3+Ca(OH)2=CaCO3↓+2NaOH |