网址:http://m.1010jiajiao.com/timu_id_889982[举报]
除去粗盐中的少量泥沙,第一步操作是溶解。溶解时应在_____(填一种仪器名称)里进行;第二步操作是对制成的液体进行_____;第三步操作是将滤液加热蒸发,待蒸发皿中出现_____固体时应熄灭酒精灯。在三步操作中都用到玻璃棒,玻璃样作用分别是:
①_____________________;②_________________;③__________________________;
查看习题详情和答案>>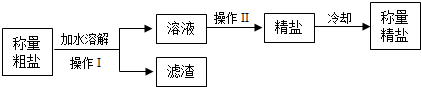
①操作Ⅰ的名称是
②已知产率=
| m(精盐) |
| m(粗盐) |
| 组别 | 1 | 2 | 3 | 4 |
| 产率 | 75% | 65% | 88% | 72% |
| 教师对产率的评价 | 偏低 | 偏低 | 偏高 | 偏低 |
A.第1组:烧杯里的食盐未溶解完就开始过滤.
B.第2组:没有蒸发干,精盐中仍然有水分.
C.第3组:过滤时滤液高于滤纸的边缘.
D.第4组:滤液中还有少量泥沙就开始蒸发.
③若现有50克10%的食盐溶液欲配制成5%的食盐溶液,则需加水
除去粗盐中不溶性杂质,制成精盐的操作流程如下:
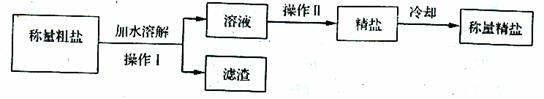 ①操作Ⅰ的名称是 (9) ,溶液中进一步分离获得精盐操作Ⅱ的名称是 (10)
①操作Ⅰ的名称是 (9) ,溶液中进一步分离获得精盐操作Ⅱ的名称是 (10)
②已知产率= ×100%。各小组的产率及评价如下:
×100%。各小组的产率及评价如下:
| 组别 | 1 | 2 | 3 | 4 |
| 产率 | 75% | 65% | 88% | 72% |
| 教师对产率的评价 | 偏低 | 偏低 | 偏高 | 偏低 |
下列各组同学对造成产率偏高或偏低的原因进行分析,其中正确的是 (11) 。
A.第1组:烧杯里的食盐未溶解完就开始过滤。
B.第2组:没有蒸发干,精盐中仍然有水分。
 C.第3组:过滤时滤液高于滤纸的边缘。
C.第3组:过滤时滤液高于滤纸的边缘。
D.第4组:滤液中还有少量泥沙就开始蒸发。
③若现有50克10%的食盐溶液欲配制成5%的食盐溶液,则需加水 (12) 克。
查看习题详情和答案>>除去粗盐中不溶性杂质,制成精盐的操作流程如下:
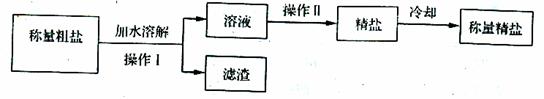
①操作Ⅰ的名称是 (9) ,溶液中进一步分离获得精盐操作Ⅱ的名称是 (10)
②已知产率= ×100%。各小组的产率及评价如下:
×100%。各小组的产率及评价如下:
| 组别 | 1 | 2 | 3 | 4 |
| 产率 | 75% | 65% | 88% | 72% |
| 教师对产率的评价 | 偏低 | 偏低 | 偏高 | 偏低 |
下列各组同学对造成产率偏高或偏低的原因进行分析,其中正确的是 (11) 。
A.第1组:烧杯里的食盐未溶解完就开始过滤。
B.第2组:没有蒸发干,精盐中仍然有水分。
C.第3组:过滤时滤液高于滤纸的边缘。
D.第4组:滤液中还有少量泥沙就开始蒸发。
③若现有50克10%的食盐溶液欲配制成5%的食盐溶液,则需加水 (12) 克。
查看习题详情和答案>>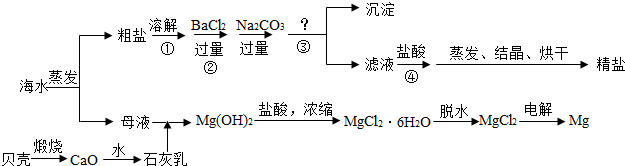
(1)制得粗盐和精盐的操作都包括蒸发步骤,有关其中“蒸发”步骤的叙述错误的是
a.蒸发的目的是得到热饱和溶液b.蒸发的目的是析出晶体
c.应用余热蒸干溶液d.应蒸发至有较多晶体析出时为止
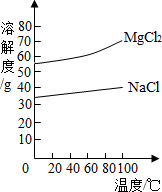
(2)由MgCl2溶液得到MgCl2?6H2O也需要蒸发,根据溶解度曲线,蒸发的目的是
(3)在第①步粗盐溶解操作中要用玻璃棒搅拌,其作用是
(4)该流程的副产品中,除钙元素能被海洋生物利用外,还需综合利用的物质是
(5)MgCl2可电解制Mg,MgO则是重要的耐火材料.
在550℃时,MgCl2?6H2O会分解生成MgO、MgCl2、HCl和水,其中MgO、MgCl2的物质的量之比为3:1,该反应的化学方程式为
(6)电解食盐水所得溶液中的溶质主要为氢氧化钠和氯化钠(其它溶质可忽略不计),已测得该溶液的密度为1.2g/mL,为进一步测定其中氢氧化钠的含量,取该溶液样品25mL与10%的稀硫酸反应,当加入49g稀硫酸时恰好完全中和.请根据化学方程式列式计算:
①25mL该溶液样品中含氢氧化钠多少克?
②该溶液样品中氢氧化钠的质量分数是多少? 查看习题详情和答案>>