网址:http://m.1010jiajiao.com/timu_id_883821[举报]
 某校兴趣小组同学准备进行常见酸、碱、盐的性质实验时,发现实验台上摆放的药品中(如图),有一装溶液的试剂瓶未盖瓶盖且标签破损,于是决定对这瓶溶液进行实验探究:
某校兴趣小组同学准备进行常见酸、碱、盐的性质实验时,发现实验台上摆放的药品中(如图),有一装溶液的试剂瓶未盖瓶盖且标签破损,于是决定对这瓶溶液进行实验探究:【提出问题】这瓶溶液是什么溶液?
【获得信息】酸、碱、盐的性质实验中用到含有钠元素的物质是氯化钠、氢氧化钠、碳酸钠
【提出猜想】这瓶溶液是:
猜想一:氯化钠溶液;
猜想二:氢氧化钠溶液;
猜想三:碳酸钠溶液.
【实验推断】
(1)小丽取样滴加无酚酞试液,溶液呈红色,得出结论:该溶液不可能是
(2)小刚另取样滴加稀盐酸有
(3)小青认为小刚的结论不完全正确,理由是
【继续探究】这瓶溶液中可能含有氢氧化钠,你能设计方案证明吗?
(1)查阅资料:
①酸、碱、盐的性质实验中用到含有钠元素的物质是氯化钠、氢氧化钠、碳酸钠;
②氯化钙溶液呈中性
(2)对这瓶溶液到底是氯化钠、氢氧化钠、碳酸钠中的哪一种,同学们根据现有的药品进行如下实验:
①甲同学取待测液于试管中,滴加无色酚酞试液,溶液呈红色,由此得出结论:该溶液不可能是 溶液,理由是 。
②乙同学另取待测液于试管中,滴加稀盐酸,有 的现象,由此得出结论:该溶液是Na2CO3溶液。
③丙同学认为乙同学的结论不严密,因为NaOH溶液露置在空气中,会与 反应生成Na2CO3,反应的化学方程式为 ,所以这瓶溶液还可能是部分变质的NaOH溶液。
④对这瓶溶液的实际成分,小组同学讨论后,一致认为还需要进行如下实验:

设计步骤Ⅰ的目的是:完全除去溶液中的 ,避免其对 的检验造成干扰。
【实验结论】该溶液是 。
(3)拓展运用:
①做实验时,取用药品后应及时 。
②NaOH溶液与盐酸发生中和反应,是 (选填“吸热”或“放热”)反应。
③除去NaOH溶液中混有的少量Na2CO3溶液,可加入适量的 溶液(填序号)。
A.CaCl2 B.HCl C.Ca(OH)2
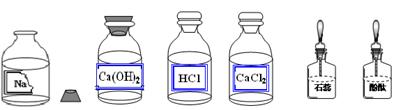
某校兴趣小组同学进行常见酸、碱、盐的性质实验时,发现实验台上摆放的药品中,有一瓶装有溶液的试剂瓶未盖瓶盖且标签破损(如下图),于是决定对这瓶溶液进行探究:

(1)查阅资料:
①酸、碱、盐的性质实验中用到含有钠元素的物质是氯化钠、氢氧化钠、碳酸钠;
②氯化钙溶液呈中性
(2)对这瓶溶液到底是氯化钠、氢氧化钠、碳酸钠中的哪一种,同学们根据现有的药品进行如下实验:
①甲同学取待测液于试管中,滴加无色酚酞试液,溶液呈红色,由此得出结论:该溶液不可能是________溶液,理由是________.
②乙同学另取待测液于试管中,滴加稀盐酸,有________的现象,由此得出结论:该溶液是Na2CO3溶液.
③丙同学认为乙同学的结论不严密,因为NaOH溶液露置在空气中,会与________反应生成Na2CO3,反应的化学方程式为________,所以这瓶溶液还可能是部分变质的NaOH溶液.
④对这瓶溶液的实际成分,小组同学讨论后,一致认为还需要进行如下实验:
设计步骤Ⅰ的目的是:完全除去溶液中的________,避免其对________的检验造成干扰.
[实验结论]该溶液是________.
(3)拓展运用:
①做实验时,取用药品后应及时________.
②NaOH溶液与盐酸发生中和反应,是________(选填“吸热”或“放热”)反应.
③除去NaOH溶液中混有的少量Na2CO3溶液,可加入适量的________溶液(填序号).
A.CaCl2
B.HCl
C.Ca(OH)2
(15分)某校兴趣小组同学进行常见酸、碱、盐的性质实验时,发现实验台上摆放的药品中,有一瓶装有溶液的试剂瓶未盖瓶盖且标签破损(如下图),于是决定对这瓶溶液进行探究:
(1)查阅资料:
①酸、碱、盐的性质实验中用到含有钠元素的物质是氯化钠、氢氧化钠、碳酸钠;
②氯化钙溶液呈中性
(2)对这瓶溶液到底是氯化钠、氢氧化钠、碳酸钠中的哪一种,同学们根据现有的药品进行如下实验:
①甲同学取待测液于试管中,滴加无色酚酞试液,溶液呈红色,由此得出结论:该溶液不可能是 溶液,理由是 。
②乙同学另取待测液于试管中,滴加稀盐酸,有 的现象,由此得出结论:该溶液是Na2CO3溶液。
③丙同学认为乙同学的结论不严密,因为NaOH溶液露置在空气中,会与 反应生成Na2CO3,反应的化学方程式为 ,所以这瓶溶液还可能是部分变质的NaOH溶液。
④对这瓶溶液的实际成分,小组同学讨论后,一致认为还需要进行如下实验:
设计步骤Ⅰ的目的是:完全除去溶液中的 ,避免其对 的检验造成干扰。
【实验结论】该溶液是 。
(3)拓展运用:
①做实验时,取用药品后应及时 。
②NaOH溶液与盐酸发生中和反应,是 (选填“吸热”或“放热”)反应。
③除去NaOH溶液中混有的少量Na2CO3溶液,可加入适量的 溶液(填序号)。
A.CaCl2 B.HCl C.Ca(OH)2
(15分)某校兴趣小组同学进行常见酸、碱、盐的性质实验时,发现实验台上摆放的药品中,有一瓶装有溶液的试剂瓶未盖瓶盖且标签破损(如下图),于是决定对这瓶溶液进行探究:
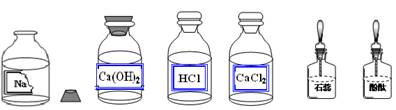
(1)查阅资料:
①酸、碱、盐的性质实验中用到含有钠元素的物质是氯化钠、氢氧化钠、碳酸钠;
②氯化钙溶液呈中性
(2)对这瓶溶液到底是氯化钠、氢氧化钠、碳酸钠中的哪一种,同学们根据现有的药品进行如下实验:
①甲同学取待测液于试管中,滴加无色酚酞试液,溶液呈红色,由此得出结论:该溶液不可能是 溶液,理由是 。
②乙同学另取待测液于试管中,滴加稀盐酸,有 的现象,由此得出结论:该溶液是Na2CO3溶液。
③丙同学认为乙同学的结论不严密,因为NaOH溶液露置在空气中,会与 反应生成Na2CO3,反应的化学方程式为 ,所以这瓶溶液还可能是部分变质的NaOH溶液。
④对这瓶溶液的实际成分,小组同学讨论后,一致认为还需要进行如下实验:

设计步骤Ⅰ的目的是:完全除去溶液中的 ,避免其对 的检验造成干扰。
【实验结论】该溶液是 。
(3)拓展运用:
①做实验时,取用药品后应及时 。
②NaOH溶液与盐酸发生中和反应,是 (选填“吸热”或“放热”)反应。
③除去NaOH溶液中混有的少量Na2CO3溶液,可加入适量的 溶液(填序号)。
A.CaCl2 B.HCl C.Ca(OH)2
查看习题详情和答案>>