摘要:5.在工业炼铁反应 3CO+Fe2O3 2Fe+3CO2中.作氧化剂的是------A.CO B.Fe2O3 C.Fe D.CO2
网址:http://m.1010jiajiao.com/timu_id_883711[举报]
化学反应对人类起着非常重要的作用.请按要求写出有关反应的化学方程式:
(1)以石灰石为原料生产生石灰
(2)工业上以赤铁矿(主要成分Fe2O3)为原料冶炼铁
(3)新制备的灰黑色铁粉暴露在空气中却能迅速燃烧生成红色的三氧化二铁粉末
(4)在汽车排气管上装一个“催化转换器”,可使汽车尾气中的NO和CO反应,生成能参与大气生态循环的两种无毒气体
查看习题详情和答案>>
(1)以石灰石为原料生产生石灰
CaCO3
CaO+CO2↑
| ||
CaCO3
CaO+CO2↑
;
| ||
(2)工业上以赤铁矿(主要成分Fe2O3)为原料冶炼铁
Fe2O3+3CO
2Fe+3CO2
| ||
Fe2O3+3CO
2Fe+3CO2
;
| ||
(3)新制备的灰黑色铁粉暴露在空气中却能迅速燃烧生成红色的三氧化二铁粉末
4Fe+3O2═2Fe2O3
4Fe+3O2═2Fe2O3
;(4)在汽车排气管上装一个“催化转换器”,可使汽车尾气中的NO和CO反应,生成能参与大气生态循环的两种无毒气体
2CO+2NO
2CO2+N2
| ||
2CO+2NO
2CO2+N2
.
| ||
铁的冶炼是钢铁工业的基础.
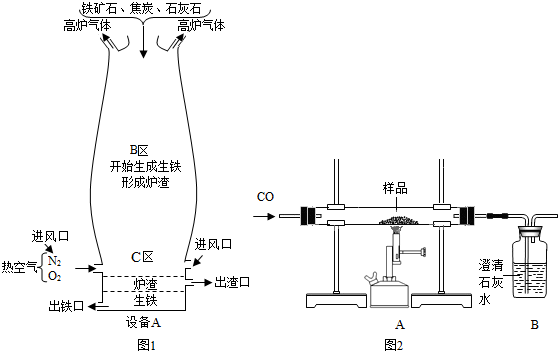
(Ⅰ)如图1是教材中炼铁高炉及炉内化学变化过程示意图,若图中采用的铁矿石的主要成分为氧化铁,请写出B区和C区所发生主要反应的化学方程式:(1)B区
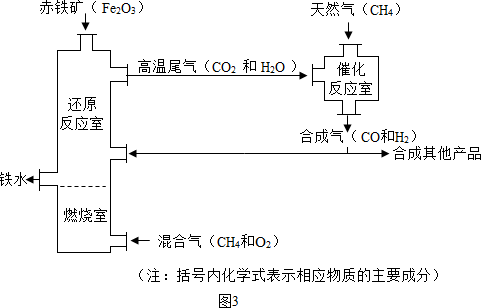
(Ⅱ)竖炉炼铁也是一种重要的炼铁方法,其工艺流程如图2所示.
(3)该工艺流程中,甲烷的作用是
(4)该工艺流程中,可循环利用的物质是
(Ⅲ)金属在活动性顺序里的位置越后,其化合物越不稳定,所以它的氧化物越容易被还原.
(5)请在下列①②中各写一个化学方程式,③中写出还原金属氧化物的方法.

(Ⅳ)某兴趣小组同学利用图3装置进行相关实验,测定样品的组成:
(6)若样品由氧化铁、氧化亚铁和四氧化三铁中的一种或几种组成,待充分反应后,实验数据记录如下:
请回答下列问题:
①兴趣小组同学经过讨论后认为应选用样品质量和装置A中玻璃管和固体的总质量的变化来计算,而不选用装置B的质量的变化来计算,理由是
②该样品所有可能的组成是
查看习题详情和答案>>


(Ⅰ)如图1是教材中炼铁高炉及炉内化学变化过程示意图,若图中采用的铁矿石的主要成分为氧化铁,请写出B区和C区所发生主要反应的化学方程式:(1)B区
3CO+Fe2O3
2Fe+3CO2
| ||
3CO+Fe2O3
2Fe+3CO2
(2)C区
| ||
C+O2
CO2
| ||
C+O2
CO2
、
| ||
2C+CO2
2CO
| ||
2C+CO2
2CO
.
| ||
(Ⅱ)竖炉炼铁也是一种重要的炼铁方法,其工艺流程如图2所示.
(3)该工艺流程中,甲烷的作用是
燃烧产生热量
燃烧产生热量
、做生产合成气的原料
做生产合成气的原料
,冶炼出的铁水属于混合物
混合物
(填“纯净物”或“混合物”).(4)该工艺流程中,可循环利用的物质是
CO2和H2O(高温尾气)
CO2和H2O(高温尾气)
.(Ⅲ)金属在活动性顺序里的位置越后,其化合物越不稳定,所以它的氧化物越容易被还原.
(5)请在下列①②中各写一个化学方程式,③中写出还原金属氧化物的方法.

(Ⅳ)某兴趣小组同学利用图3装置进行相关实验,测定样品的组成:
(6)若样品由氧化铁、氧化亚铁和四氧化三铁中的一种或几种组成,待充分反应后,实验数据记录如下:
| 样品质量 | 装置A中玻璃管和固体的总质量 | 装置B的质量 |
| 2.32g | 反应前55.72g | 反应前 281.00g |
| 反应后55.08g | 反应后 281.56g |
①兴趣小组同学经过讨论后认为应选用样品质量和装置A中玻璃管和固体的总质量的变化来计算,而不选用装置B的质量的变化来计算,理由是
装置B不能将反应产生的CO2全部吸收
装置B不能将反应产生的CO2全部吸收
.②该样品所有可能的组成是
Fe3O4;Fe2O3、FeO;Fe3O4、Fe2O3、FeO
Fe3O4;Fe2O3、FeO;Fe3O4、Fe2O3、FeO
.(2012?海淀区一模)工业上用硫铁矿石(主要成分FeS2)在沸腾炉中焙烧,经过一系列反应,得到硫酸.焙烧后的矿渣用于炼铁.其转化过程如下(部分条件和产物已略去).

请回答下列问题:
(1)如图出现的含硫元素的物质中,属于氧化物的有
(2)FeS2中的铁元素是+2价,硫元素的化合价为
(3)写出②处炼铁的化学方程式
(4)在煤炭燃烧过程中也会产生SO2.工业上将煤燃烧产生的烟气通入吸收塔,用石灰水淋洗,外加氧气的作用,使之反应生成硫酸钙和水.请写出该反应的化学方程式
查看习题详情和答案>>

请回答下列问题:
(1)如图出现的含硫元素的物质中,属于氧化物的有
SO2、SO3
SO2、SO3
(填化学式).(2)FeS2中的铁元素是+2价,硫元素的化合价为
-1
-1
.(3)写出②处炼铁的化学方程式
3CO+Fe2O3
2Fe+3CO2
| ||
3CO+Fe2O3
2Fe+3CO2
.若用2000t含杂质30%的矿渣炼铁,理论上可得到含铁98%的生铁质量为
| ||
1000
1000
t.(4)在煤炭燃烧过程中也会产生SO2.工业上将煤燃烧产生的烟气通入吸收塔,用石灰水淋洗,外加氧气的作用,使之反应生成硫酸钙和水.请写出该反应的化学方程式
2SO2 +2Ca(OH)2 +O2 ═2CaSO4 +2H2O
2SO2 +2Ca(OH)2 +O2 ═2CaSO4 +2H2O
.化学时刻影响着我们的生活,它在工农业生产和日常生活中起到了非常重要的作用.
(1)请选择适当物质的序号填空:①二氧化硫 ②硝酸钾 ③酒精 ④干冰
西南地区持续干旱,能用于人工降雨的是
(2)某些食品包装中有一小袋干燥剂(主要成分为生石灰),它吸收水蒸气的化学方程式
(3)工业上利用一氧化碳与铁矿石(主要成分氧化铁)炼铁.写出其化学反应的方程式
查看习题详情和答案>>
(1)请选择适当物质的序号填空:①二氧化硫 ②硝酸钾 ③酒精 ④干冰
西南地区持续干旱,能用于人工降雨的是
④
④
,常作为复合肥料使用的②
②
.(2)某些食品包装中有一小袋干燥剂(主要成分为生石灰),它吸收水蒸气的化学方程式
CaO+H2O═Ca(OH)2
CaO+H2O═Ca(OH)2
(3)工业上利用一氧化碳与铁矿石(主要成分氧化铁)炼铁.写出其化学反应的方程式
3CO+Fe2O3
2Fe+3CO2
| ||
3CO+Fe2O3
2Fe+3CO2
.
| ||
(2013?常熟市模拟)请写出下列相关的化学反应方程式并完成题后填空:
(1)铁丝在纯净氧气中燃烧
(2)高温下一氧化碳还原氧化铁
(3)稀硫酸除铁锈
(4)氯化铵晶体(NH4Cl)和熟石灰混合研磨生成一种氨臭味的气体:
(5)碳酸氢钠在医学上被用于治疗胃酸过多
查看习题详情和答案>>
(1)铁丝在纯净氧气中燃烧
3Fe+2O2
Fe3O4
| ||
3Fe+2O2
Fe3O4
,完成该实验时,集气瓶底部留有的水的作用是
| ||
防止生成物熔化溅落下来,使瓶底炸裂
防止生成物熔化溅落下来,使瓶底炸裂
;(2)高温下一氧化碳还原氧化铁
Fe2O3+3CO
2Fe+3CO2
| ||
Fe2O3+3CO
2Fe+3CO2
,工业冶炼生铁的设备名称
| ||
高炉
高炉
;(3)稀硫酸除铁锈
Fe2O3+3H2SO4═Fe2(SO4)3+3H2O
Fe2O3+3H2SO4═Fe2(SO4)3+3H2O
,反应后溶液中一定含有的微粒Fe3+、SO42-、H2O
Fe3+、SO42-、H2O
(填符号);(4)氯化铵晶体(NH4Cl)和熟石灰混合研磨生成一种氨臭味的气体:
2NH4Cl+Ca(OH)2═CaCl2+2H2O+2NH3↑
2NH4Cl+Ca(OH)2═CaCl2+2H2O+2NH3↑
,检验该气体可用湿润的红色石蕊
红色石蕊
试纸.(5)碳酸氢钠在医学上被用于治疗胃酸过多
NaHCO3+HCl═NaCl+H2O+CO2↑
NaHCO3+HCl═NaCl+H2O+CO2↑
,该反应的基本类型复分解反应
复分解反应
.