摘要:4.下图所示是二氧化碳的几种用途.其中既利用了它的物理性质.又利用了它的化学性质的是
网址:http://m.1010jiajiao.com/timu_id_883624[举报]
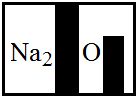 (2013?西华县二模)酸、碱、盐是几类有广泛用途的重要化合物.
(2013?西华县二模)酸、碱、盐是几类有广泛用途的重要化合物.(1)酸和碱在组成和性质方面有很多共同的特点,请任写出其中的一条.
(2)氢氧化钙是一种常见的碱,列举其在生产、生活中的一种用途.
(3)某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如右图)的溶液,他们对此产生了兴趣.
提出问题:这瓶溶液究竟是什么?
经过询问实验老师平时的药品保管得知,这瓶无色溶液应该是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中的某一种.为了确定该药品,他们首先进行了理论分析:
①小明根据标签上的组成元素认为一定不可能是
氯化钠
氯化钠
(提示:只有其中一种).②小英提出,碳酸氢钠、硝酸钠也不可能,你认为她的依据是:
设计实验:为了确定该溶液究竟是剩余两种盐的哪一种,他们设计了如下实验.
| 实验操作 | 实验现象 |
| 取少量样品于试管中,慢慢滴加BaCl2溶液 | 出现白色沉淀 |
| 静置一段时间后,倾去上层清液,向沉淀中滴加稀盐酸 | 白色沉淀全部溶解,并产生大量气泡 |
碳酸钠溶液
碳酸钠溶液
.出现白色沉淀过程的化学方程式是:BaCl2 +Na2CO3═BaCO3↓+2NaCl
BaCl2 +Na2CO3═BaCO3↓+2NaCl
.实验反思:④小强认为上述设计实验还可简化,也能达到目的.小强的实验操作是:
(4)若73 g质量分数为20%的盐酸与127g氢氧化钠溶液恰好完全中和,试计算反应后所得溶液中溶质的质量分数.
Ⅰ下图是初中化学实验室几种常用仪器,请按要求用仪器的序号字母填空.

(1)仪器A的名称叫 ,仪器C的用途是 .
(2)仪器C的注意事项是 .
(3)进行过滤操作时,除了需要用到A、E仪器外,还需用到 ,
(4)使用F仪器称量易潮解的药品时必须放在 .
Ⅱ实验室制取气体所需的装置如下图所示,请回答下列问题:

(1)实验室制取二氧化碳所选用的发生装置为 ;收集装置为 (填装置序号字母).
(2)检查集气瓶中是否已收集满二氧化碳气体的方法是 .
(3)在实验室中,若用A装置制取氧气,需要在试管口放一团 .若用B装置制取氧气的化学方程式为 ;若用E装置收集氧气,当观察至导管口有气泡 地放出时,即可进行收集. 查看习题详情和答案>>

(1)仪器A的名称叫 ,仪器C的用途是 .
(2)仪器C的注意事项是 .
(3)进行过滤操作时,除了需要用到A、E仪器外,还需用到 ,
(4)使用F仪器称量易潮解的药品时必须放在 .
Ⅱ实验室制取气体所需的装置如下图所示,请回答下列问题:

(1)实验室制取二氧化碳所选用的发生装置为 ;收集装置为 (填装置序号字母).
(2)检查集气瓶中是否已收集满二氧化碳气体的方法是 .
(3)在实验室中,若用A装置制取氧气,需要在试管口放一团 .若用B装置制取氧气的化学方程式为 ;若用E装置收集氧气,当观察至导管口有气泡 地放出时,即可进行收集. 查看习题详情和答案>>
Ⅰ下图是初中化学实验室几种常用仪器,请按要求用仪器的序号字母填空.

(1)仪器A的名称叫
(2)仪器C的注意事项是
(3)进行过滤操作时,除了需要用到A、E仪器外,还需用到
(4)使用F仪器称量易潮解的药品时必须放在
Ⅱ实验室制取气体所需的装置如下图所示,请回答下列问题:

(1)实验室制取二氧化碳所选用的发生装置为
(2)检查集气瓶中是否已收集满二氧化碳气体的方法是
(3)在实验室中,若用A装置制取氧气,需要在试管口放一团
查看习题详情和答案>>

(1)仪器A的名称叫
铁架台
铁架台
,仪器C的用途是量度液体体积
量度液体体积
.(2)仪器C的注意事项是
不能作反应容器
不能作反应容器
.(3)进行过滤操作时,除了需要用到A、E仪器外,还需用到
B、D
B、D
,(4)使用F仪器称量易潮解的药品时必须放在
B
B
.Ⅱ实验室制取气体所需的装置如下图所示,请回答下列问题:

(1)实验室制取二氧化碳所选用的发生装置为
B
B
;收集装置为C
C
(填装置序号字母).(2)检查集气瓶中是否已收集满二氧化碳气体的方法是
用一根燃着的木条放在集气瓶口
用一根燃着的木条放在集气瓶口
.(3)在实验室中,若用A装置制取氧气,需要在试管口放一团
棉花
棉花
.若用B装置制取氧气的化学方程式为2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
;若用E装置收集氧气,当观察至导管口有气泡
| ||
连续均匀
连续均匀
地放出时,即可进行收集.23、探究是一种重要的学习方式,是充分理解学科本质的基本途径.请你和化学兴趣小组的同学一起完成下面三个探究实验.
实验一:实验室常用的干燥剂“碱石灰”是CaO和固体NaOH的混合物,极易与空气中水蒸气和CO2反应而变质.兴趣小组的同学对一瓶久置的“碱石灰”作了如下探究:
(1) 猜想
猜想Ⅰ:没有变质,“碱石灰”只含有CaO、固体NaOH;
猜想Ⅱ:已完全变质,“碱石灰”全部变成了CaCO3和Na2CO3.
(2) 实验
如图所示:

(3) 判断
a.若Ca(OH)2、CaCO3和Na2CO3投入到水中不会放热,则由操作②现象判断:猜想Ⅱ
b.操作④发生化学反应的方程式为
c.综合a和b的结论,判断该样品变质情况为
(4) 拓展
由上述实验说明,实验室中“碱石灰”应
实验二:向NaOH溶液中滴入紫色石蕊试液,溶液显蓝色.
(1)提出问题:是什么粒子使紫色石蕊试液变蓝色呢?
(2)查找资料:NaOH溶液中存在的粒子有大量的H2O、Na+、OH-和极少量的H+.
(3)猜想:是大量的OH-使紫色石蕊试液变蓝色.
(4)实验探究步骤及其说明:
①在一支干净试管中加入2mL蒸馏水,再滴入几滴紫色石蕊试液,溶液几乎不变色,说明
②在一支干净试管中加入2mL氯化钠溶液,再滴入几滴紫色石蕊试液,溶液几乎不变色,说明
③在一支干净试管中加入2mL
(5)结论:原假设
实验三:实验室的废液中,可能含有氯化铁、硫酸、氯化钠、碳酸钠和硝酸钡中的一种或多种.化学兴趣小组的同学对废液进行了如下试验:
(1)取废液观察,为无色溶液;
(2)取废液,向其中滴加氯化钡溶液,有白色沉淀产生,继续加入稀硝酸,无明显现象;
(3)另取废液,向其中加入铁粉后,产生大量气泡.
根据以上试验现象可推断,废液中肯定含有
通过实验还不能确定是否含有的物质是

查看习题详情和答案>>
实验一:实验室常用的干燥剂“碱石灰”是CaO和固体NaOH的混合物,极易与空气中水蒸气和CO2反应而变质.兴趣小组的同学对一瓶久置的“碱石灰”作了如下探究:
(1) 猜想
猜想Ⅰ:没有变质,“碱石灰”只含有CaO、固体NaOH;
猜想Ⅱ:已完全变质,“碱石灰”全部变成了CaCO3和Na2CO3.
(2) 实验
如图所示:

(3) 判断
a.若Ca(OH)2、CaCO3和Na2CO3投入到水中不会放热,则由操作②现象判断:猜想Ⅱ
不成立
(填:成立、不成立).b.操作④发生化学反应的方程式为
CaCO3+2HCl═CaCl2+CO2↑+H2O
;由操作⑤⑥的现象判断:滤液中含有Na2CO3
(写化学式);由此判断猜想Ⅰ不成立
(填:成立、不成立).c.综合a和b的结论,判断该样品变质情况为
部分变质
.(4) 拓展
由上述实验说明,实验室中“碱石灰”应
密封
保存.实验二:向NaOH溶液中滴入紫色石蕊试液,溶液显蓝色.
(1)提出问题:是什么粒子使紫色石蕊试液变蓝色呢?
(2)查找资料:NaOH溶液中存在的粒子有大量的H2O、Na+、OH-和极少量的H+.
(3)猜想:是大量的OH-使紫色石蕊试液变蓝色.
(4)实验探究步骤及其说明:
①在一支干净试管中加入2mL蒸馏水,再滴入几滴紫色石蕊试液,溶液几乎不变色,说明
H2O不能使石蕊试液变蓝色
;②在一支干净试管中加入2mL氯化钠溶液,再滴入几滴紫色石蕊试液,溶液几乎不变色,说明
Na+不能使紫色石蕊试液变蓝色
;③在一支干净试管中加入2mL
氢氧化钠
溶液,再滴入几滴紫色石蕊试液,溶液变蓝色,说明OH-能使紫色石蕊试液变蓝色.(5)结论:原假设
成立
.(填“成立”或“不成立”)实验三:实验室的废液中,可能含有氯化铁、硫酸、氯化钠、碳酸钠和硝酸钡中的一种或多种.化学兴趣小组的同学对废液进行了如下试验:
(1)取废液观察,为无色溶液;
(2)取废液,向其中滴加氯化钡溶液,有白色沉淀产生,继续加入稀硝酸,无明显现象;
(3)另取废液,向其中加入铁粉后,产生大量气泡.
根据以上试验现象可推断,废液中肯定含有
硫酸
,肯定不含有氯化铁、碳酸钠、硝酸钡
.通过实验还不能确定是否含有的物质是
氯化钠
.为了确定它是否存在,同学们设计了下面的实验方案,请按同学们的思路填写表:
碳酸氢钠是一种重要的盐类物质,在生活中用途广泛.小滨同学设计了实验,以探究碳酸氢钠的化学性质.
【探究实验1】碳酸氢钠溶液的酸碱性
【实验方案】取少量该固体加入试管中,加适量水溶解,再滴入几滴酚酞实验,震荡.
现象:溶液变成浅红色.由此得出结论 ;
【探究实验2】能与酸反应
【实验方案】取少量该固体加入试管中,滴加稀盐酸,现象为 ;
【探究实验3】碳酸氢钠的热稳定性
【实验方案】用如图所示装置进行实验
现象:充分加热后,大试管口有. 出现,管底有白色固体残留,
小试管中的现象. .
结论:碳酸氢钠受热能生成二氧化碳、水和一种白色固体.
验证:(1)请你帮小滨设计实验,证明试管中留下的白色固体是Na2CO3,而不是NaOH(所选试剂不能用酸).
| 步骤 | 现象 | 结论 |
| 取样于试管中,往试管中滴加 | | |
(2)写出碳酸氢钠受热分解的化学方程式 ;
【拓展应用】试说出碳酸氢钠在日常生活中的一种用途 .
 查看习题详情和答案>>
查看习题详情和答案>>