网址:http://m.1010jiajiao.com/timu_id_882885[举报]
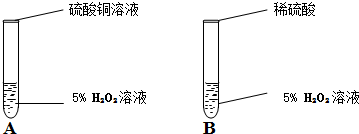
(1)你认为最不可能的是哪一种微粒?
(2)用化学式表示实验A发生的化学反应
| ||
| ||
(3)在实验B中加入稀硫酸(含有H2O、H+、SO42-)后,无明显变化,证明
结论:硫酸铜溶液中,加快双氧水分解速率的微粒是
(4)要验证双氧水分解速率与双氧水的浓度有关,可以进行以下实验:取两套相同装置,其中一套加入5%的双氧水溶液和MnO2,你认为另一套装置所加药品应该是
a.15%的双氧水溶液 b.MnO2 c.5%的双氧水溶液 d.硫酸铜溶液
(5)小东同学注意到试管内只有15%的双氧水时就有少量小气泡浮起,将这支试管浸入约80°C的热水中,气泡明显增多,由此小东认为,双氧水分解速率还与
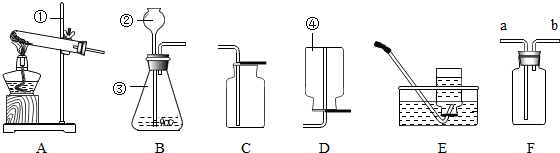
请按要求回答下列问题:
(1)写出带标号的仪器的名称:
①
(2)写出一个在实验室中可用装置A制取氧气的文字表达式或化学方程式:
| ||
| △ |
| ||
| △ |
收集此气体的装置是
(3)如何检查B装置的气密性:
(4)在常温下,用硫化亚铁固体和稀硫酸制取硫化氢气体,应选用的发生装置是
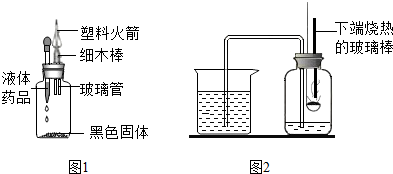
(5)某学生运用了化学反应的原理设计了如图1所示的装置表演趣味化学实验--“发射火箭”.表演时,挤压胶头滴管,套着塑料火箭的轻质细木棒向上冲出,完成发射.细木棒能够向上冲出的原因是:
| ||
| ||
(6)图2是“空气中氧气体积分数测定”实验的改进装置.主要操作是:在实际容积为150mL的集气瓶里,先装进50mL的水,再按图连好仪器,按下热的玻璃棒,白磷立即被点燃.
①白磷从燃烧到熄灭冷却的过程中,瓶内水面的变化是
②集气瓶里预先装进的50mL水,在实验过程中起到哪些作用?
a.加快集气瓶冷却 b.液封导气管末端以防气体逸出 c.缓冲集气瓶内气压的骤然升高.
实验是进行科学探究的重要途径。在探究过程中,很多因素都会对实验结果产生影响。
(1)反应物的浓度不同,反应现象可能不同。请举出实例说明 。
(2)碳在充足的氧气中燃烧生成二氧化碳,在不足的氧气中燃烧生成一氧化碳。对比这两个反应可得到的结论是 。
(3)H2在加热条件下可以与CuO反应,生成Cu和H2O。
①亮亮同学利用下图A装置完成了该实验。
实验步骤:先通入H2,再加热,实验结束后,先撤酒精灯,继续通入H2直至试管冷却。可观察到黑色CuO变成红色。
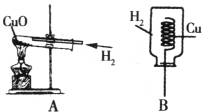
②明明同学利用上图B装置也完成了该实验。
实验步骤:将铜丝在酒精灯外焰上加热变黑后,迅速伸入盛有H2的集气瓶中,片刻可观察到黑色CuO变为红色。
对比A、B两套装置,B装置的优点是 。
③在明明同学的实验中,当铜丝表面生成CuO后,若继续在酒精灯外焰上加热至炽热状态时,则与H2反应较快;若只加热至红热状态时,则反应较慢,甚至没有明显现象。对比这两种情况,可得到的结论是 。
(4)在用废铜屑制取硫酸铜的实验中,有下列两种实验方案可供选择:
甲方案:![]()
乙方案:![]()
![]()
①分别用上述两种方案制取80g硫酸铜,甲方案参加反应的硫酸的质量为98g,请计算乙方案中参加反应的硫酸的质量为多少?
②通过对比这两种实验方案及计算结果,你认为选用哪种方案更好? ;请说明你的理由 。
(5)通过对上述实验的对比与分析可知,探究某一化学问题时,除了应根据具体情况考虑恰当的实验装置外,还应考虑 等因素。
查看习题详情和答案>>某有机物只含C、H两种元素.为了测定它的组成,两位同学分别设计了如图所示的甲、乙两套装置.他们的实验方法是:把一定质量的该有机物在O2中充分燃烧后的产物,按箭头方向缓缓通过各自的装置,根据a、b两瓶在实验前后质量的变化,计算出所生成的水和二氧化碳的质量,从而确定有机物中C、H元素的质量比.
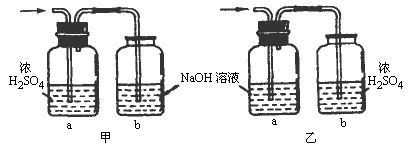
(1)使用哪一套装置得不到正确的结果?请说明原因.
(2)使用另一套装置虽然可以得出正确结果,但需要简化.请你帮他设计一个简化的装置(用文字说明或绘出简图均可).
查看习题详情和答案>> 喷泉是一种常见的自然现象,其产生的原因是存在压强差.在化学实验中经常也可以形成美丽的喷泉.
喷泉是一种常见的自然现象,其产生的原因是存在压强差.在化学实验中经常也可以形成美丽的喷泉.